El futuro de la terapia génica
Farmazian doktorea. Biofarmazia, Farmakozinetika eta Farmazia-teknologiako irakasle kolaboratzailea
Farmazia Fakultatea UPV-EHU, Vitoria-Gasteiz
El concepto de terapia génica es relativamente sencillo y sencillo: una copia adecuada de un gen se entrega a un paciente para corregir su trastorno patológico, es decir, el ADN actúa como medicamento en la terapia génica. Sin embargo, llevar a cabo con éxito este concepto no es nada fácil. Es muy difícil insertar una copia adecuada de un gen en un lugar concreto de una célula.
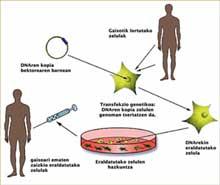
La corrección y transferencia de copias de ADN a células apropiadas se realiza en muchos casos con virus. Para muchos virus esta es la vía de provocar una infección: incorporan al ADN celular de la víctima su información genética para poder reproducirse. En la terapia génica, los investigadores han querido aprovechar esta capacidad intrínseca de ciertos virus, pero en este caso para introducir un gen curativo en el ADN de la ‘víctima’.
A principios de la década de los 90, debido a los prometedores ensayos en animales de laboratorio, varios grupos de investigación de París, Londres y Milán comenzaron a realizar ensayos de terapia génica con humanos. El objetivo era curar el mal de los niños conocidos como niños de burbujas. Estos niños deben vivir completamente aislados del medio, ya que debido a una inmunodeficiencia, las células que intervienen en la respuesta inmunológica del cuerpo no se desarrollan adecuadamente. En consecuencia, cualquier enfermedad común puede causar la muerte.
Desgraciadamente no hay medicamentos para curar esta grave enfermedad. El único tratamiento sería el trasplante de médula ósea de donantes con las mismas características genéticas. Sin embargo, la tasa de eficacia de esta última solución es escasa (30%) y presenta un riesgo de alteraciones inmunológicas severas.
XX. En los ensayos clínicos realizados a finales del siglo XX participaron un total de 18 niños. Los ensayos de terapia génica se realizaron con retrovirus, algunos de ellos que integran su información genética en el ADN de la víctima. Los resultados fueron muy satisfactorios desde el principio. 17 niños recuperaron la función del sistema inmunológico y hoy en día están vivos y sanos.
Como resultado de estos resultados, además de verificar el potencial terapéutico de la terapia génica, se pusieron en marcha nuevos ensayos clínicos y se impulsó la creación de industrias biotecnológicas.
Lamentablemente, los dos niños que participaron en el ensayo francés desarrollaron a finales de 2002 una enfermedad similar a la leucemia y, de repente, el optimismo generado en torno a esta tecnología se convirtió en preocupación y nerviosismo. De hecho, muchos recordaban la muerte de un joven en otro ensayo en 1999.
Durante este período, la sobredosis de partículas víricas y la respuesta inmunológica posterior violenta fueron los responsables del resultado trágico. La aparición de leucemia era una noticia muy grave, por un lado, porque en todas las investigaciones realizadas hasta entonces con animales de laboratorio nunca se había tenido conocimiento de una alteración de este tipo y, por otro lado, se volvía a cuestionar la seguridad de la terapia génica.
Las consecuencias a corto plazo fueron muy duras para el futuro de la terapia génica. Hay que tener en cuenta que garantizar la seguridad de los pacientes es el primer requisito que debe cumplir cualquier nuevo tratamiento. Las asociaciones reguladoras de la sanidad de varios países prohibieron inmediatamente más ensayos clínicos y algunas empresas de terapia génica abandonaron los retrovirus y comenzaron a trabajar con otros virus que ofrecían mayor seguridad.
Éxitos y fracasos de la terapia génica
No cabe duda de que la terapia génica es eficaz para el tratamiento de las enfermedades que provocan la inmunodeficiencia. Las células obtenidas de las médula ósea de los pacientes son tomadas y transformadas con virus que tienen incorporadas las copias adecuadas del ADN. Una vez que las copias del ADN se han integrado en los genomas de las células, se obtienen células maduras y funcionales que se inyectan a los pacientes para curarlas. La aparición de la leucemia indicaba que algo había ido mal en ese proceso, pero ¿qué?
La respuesta la encontró el equipo de investigación de Von Kalle, un proceso conocido como “vacunación mutagénica”. En este proceso, al integrarse en el genoma de las células, el retrovirus cambió unos genes indeseables, entre ellos el gen LMO2 que participa en los cánceres infantiles. Esto puso de manifiesto que el fenómeno a controlar es el lugar exacto en el que los virus se integran en los genomas de las células para evitar que en el futuro se repitan estas alteraciones. Pero, ¿cómo se puede conseguir tanta precisión si al paciente se le suministran millones de células curadas en el laboratorio?
Buscando soluciones
Todos los expertos consideran que el futuro de la terapia génica debe basarse en la seguridad y la eficacia. Para lograrlo, se necesitan vectores de mayor seguridad que permitan integrar la copia del ADN únicamente en las células deseadas, con seguridad, eficacia y precisión.
Hay quien opina que los transportadores que no se incorporan al genoma pueden ser una buena opción, pero otros creen que los únicos virus que son útiles para producir cambios a largo plazo en las células son los retrovirus. De cara a la seguridad también se pueden utilizar virus que llevan ‘genes suicidas’. Estos virus, si se integran en células inadecuadas o se multiplican incontroladamente, pueden inactivarse después de administrar un fármaco al paciente.
Por otro lado, en los últimos años se han optimizado los llamados sistemas de expresión génica de primera generación. En estos sistemas, los transportadores responden a estímulos concretos: medicamentos, calor, radiación, cantidad de glucosa o oxígeno, etc.
Por ejemplo, el sistema de expresión génica integrado en un paciente con diabetes tendrá como objetivo producir insulina, pero esta producción debe estar muy controlada para evitar hiperglucemias e hipoglucemias. Con estos nuevos sistemas se puede diseñar un sistema que produzca más o menos insulina en función del nivel de glucosa, de forma que la insulina sólo se suelte cuando lo necesita el paciente y además a la dosis necesaria.
También se está investigando un sistema similar de tratamiento de la anemia, que produce eritropoyetina (EPO) en función del nivel de oxígeno en la sangre.
Junto a ello, es imprescindible mejorar los controles de calidad disponibles para el estudio de las células transformadas con ADN. El desarrollo de técnicas moleculares y genéticas adecuadas permitiría analizar muestras de haces celulares modificados en cada turno. Lo mejor sería estudiar todas las células, porque cada una tiene sus propias características, pero hoy en día parece imposible, ya que se tarda mucho tiempo y los ensayos nunca finalizarían.
La recuperación de la confianza perdida tardará en recuperarse, pero con el tiempo, los pacientes de terapia génica han producido sistemas más eficientes y, sobre todo, más seguros. Aunque queda mucho trabajo por hacer, se puede afirmar que la terapia génica todavía no ha escrito su último capítulo.
BIBLIOGRAFÍA
- Orive, G. y otros ‘Terapia génica, de la
esperanza a la
realidad’ Elhuyar Zientzia eta Teknika, 170:27-32 (2001).
Cavazzana-Calvo, M. y otros ‘Gene
therapy of human severe combined inmunodeficiency (SCID)-X1 disease’
Science, 288:669-672 (2000).
Check, E.
‘Second cancer case halts gene-therapy trials’
Nature, 421:305 (2003).