Adipocitos, obesidade e saúde: relación máis complexa do esperado
Nutrizioa eta Obesitatea ikerketa taldea (EHU) CIBEROBN eta BIOARABA Osasun Institutuak
Nutrizioa eta Obesitatea taldea, EHU. CIBERobn, Carlos III Osasun Institutua. BIOARABA Osasunaren Ikerketa Zentroa
Pero empecemos polo principio. A obesidade é una enfermidade crónica caracterizada por unha acumulación excesiva de graxa que pode ser prexudicial paira a saúde. A pesar de tratarse dunha enfermidade multifactorial, os hábitos alimenticios e os factores ambientais considéranse como factores principais (estilo de vida sedentario e inxestión enerxética excesiva) [1]. O desenvolvemento da obesidade require un desequilibrio entre o consumo e o gasto enerxético, que se alarga no tempo. Este exceso de enerxía acumúlase nas unidades funcionais do tecido adiposo, adipocitos, en forma de triglicéridos, mediante dous mecanismos: a hipertrofia dos adipocitos (aumento de tamaño dos adipocitos paira acumular excedentes enerxéticos) e a hiperplasia dos adipocitos (aumento do número de adipocitos). A pesar de que desde hai tempo coñécese o papel que desempeñan os adipocitos na acumulación de enerxía, non fixemos máis que tomar conciencia da importancia que teñen estas células de tecido adiposo no mantemento da homeostasis metabólica do corpo [2].
En xeral, a capacidade de hipertrofia dos adipocitos relaciónase coa obesidade que se desenvolve na idade adulta, mentres que a hiperplasia considerouse como o mecanismo impulsor da obesidade infantil e xuvenil. De feito, até hai pouco pensábase que o número de adipocitos dun tecido graso era limitado e mantíñase constante desde a infancia até a madurez [3]. Con todo, en estudos recentes con roedores observouse que na idade adulta tamén se producen novos adivenitos ao abusar da enerxía. Estes novos adipocitos xorden da diferenciación dos adipocitos inmaturos e participan na difusión do tecido adiposo (hiperplasia) [4]. Pero, a pesar diso, que relación teñen coa saúde a hipertrofia e hiperplasia dos adipocitos?
Pois grande. Cando se produce una hipertrofia dos adipocitos, os adipocitos van crecendo de tamaño até chegar a tocarse. Nesta situación, a difusión do osíxeno tamén está obstruida e os adipocitos sofren un estado de hipoxia [5]. Doutra banda, a estes adivenitos nos que se atopan hipertrofiados engádense tamén os macrófagos inflamatorios. Así, o tecido adiposo segrega citoquinas inflamatorias ao sangue, como as interleucinas 6 e 8 (IL-6 e IL-8), a proteína 1 monocitaria (MCP1) e o factor de necrosis tumoral (TNF) [6]. Todos estes procesos darán lugar a unha inflamación crónica a baixo nivel que provocará alteracións no funcionamento normal dos adipocitos (Figura 1). Por unha banda, intensifícase a lipólisis en estado basal dos adipocitos (mobilización de graxas de reserva) e libéranse máis acedos grasos libres ao sangue. Estes ácidos grasos libres acumularanse en órganos e tecidos distintos do tecido adiposo, en forma de triglicéridos, principalmente en fígado e músculos, producindo o que se denomina lipotoxicidad. Algúns estudos demostraron que os maiores niveis de ácidos grasos libres asócianse ao desenvolvemento da resistencia á insulina e o esteatosis hepática (acumulación excesiva de graxa no fígado) [7]. Por outra banda, a produción de axentes inflamatorios do citoquino anteriormente mencionado impedirá a adipogénesis. En consecuencia, a diferenciación dos adipocitos inmaturos será máis limitada e xeraranse menos adipocitos novos [8]. Todos estes feitos conducirannos ao contexto que se explica ao comezo deste parágrafo, entrando nun círculo vicioso, aparentemente sen solución.
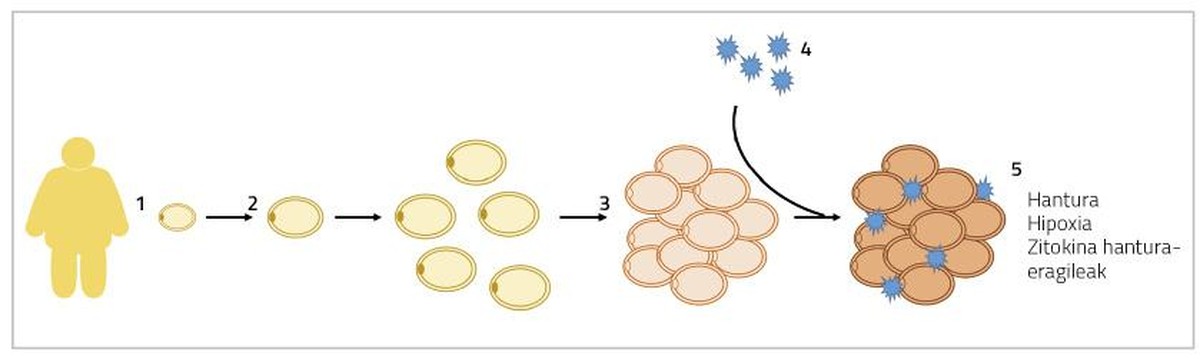
En caso de hiperplasia dos adipocitos, os excedentes enerxéticos acumularanse en novos adivenitos, diminuíndo a presenza de adivenitos hipertrofiados. En consecuencia, o fluxo de citoquinas inflamatorias tamén diminuirá [5]. Por outra banda, relacionouse a formación de adipocitos de menor tamaño coa angiogénesis (formación de novos vasos sanguíneos), que evitará a hipoxia dos adipocitos e a inflamación do tecido adiposo asociado [9]. Neste sentido, observouse que os ratos afectados xeneticamente pola adipogénesis indefinida da porcentaxe de graxa son metabolicamente sans cando se alimentan de dietas de engorde. Nos seres humanos atopouse algo parecido.
De feito, as porcentaxes adipocitos de graxa en persoas con síndrome metabólico presentan una infiltración de hipertrofia, hipoxia e macrófagos; e, doutra banda, no tecido adiposo de persoas obesas e metabolicamente sas, describíronse adipocitos de menor tamaño e maior número de vasos sanguíneos (Figura 2) [2]. Por tanto, una solución ao problema pode ser provocar a adipogénesis nas persoas obesas. Deste xeito, estas persoas desenvolverían menores adipocitos e, en consecuencia, terían menor risco de padecer enfermidades metabólicas.
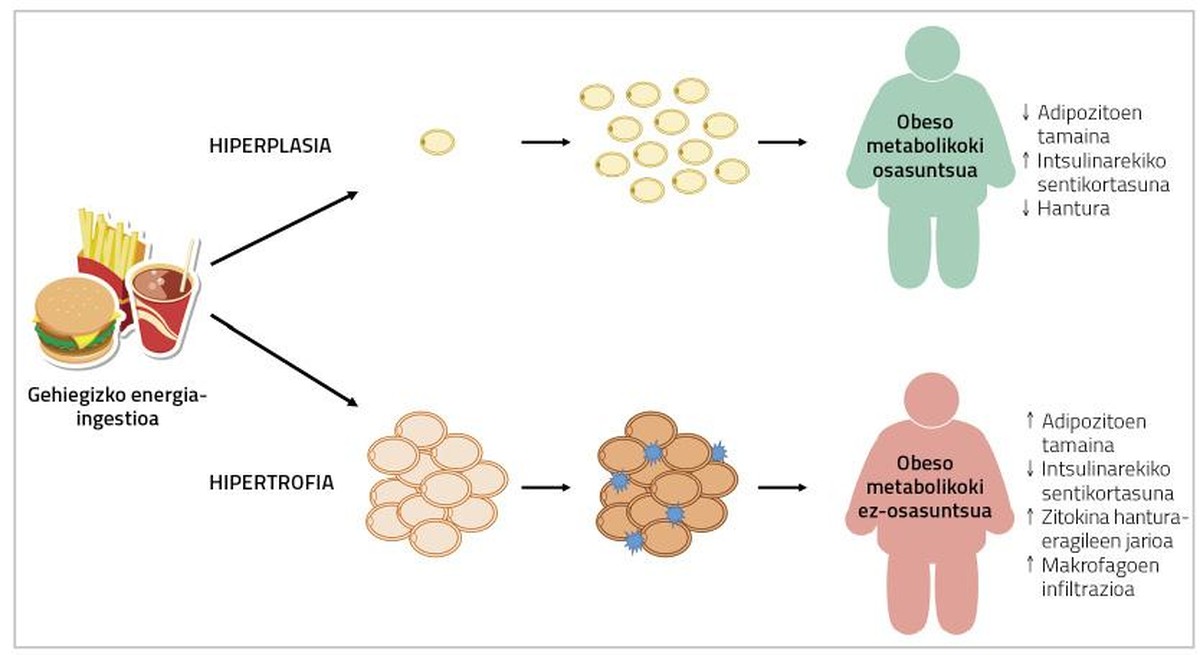
Desgraciadamente, non é tan simple. De feito, segundo o tecido graso, os adipocitos que se poden atopar nel son diferentes. Por exemplo, o tecido graso visceral aumenta por hipertrofia, mentres que o tecido adiposo subcutáneo tende a hiperplasia. Ademais, a capacidade dos depósitos de graxa paira a adipogénesis difire dos estímulos que o inducen [2]. Nos estudos realizados cos roedores observouse que a activación da adipogénesis xeneticamente inducida provoca o desenvolvemento de adipocitos de menor tamaño nas cepas transxénicas (sen influír no contido de graxa corporal nin no peso) e que se converten en metabolicamente máis sans [7]. No caso dos seres humanos, a pesar de non realizar este tipo de traballo, describiuse algo parecido co medicamento tiazolidinediona (DXT) utilizado paira o tratamento da diabetes tipo 2. Isto débese a que, ademais de mellorar a diabetes, produce un aumento do tecido adiposo, una diminución do tamaño dos adipocitos locais e una diminución do fluxo de axentes inflamatorios da citoquina. A diferenza dos animais, a mellora metabólica que producen estes fármacos coincide co aumento do peso corporal [10]. Con todo, aínda queda por ver si é posible producir a adipogénesis en humanos adultos sen efectos nocivos sobre o peso corporal ou outros procesos metabólicos. Neste contexto hai que destacar que moitos estudos realizados até a data ao redor da adipogénesis dirixíronse a inhibir a propia adipogénesis. De feito, ao probar moléculas e compostos que poden ser adecuados paira tratar a obesidade, estúdase a súa capacidade paira inhibir a adipogénesis. E a verdade é que iso ten o seu sentido: se se producen menos adivenitos, dificultarase a difusión do tecido graso (e por tanto a obesidade).
Como se pode observar, aínda queda moito camiño por percorrer paira lograr un tratamento farmacolóxico efectivo da obesidade. A pesar de que o concepto de obeso é aparentemente atractivo (e razoable), metabolicamente san, non existe un consenso absoluto entre os investigadores sobre as consecuencias paira a saúde desta situación. Comprender ben o desenvolvemento de tecidos grasos anatomicamente diferentes pode axudar a modificar a distribución de graxa corporal ou o funcionamento do tecido adiposo en persoas obesas. Con todo, aínda queda claro que a prevención é a intervención máis eficaz contra a obesidade.
Bibliografía
Traballo presentado aos premios CAF-Elhuyar.






