Inmunoterapia CAR: una porta á esperanza
A oncohematóloga Izaskun Zeberio Etxetxipia fala con orgullo sobre a súa obra. Tras a súa investigación e traballo no Hospital de Navarra e no Centro de Cancro Memorial Sloan-Kettering (Nova York), desde 2014 atópase no Hospital Universitario de Donostia. É o referente da Unidade Linfoma e explica que prestan atención diúrna a pacientes sen ingreso: “Procuramos evitar o ingreso xa que paira o paciente é moito máis agradable e tenra”.
É testemuña directa da evolución que está a experimentar nos tratamentos e vive de primeira man a porta aberta pola inmunoterapia. Explica que o tratamento clásico é a quimioterapia: “Paira comprendela facilmente, as células cancerosas son células que se reproducen máis do suficiente e non morren, e a quimioterapia curta o ciclo celular”.
En inmunoterapia o foco é outro: en lugar de pór a forza na destrución da célula cancerígena, colócase no reforzo ou aumento do sistema inmunitario. “Precisamente a iso déronlle o Premio Nobel de Medicamento de 2018”, lembrou Zeberio. “Grazas a estes estudos sabemos que as células tumorales ocúltanse paira evitar que o sistema de vixilancia do sistema inmunitario detecte e destrúa. Envían una sinal paira crear una zona de protección e entregaron o Premio Nobel a aqueles que desenvolveron anticorpos monoclonales que bloqueaban eses sinais”.
Hoxe en día séguense utilizando anticorpos monoclonales pero, ademais, as células CAR adquiriron una gran forza: “Espertaron una gran esperanza. Una esperanza baseada en evidencias, non demasiado”, afirmou.
Segundo el, levan máis de vinte anos investigando con células CAR e realizáronse numerosos ensaios clínicos, sobre todo en EEUU e China, que xa chegaron á clínica: “Desde hai un ano é posible aplicar esta terapia no sistema sanitario público”.
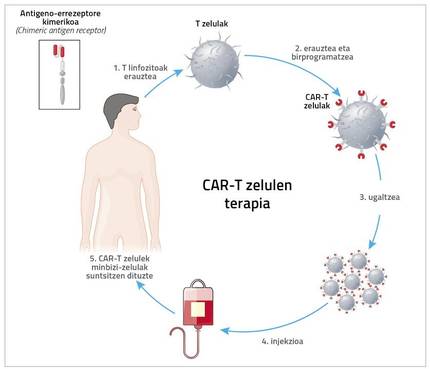
O núcleo é una quimera
O acrónimo CAR significa chimeric antígeno receptor receptor químico. Paira iso extráese ao paciente unhas células do sistema inmunitario. “Normalmente trátase de células T, polo que se denomina terapia CAR-T. Pero se pode facer con outras células, como as NK. Cristina Egizabal Argaiz, do Centro de Transfusións e Tecidos Humanos da Comunidade Autónoma do País Vasco, está a realizar con eles estudos moi interesantes”, explica Zeberio.
Con todo, o que de momento chegou á aplicación clínica é a terapia de células CAR-T. Por tanto, ao paciente extráenselle as células T e, mediante un proceso moi complexo e caro, introdúcese un novo receptor a esta célula T. Grazas a este receptor, a célula T ten una gran capacidade de detección e destrución de antígenos de células cancerosas.
E de aí o nome. Zeberio: “Kimera é un monstro da mitoloxía grega formado por fragmentos de cabra, león e dragón. Pois ben, no receptor quimérico realízase una mestura de linfocitos B e T. A parte do linfocito B detecta o antígeno e a do linfocito T penetra na célula e dá sinal de activación e reprodución”.
Esta tecnoloxía pódese deseñar paira diferentes antígenos. Zeberio indica que en hematología predomina un antígeno, o CD19, polo que as células CAR-T que se utilizan son anti. “Por tanto, o maior desenvolvemento e os mellores resultados obtivéronse nos cancros da liña B onde se expresa o antígeno CD19. Especialmente na leucemia aguda linfoblástica, é dicir, na leucemia infantil. Ademais, todos os linfomas non Hodgkin B (90% dos linfomas que tratamos) expresan o CD19”.
Da investigación á clínica
En base aos resultados dos ensaios clínicos, en 2017 a Axencia Estadounidense de Alimentos e Medicamentos, FDA, aprobou o uso comercial das células CAR-T e foi aprobada un ano despois pola Axencia Europea de Medicamentos, a SEM. En España, desde novembro de 2018 é posible utilizar a terapia nos centros.
“É moi importante elixir ben aos pacientes que realmente se benefician”, advirte Zeberio. “É certo que xerou unhas expectativas moi elevadas, xa que estes pacientes non teñen outra alternativa, pero hai que ter en conta que hai que ter en conta que hai que elixir ben a aqueles pacientes aos que lles vai a beneficiar o tratamento, porque o procedemento é moi complicado, moi caro e pode ter efectos secundarios graves. Non é paira todos os pacientes e temos que decidir con moito coidado a quen entregalo”.
“Ademais, non hai que esquecer que a terapia ten efectos secundarios significativos”. De feito, ao paciente primeiro extráenselle os linfocitos T e envíanse a EEUU. Alí, mediante uns retrovirus ou lentivirus, introducen un receptor aos linfocitos. Logo reprodúcense no laboratorio e son enviados de volta. Mentres tanto, poden transcorrer 5 semanas nas que hai que analizar como tratar ao paciente. Una vez chegadas as células incorpóranse ao paciente.
Cando recibe aos pacientes, Zeberio explica que hai toxicidade durante as dúas primeiras semanas: “Por iso, o paciente debe estar en bo estado. Hai que ter en conta que existe una loita entre os linfocitos T que recibiu e as células cancerosas e outras células do paciente. Prodúcese una tormenta de citoquinas que pode provocar shock e insuficiencia respiratoria. Entón hai que atender ao paciente en coidados especiais”.
Non é de estrañar, por tanto, subliñar que deben actuar con responsabilidade. “Non hai que esquecer que esta terapia se aceptou con moi poucos casos. Dado que os seus resultados son tan satisfactorios en pacientes que non teñen outra alternativa, saltou moi rápido dos ensaios dos investigadores á práctica hospitalaria, pero debemos medir con rigor a seguridade e a eficacia. Dalgunha maneira é coma se estivesen na 3ª fase clínica”. En definitiva, a prioridade é curar aos pacientes, pero ao mesmo tempo están a aprender e mellorando.
Ademais da tormenta de citoquinas, puntualiza que ás veces se produce neurotoxicidad. Aínda non entenden moi ben o mecanismo, pero hai pacientes que sofren neurotoxicidad, desde a confusión, até a dificultade de escribir ou falar, pasando polo coma. Paira facer fronte a estes riscos é evidente que o paciente debe estar forte no momento de recibir os linfocitos modificados.
Di Zeberio: “Os médicos debemos medir beneficios e riscos, e só aplicaremos o tratamento se o beneficio é maior que o risco. Non paira todos”.
Criterios estritos, plan detallado
En España, o Plan de Terapias Avanzadas establece os criterios paira a implantación do tratamento CAR-T. O obxecto do citado plan é, literalmente, o seguinte: Organizar de forma planificada, equitativa, segura e eficaz o uso dos medicamentos CAR e actualmente dos CAR-T no sistema sanitario público, así como a súa investigación e produción no ámbito académico do sistema sanitario público en condicións que garantan estándares de calidade, seguridade e eficiencia.
Zeberio ve con bos ollos o plan. Di que é moi importante centralizar os casos e que os grupos estean ben preparados. A experiencia tamén é necesaria: “Non é a túa experiencia. O traballo en equipo é fundamental en medicamento e nestas terapias máis que en ningún outro sitio. Os pacientes reciben tratamento no servizo de hematología, pero inclúe o traballo de profesionais de diferentes servizos, todos eles con formación de enfermeiras, intensivistas, neurólogos, infecciosos, inmunolos... É dicir, necesítase un equipo interdisciplinar, ben formado”.
Por iso, son necesarios criterios rigorosos. Segundo eles, en España hai oito centros designados paira incluír terapias de células CAR-T, que non son poucos en relación á poboación europea. En Euskal Herria non hai ningunha, pero Zeberio considera que non hai nada malo: “Hai que facer as cousas ben. Na Comunidade Autónoma do País Vasco existe un plan e está decidido que no futuro o Hospital Universitario de Donostia sexa un centro de terapias CAR. Estamos a nos preparar paira iso”.
Mentres tanto, o seguimento dos pacientes realízase no propio Hospital Universitario de Donostia-San Sebastián, pero son enviados a tratamento a un destes oito centros. Polo momento, os pacientes opcionais son aqueles que presentan tumores da liña B con antígeno CD19, pero Zeberio espera que co tempo póidase utilizar esta tecnoloxía noutros tumores como os tumores sólidos. Cada vez ábrese máis a porta á esperanza.