Immunothérapie CAR: une porte à l'espoir
L'oncohématologue Izaskun Zeberio Etxetxipia parle fièrement de son œuvre. Après sa recherche et son travail à l'hôpital de Navarre et au Centre de Cancer Memorial Sloan-Kettering (New York), il se trouve depuis 2014 à l'hôpital universitaire de Donostia. Il est la référence de l'unité lymphome et explique qu'ils fournissent des soins diurnes aux patients sans revenu: « Nous essayons d’éviter l’entrée car le patient est beaucoup plus agréable et tendre. »
Il est témoin direct de l'évolution qu'il subit dans les traitements et vit de première main la porte ouverte par l'immunothérapie. Il explique que le traitement classique est la chimiothérapie: « Pour la comprendre facilement, les cellules cancéreuses sont des cellules qui se reproduisent assez et ne meurent pas, et la chimiothérapie coupe le cycle cellulaire. »
En immunothérapie, le foyer est un autre: au lieu de mettre la force dans la destruction de la cellule cancérogène, il est placé dans le renforcement ou l'augmentation du système immunitaire. « C’est précisément à cela qu’ils ont reçu le Prix Nobel de médecine 2018 », a rappelé Zeberio. « Grâce à ces études, nous savons que les cellules tumorales sont cachées pour empêcher le système de surveillance du système immunitaire de détecter et de détruire. Ils envoient un signal pour créer une zone de protection et remettent le prix Nobel à ceux qui ont développé des anticorps monoclonaux qui bloquaient ces signaux ».
Aujourd'hui, les anticorps monoclonaux sont encore utilisés, mais en outre, les cellules CAR ont acquis une grande force: « Ils ont suscité un grand espoir. Une espérance basée sur des preuves, pas trop », a-t-il affirmé.
Selon lui, il a fait des recherches sur les cellules CAR depuis plus de vingt ans et de nombreux essais cliniques ont été réalisés, notamment aux États-Unis et en Chine, qui sont déjà arrivés à la clinique : « Depuis un an, il est possible d’appliquer cette thérapie dans le système sanitaire public. »
Le noyau est une chimère
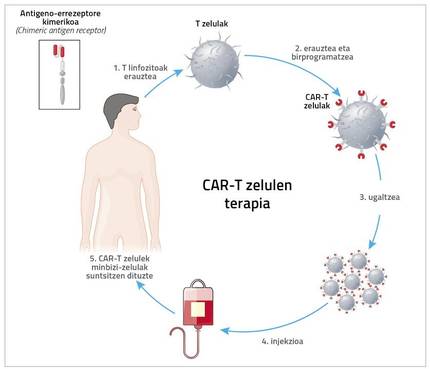
L'acronyme CAR signifie antigène chimeric récepteur chimique récepteur. Pour cela, le patient est extrait des cellules du système immunitaire. “Il s’agit normalement de cellules T, c’est pourquoi on appelle thérapie CAR-T. Mais il peut être fait avec d'autres cellules, comme les NK. Cristina Egizabal Argaiz, du Centre de Transfusions et de Tissus Humains de la Communauté Autonome du Pays Basque, mène avec eux des études très intéressantes », explique Zeberio.
Cependant, ce qui est arrivé pour le moment à l'application clinique est la thérapie de cellules CAR-T. Le patient est donc extrait des cellules T et, par un processus très complexe et coûteux, un nouveau récepteur est introduit à cette cellule T. Grâce à ce récepteur, la cellule T a une grande capacité de détection et de destruction des antigènes de cellules cancéreuses.
Et d'où le nom. Zeberio: « Kimera est un monstre de la mythologie grecque composé de fragments de chèvre, de lion et de dragon. Dans le récepteur chimérique, un mélange de lymphocytes B et T est produit. La partie du lymphocyte B détecte l'antigène et celle du lymphocyte T pénètre dans la cellule et donne un signal d'activation et de reproduction ».
Cette technologie peut être conçue pour différents antigènes. Zeberio indique qu'en hématologie prédomine un antigène, le CD19, de sorte que les cellules CAR-T utilisées sont anti. « Par conséquent, le plus grand développement et les meilleurs résultats ont été obtenus dans les cancers de la ligne B où l’antigène CD19 est exprimé. Surtout dans la leucémie aiguë lymphoblastique, à savoir dans la leucémie infantile. En outre, tous les lymphomes non hodgkiniens B (90% des lymphomes que nous traitons) expriment le CD19 ».
De la recherche à la clinique
Sur la base des résultats des essais cliniques, en 2017, l'Agence américaine des aliments et des médicaments, la FDA, a approuvé l'utilisation commerciale des cellules CAR-T et a été approuvée un an plus tard par l'Agence européenne des médicaments, la SEM. En Espagne, depuis novembre 2018, il est possible d'utiliser la thérapie dans les centres.
« Il est très important de bien choisir les patients qui en bénéficient », avertit Zeberio. « Il est vrai qu’il a généré des attentes très élevées, puisque ces patients n’ont pas d’autre alternative, mais il faut garder à l’esprit qu’il faut bien choisir les patients qui bénéficieront du traitement, parce que la procédure est très compliquée, très cher et peut avoir des effets secondaires graves. Ce n’est pas pour tous les patients et nous devons décider avec beaucoup de soin qui le livrer.»
“En outre, il ne faut pas oublier que la thérapie a des effets secondaires significatifs”. En fait, le patient est d'abord extrait les lymphocytes T et envoyé aux États-Unis. Là, par des retrovirus ou lentivirus, ils introduisent un récepteur aux lymphocytes. Puis ils sont reproduits dans le laboratoire et sont renvoyés. En attendant, il peut s'écouler 5 semaines pour analyser comment traiter le patient. Une fois arrivés, les cellules sont incorporées au patient.
Quand il reçoit les patients, Zeberio explique qu'il y a toxicité pendant les deux premières semaines: « Le patient doit donc être en bon état. Notez qu'il existe une lutte entre les lymphocytes T que vous avez reçus et les cellules cancéreuses et d'autres cellules du patient. Une tempête de cytokines peut provoquer un choc et une insuffisance respiratoire. Il faut alors soigner le patient dans des soins spéciaux».
Il n'est pas surprenant, par conséquent, de souligner qu'ils doivent agir avec responsabilité. « Il ne faut pas oublier que cette thérapie a été acceptée avec très peu de cas. Comme ses résultats sont si satisfaisants chez les patients qui n'ont pas d'autre alternative, il a sauté très vite des essais des chercheurs à la pratique hospitalière, mais nous devons mesurer avec rigueur la sécurité et l'efficacité. D’une certaine façon, c’est comme s’ils étaient dans la 3ème phase clinique.» En définitive, la priorité est de soigner les patients, mais en même temps ils apprennent et améliorent.
En plus de la tempête de cytokines, il note que la neurotoxicité se produit parfois. Ils ne comprennent pas encore très bien le mécanisme, mais il y a des patients souffrant de neurotoxicité, de la confusion, à la difficulté d'écrire ou de parler, en passant par le coma. Pour faire face à ces risques, il est évident que le patient doit être fort au moment de recevoir les lymphocytes modifiés.
Zeberio dit: « Les médecins doivent mesurer les avantages et les risques, et nous appliquerons uniquement le traitement si le bénéfice est supérieur au risque. Pas pour tous. »
Critères stricts, plan détaillé
En Espagne, le Plan de thérapies avancées définit les critères pour l'implantation du traitement CAR-T. L'objet de ce plan est littéralement ce qui suit: Organiser de manière planifiée, équitable, sûre et efficace l’utilisation des médicaments CAR et actuellement des CAR-T dans le système sanitaire public, ainsi que leur recherche et production dans le domaine académique du système sanitaire public dans des conditions garantissant des normes de qualité, sécurité et efficacité.
Zeberio voit avec de bons yeux le plan. Il dit qu'il est très important de centraliser les cas et que les groupes soient bien préparés. L'expérience est également nécessaire: « Ce n’est pas votre expérience. Le travail d'équipe est fondamental en médecine et dans ces thérapies plus que partout ailleurs. Les patients reçoivent un traitement dans le service d'hématologie, mais comprend le travail de professionnels de différents services, tous avec la formation d'infirmières, intensives, neurologues, infectieux, immunolos... C’est-à-dire qu’il faut une équipe interdisciplinaire, bien formée».
Des critères rigoureux sont donc nécessaires. Selon eux, en Espagne, huit centres sont désignés pour inclure des thérapies cellulaires CAR-T, qui ne sont pas rares par rapport à la population européenne. Dans Euskal Herria il n'y a pas, mais Zeberio estime qu'il n'y a rien de mal: « Il faut bien faire les choses. Dans la Communauté Autonome du Pays Basque, il existe un plan et il est décidé que l'Hôpital Universitaire de Donostia sera un centre de thérapies CAR. Nous nous préparons à cela. »
Pendant ce temps, le suivi des patients est effectué dans l'hôpital universitaire de Saint-Sébastien lui-même, mais ils sont envoyés au traitement à l'un de ces huit centres. Pour le moment, les patients optionnels sont ceux qui présentent des tumeurs de la ligne B avec antigène CD19, mais Zeberio espère qu'avec le temps cette technologie peut être utilisée dans d'autres tumeurs comme les tumeurs solides. La porte à l'espérance s'ouvre de plus en plus.