Titanio, coxín estabilizador interior de baterías
As baterías de ion litio (VOL) foron clave no desenvolvemento de dispositivos portátiles, vehículos eléctricos e enerxías renovables. Hoxe en día, con todo, a indisponibilidad do litio, a desigual distribución do litio no mundo e os danos ambientais que se derivan da utilización de níquel (Nin) e cobalto (Co) neste tipo de baterías pon en dúbida esta revolución.
Debido ao desenvolvemento dos últimos anos, o custo e a dispoñibilidade de materias primas son importantes, polo que se comprobou que as baterías de sodio ion (NIB) poden chegar a ser sustitutivas das OPS. Así, os óxidos laminares de sodio e manganeso (Na e Mn respectivamente), sen Co e sen Nin, fixéronse moi interesantes.
Este interese débese en gran medida aos procesos electroquímicos favorables e ao feito de que o principal metal de transición electroactivo sexa o Mn. En definitiva, o Mn é un elemento alcanzable, limpo e barato que, con máis dunha situación de oxidación, permite a síntese de compostos paira a adaptación desexada do potencial redox (o par máis utilizado é Mn3+/Mn4+).
Púidose comprobar que a dopaxe destes óxidos laminos con titanio (Ti) mellora a durabilidad das baterías e pode provocar un mellor mantemento da capacidade en cada ciclo de carga/descarga. Pero antes de explicar o papel que xoga o titanio niso, vexamos cal é a estrutura dos óxidos laminados e cales son os seus principais problemas.
Compoñentes sándwich
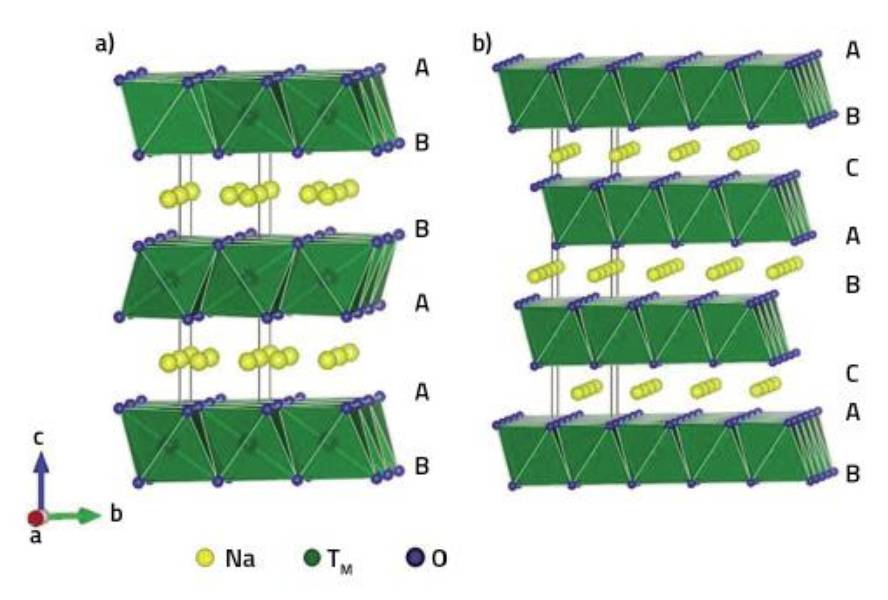
Nos óxidos laminados utilizados paira os cátodos de baterías de sodio ion pódense distinguir capas de osíxeno, metais de transición e sodio. Os metais de transición localízanse nos ocos octaédricos entre as dúas capas de osíxeno, ocupando o resto de ocos interoxigénicos. Así, en función dos ocos nos que se localizan os átomos de sodio, distínguense estrutúralas tipo P e tipo Ou: Denomínanse P cando os átomos de sodio atópanse en prismas trigonales e Ou cando están en ocos octaédricos. Tamén se utilizan números no nome que indican o número de capas de sodio necesarias paira describir toda a estrutura. Desta forma, pódense dispor de estruturas tipo P2, O2 e O3 dependendo da posición relativa das capas de osíxeno.
Estudos demostran que as estruturas P son máis apropiadas paira os cátodos das baterías que as estruturas Ou, xa que os átomos de sodio desprázanse máis facilmente dun prisma a outro que dun octaedro a outro. No entanto, en función das condicións e cantidade de sodio utilizados, prodúcense transformacións de P> Ou, o que limita o proceso de carga/descarga da batería.
Manganeso, elemento activo
Nos óxidos laminares de manganeso, o elemento activo é o Mn. É dicir, durante o proceso de carga/descarga da batería, cando o sodio extráense/introducen do óxido laminar, o manganeso capta/libera os electróns do sodio, converténdose en Mn3+/Mn4+. Este é o principal problema destes óxidos laminos. E é que, a diferenza de Mn4+, Mn3+ sofre una distorsión de Jahn-Teller (JT) debido á súa configuración electrónica. Como consecuencia diso, o octaedro formado polos seis osíxenos ao redor do manganeso alárgase e acurta, e tendo en conta que en cada ciclo de carga/descarga prodúcese a transformación de Mn3+{ Mn4+> Mn3+, o que afecta negativamente ao óxido laminar durante ciclos.
Paira facer fronte a este problema, os óxidos laminares dópanse con elementos inactivos, como o magnesio e o titanio, que non captan/liberan electróns durante o proceso de carga/descarga da batería. Neste sentido, investigadores de CIC EnergiGUNE realizamos un estudo baseado no composto Na2/3Fe0,2 Mn0.8O2, que é o óxido laminar de ferro e manganeso que obtén as condicións electroquímicas máis favorables. No estudo vimos que ao dopar este composto con distintas cantidades de titanio, a evolución da capacidade de ciclo a ciclo cambiaba. Recentemente, nun traballo publicado na revista Journal of Material Chemistry A, explicamos o papel do titanio neste sentido, combinando medicións electroquímicas, espectroscopía de absorción de raios X e cálculos teóricos utilizando a teoría da densidade funcional (DFT).
En resumo, pódese dicir que o titanio é capaz de absorber as distorsiones de octaedros dos metais activos da zona, neste caso o manganeso. É dicir, aínda que a configuración electrónica non produza distorsiones JT, o titanio é capaz de adaptar o seu octaedro ás distorsiones da contorna. En esencia, ao ser máis débil a unión titanio-osíxeno, adaptándose aos movementos da contorna, este metal compórtase na estrutura como un coxín capaz de dar estabilidade a toda a estrutura.
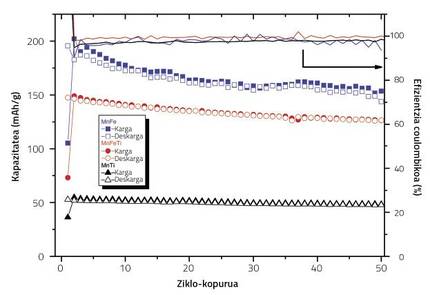
En calquera caso, a concentración de titanio debe coidarse adecuadamente. O estudo baseouse no Na2/3Fe0,2 Mn350O2, que é o que obtén a mellor condición electroquímica entre os óxidos laminados de ferro e manganeso. Na investigación utilizamos tres concentracións de titanio, das cales só se obtiveron resultados satisfactorios. En ausencia de titanio, a medida que se facían ciclos de carga/descarga, a capacidade do cátodo diminuía notablemente. Cando substituïamos todo o ferro do composto por titanio, a capacidade inicial diminuía considerablemente. En cambio, cando substituímos a metade do ferro por titanio, a capacidade inicial era adecuada, así como a súa evolución ciclo a ciclo. De feito, a medida que aumenta a concentración de titanio, aumenta a concentración de Mn3+ que sofren o estiramento/acortamiento dos seus octaedros, o que fai que a capacidade da batería sexa baixa desde o principio. Con todo, cando a concentración do dopante é menor, Mn3+ estará menos no composto, e ademais de ter una capacidade inicial máis alta, a coitela do titanio na estrutura permite manter mellor a capacidade ciclo a ciclo.
Como reflexo deste carácter, calculamos teoricamente os índices de distorsión de todos os metais de transición do composto (Fe, Ti, Mn3+ e Mn4+). Este índice indícanos canto se afasta dun octaedro regular formado por seis osíxenos ao redor de cada átomo do metal de transición.
Así, paira o tres compostos analizados, o catión Mn3+ era o que presentaba maior índice de distorsión. No outro extremo situábase Mn4+, o máis próximo a un octaedro regular. Isto é facilmente comprensible si temos en conta que o catión Mn3+ sofre distorsión JT pola súa configuración electrónica.
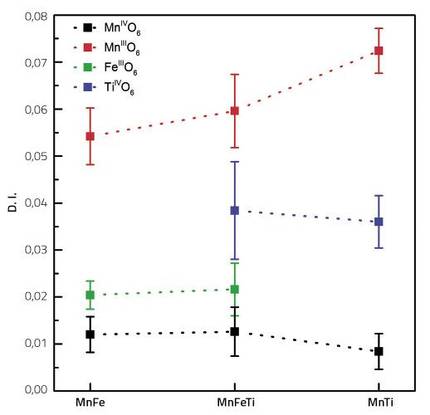
O máis rechamante é a diferenza entre Ti e Fe. O índice de distorsión do titanio é entre dous e tres veces superior ao do ferro. Basicamente, estes dous metais de transición non deberían presentar por si mesmos distorsiones, xa que a súa configuración electrónica non lles afecta. A distorsión destes dous metais inactivos é debida unicamente ás distorsiones dos octaedros circundantes. Así, o feito de que o índice de titanio sexa dous ou tres veces superior ao do ferro indica que o titanio adapta mellor as distorsiones da zona que o ferro. É dicir, se comparamos os compoñentes inactivos do cátodo cun coxín, o seu índice de distorsión indicaría o grao de flacidez do coxín. Canto maior sexa o índice de distorsión, máis flexible será o coxín, o que facilitará a absorción das irregularidades dos octaedros circundantes.
Paso a paso…
Naquel traballo puidemos comprobar que o titanio podería mellorar a duración das posibles baterías de sodio ion. É dicir, poderiamos cargar máis a miúdo o portátil ou o vehículo eléctrico que usase este tipo de baterías sen danar demasiado a capacidade da súa batería.
Con todo, leste é un pequeno paso máis no camiño das baterías de sodio ion. Está por ver como afectarían outros dopantes distintos do titanio. Por exemplo, púidose comprobar que ás veces se obteñen resultados moi interesantes incluso cando se utiliza zinc como dopador, o que aínda non se entende moi ben.
Así mesmo, nos óxidos laminares tipo P2, cando se detecta presenza de sodio en prismas que comparten una cara con octaedros de metais de transición, observouse que a transformación P2> O2 complícase. Isto facilita o proceso de carga/descarga da batería. Por tanto, ademais do dopante, haberá que ter en conta a función que pode ter a posición dos átomos de sodio.
En todas estas investigacións estamos involucrados diferentes grupos de investigación da liña de baterías de sodio ion de CIC EnergiGUNE.





