Titanio, cojín estabilizador interior de baterías
Las baterías de ion litio (VOL) fueron clave en el desarrollo de dispositivos portátiles, vehículos eléctricos y energías renovables. Hoy en día, sin embargo, la indisponibilidad del litio, la desigual distribución del litio en el mundo y los daños ambientales que se derivan de la utilización de níquel (Ni) y cobalto (Co) en este tipo de baterías ponen en duda esta revolución.
Debido al desarrollo de los últimos años, el coste y la disponibilidad de materias primas son importantes, por lo que se ha comprobado que las baterías de sodio ion (NIB) pueden llegar a ser sustitutivas de las OPS. Así, los óxidos laminares de sodio y manganeso (Na y Mn respectivamente), sin Co y sin Ni, se han hecho muy interesantes.
Este interés se debe en gran medida a los procesos electroquímicos favorables y al hecho de que el principal metal de transición electroactivo sea el Mn. En definitiva, el Mn es un elemento asequible, limpio y barato que, con más de una situación de oxidación, permite la síntesis de compuestos para la adaptación deseada del potencial redox (el par más utilizado es Mn3+/Mn4+).
Se ha podido comprobar que el dopaje de estos óxidos laminos con titanio (Ti) mejora la durabilidad de las baterías y puede provocar un mejor mantenimiento de la capacidad en cada ciclo de carga/descarga. Pero antes de explicar el papel que juega el titanio en ello, veamos cuál es la estructura de los óxidos laminados y cuáles son sus principales problemas.
Componentes sándwich
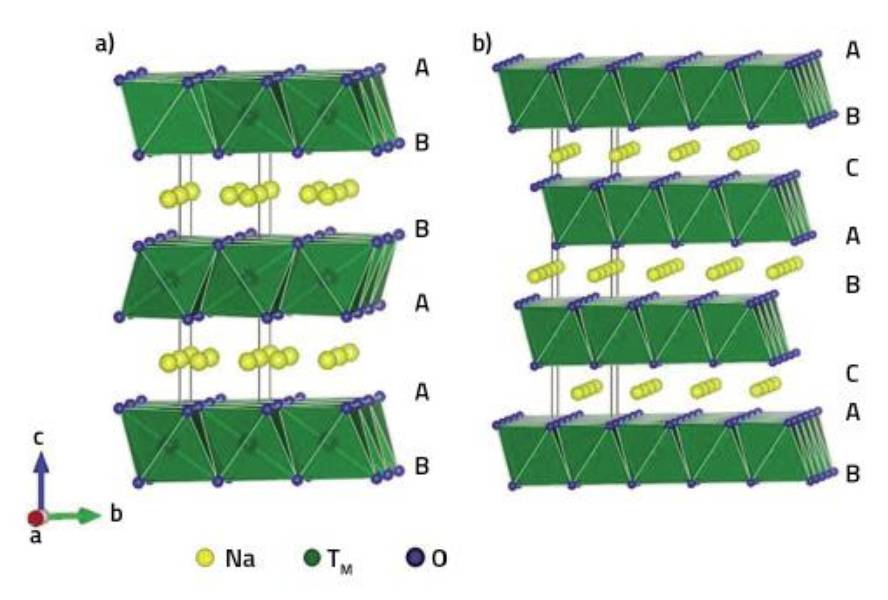
En los óxidos laminados utilizados para los cátodos de baterías de sodio ion se pueden distinguir capas de oxígeno, metales de transición y sodio. Los metales de transición se localizan en los huecos octaédricos entre las dos capas de oxígeno, ocupando el resto de huecos interoxigénicos. Así, en función de los huecos en los que se localizan los átomos de sodio, se distinguen las estructuras tipo P y tipo O: Se denominan P cuando los átomos de sodio se encuentran en prismas trigonales y O cuando están en huecos octaédricos. También se utilizan números en el nombre que indican el número de capas de sodio necesarias para describir toda la estructura. De esta forma, se pueden disponer de estructuras tipo P2, O2 y O3 dependiendo de la posición relativa de las capas de oxígeno.
Estudios demuestran que las estructuras P son más apropiadas para los cátodos de las baterías que las estructuras O, ya que los átomos de sodio se desplazan más fácilmente de un prisma a otro que de un octaedro a otro. No obstante, en función de las condiciones y cantidad de sodio utilizados, se producen transformaciones de P> O, lo que limita el proceso de carga/descarga de la batería.
Manganeso, elemento activo
En los óxidos laminares de manganeso, el elemento activo es el Mn. Es decir, durante el proceso de carga/descarga de la batería, cuando los sodio se extraen/introducen del óxido laminar, el manganeso capta/libera los electrones del sodio, convirtiéndose en Mn3+/Mn4+. Este es el principal problema de estos óxidos laminos. Y es que, a diferencia de Mn4+, Mn3+ sufre una distorsión de Jahn-Teller (JT) debido a su configuración electrónica. Como consecuencia de ello, el octaedro formado por los seis oxígenos alrededor del manganeso se alarga y acorta, y teniendo en cuenta que en cada ciclo de carga/descarga se produce la transformación de Mn3+{ Mn4+> Mn3+, lo que afecta negativamente al óxido laminar durante ciclos.
Para hacer frente a este problema, los óxidos laminares se dopan con elementos inactivos, como el magnesio y el titanio, que no captan/liberan electrones durante el proceso de carga/descarga de la batería. En este sentido, investigadores de CIC EnergiGUNE realizamos un estudio basado en el compuesto Na2/3Fe0,2 Mn0.8O2, que es el óxido laminar de hierro y manganeso que obtiene las condiciones electroquímicas más favorables. En el estudio vimos que al dopar este compuesto con distintas cantidades de titanio, la evolución de la capacidad de ciclo a ciclo cambiaba. Recientemente, en un trabajo publicado en la revista Journal of Material Chemistry A, hemos explicado el papel del titanio en este sentido, combinando mediciones electroquímicas, espectroscopía de absorción de rayos X y cálculos teóricos utilizando la teoría de la densidad funcional (DFT).
En resumen, se puede decir que el titanio es capaz de absorber las distorsiones de octaedros de los metales activos de la zona, en este caso el manganeso. Es decir, aunque la configuración electrónica no produzca distorsiones JT, el titanio es capaz de adaptar su octaedro a las distorsiones del entorno. En esencia, al ser más débil la unión titanio-oxígeno, adaptándose a los movimientos del entorno, este metal se comporta en la estructura como un cojín capaz de dar estabilidad a toda la estructura.
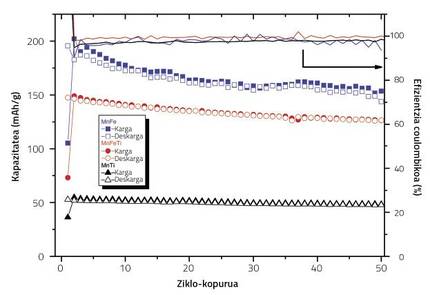
En cualquier caso, la concentración de titanio debe cuidarse adecuadamente. El estudio se basó en el Na2/3Fe0,2 Mn350O2, que es el que obtiene la mejor condición electroquímica entre los óxidos laminados de hierro y manganeso. En la investigación utilizamos tres concentraciones de titanio, de las cuales sólo se obtuvieron resultados satisfactorios. En ausencia de titanio, a medida que se hacían ciclos de carga/descarga, la capacidad del cátodo disminuía notablemente. Cuando sustituíamos todo el hierro del compuesto por titanio, la capacidad inicial disminuía considerablemente. En cambio, cuando sustituimos la mitad del hierro por titanio, la capacidad inicial era adecuada, así como su evolución ciclo a ciclo. De hecho, a medida que aumenta la concentración de titanio, aumenta la concentración de Mn3+ que sufren el estiramiento/acortamiento de sus octaedros, lo que hace que la capacidad de la batería sea baja desde el principio. Sin embargo, cuando la concentración del dopante es menor, Mn3+ estará menos en el compuesto, y además de tener una capacidad inicial más alta, la cuchilla del titanio en la estructura permite mantener mejor la capacidad ciclo a ciclo.
Como reflejo de este carácter, calculamos teóricamente los índices de distorsión de todos los metales de transición del compuesto (Fe, Ti, Mn3+ y Mn4+). Este índice nos indica cuánto se aleja de un octaedro regular formado por seis oxígenos alrededor de cada átomo del metal de transición.
Así, para los tres compuestos analizados, el catión Mn3+ era el que presentaba mayor índice de distorsión. En el otro extremo se situaba Mn4+, el más cercano a un octaedro regular. Esto es fácilmente comprensible si tenemos en cuenta que el catión Mn3+ sufre distorsión JT por su configuración electrónica.
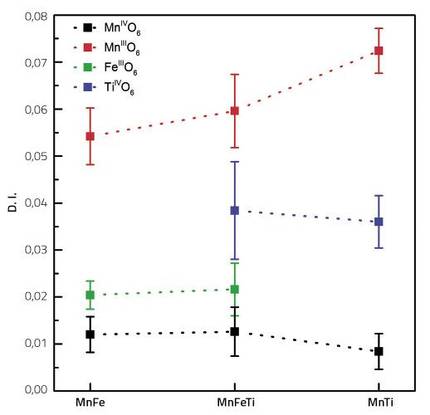
Lo más llamativo es la diferencia entre Ti y Fe. El índice de distorsión del titanio es entre dos y tres veces superior al del hierro. Básicamente, estos dos metales de transición no deberían presentar por sí mismos distorsiones, ya que su configuración electrónica no les afecta. La distorsión de estos dos metales inactivos es debida únicamente a las distorsiones de los octaedros circundantes. Así, el hecho de que el índice de titanio sea dos o tres veces superior al del hierro indica que el titanio adapta mejor las distorsiones de la zona que el hierro. Es decir, si comparamos los componentes inactivos del cátodo con un cojín, su índice de distorsión indicaría el grado de flacidez del cojín. Cuanto mayor sea el índice de distorsión, más flexible será el cojín, lo que facilitará la absorción de las irregularidades de los octaedros circundantes.
Paso a paso…
En aquel trabajo pudimos comprobar que el titanio podría mejorar la duración de las posibles baterías de sodio ion. Es decir, podríamos cargar más a menudo el portátil o el vehículo eléctrico que usase este tipo de baterías sin dañar demasiado la capacidad de su batería.
Sin embargo, este es un pequeño paso más en el camino de las baterías de sodio ion. Está por ver cómo afectarían otros dopantes distintos del titanio. Por ejemplo, se ha podido comprobar que a veces se obtienen resultados muy interesantes incluso cuando se utiliza zinc como dopador, lo que todavía no se entiende muy bien.
Asimismo, en los óxidos laminares tipo P2, cuando se detecta presencia de sodio en prismas que comparten una cara con octaedros de metales de transición, se ha observado que la transformación P2> O2 se complica. Esto facilita el proceso de carga/descarga de la batería. Por tanto, además del dopante, habrá que tener en cuenta la función que puede tener la posición de los átomos de sodio.
En todas estas investigaciones estamos involucrados diferentes grupos de investigación de la línea de baterías de sodio ion de CIC EnergiGUNE.





