Revêtements durables utilisant des nanoparticules fonctionnelles
Les revêtements ou revêtements (peintures, vernis, laques, encres…) sont nécessaires dans la vie actuelle, car presque toutes les surfaces doivent être couvertes. Ses principales fonctions sont la protection et la décoration de la surface [1]. Les surfaces à protéger comprennent l'acier et le bois. Si le premier ne se protège pas de l'oxydation et le second de l'atmosphère, les produits et structures fabriqués avec ces matériaux dureraient très peu, mais les revêtements permettent d'allonger pendant plusieurs années. Les revêtements décoratifs sont utilisés pour rendre les produits plus attrayants.
Les compositions des revêtements sont généralement très complexes et ont de nombreux composants. Parmi eux se distinguent le polymère, les remplissages, les pigments et les additifs. Le polymère agit comme liant et génère une matrice dans le revêtement qui regroupe les autres composants. Les propriétés mécaniques, la luminosité et la capacité barrière dépendent du polymère, qui est la composante analysée dans ce travail. Avant que le revêtement ou la peinture sèche, tous les composants sont dispersés dans une phase continue liquide qui peut être un solvant organique ou de l'eau.
Bien que les revêtements aient d'abord été commercialisés dans des solvants organiques [2], au cours des dernières décennies, le marché se déplace vers des revêtements à base d'eau. Le principal inconvénient de ces premiers revêtements est l'émission au milieu de composés organiques volatils (COV). Les COV sont des solvants à faible point d'ébullition comme l'acétone, l'acétate d'éthyle et les hydrocarbures aliphatiques. Ils ont une mauvaise odeur, beaucoup sont toxiques, augmentent l'effet de serre et augmentent le changement climatique. En outre, dans les revêtements à base d'eau, la phase continue est l'eau, de sorte que les produits ont (ou non) faible teneur en COV. Cela rend les produits plus sûrs, moins chers et plus faciles à utiliser.
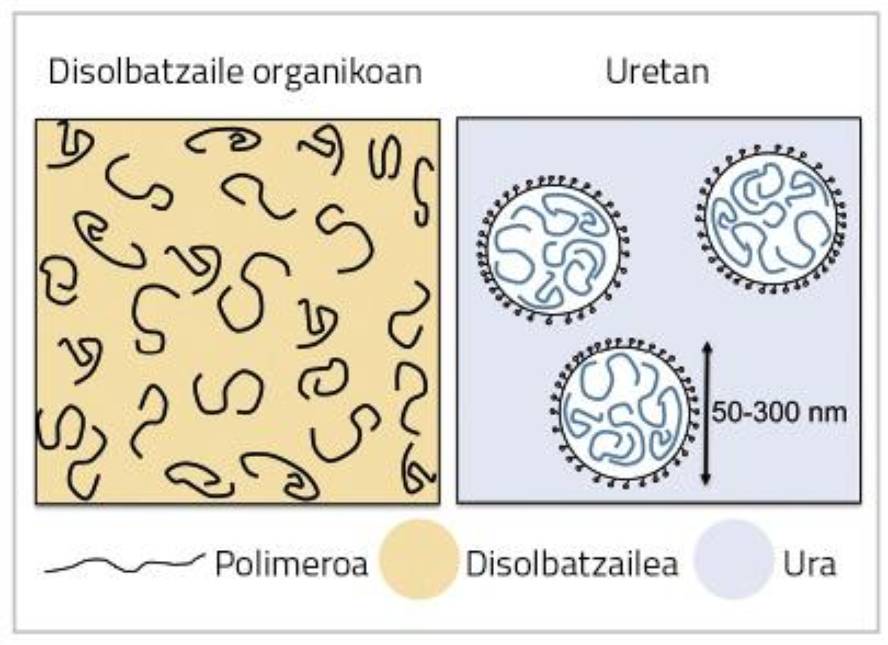
Bien qu'ils soient plus adaptés à l'environnement, les revêtements à base d'eau ont leurs limites. Dans ce type de système, le polymère n'est pas dissous mais dans une dispersion colloïdale (voir figure 1). Pour maintenir la stabilité de la dispersion, il est nécessaire d'utiliser des émulsifiants ou des stabilisateurs polymères qui augmentent la sensibilité au revêtement final.
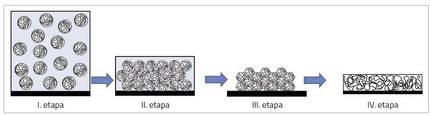
Le processus d'obtention d'un film à partir d'une dispersion aqueuse est complexe et se compose de quatre étapes ou situations, comme le montre la figure 2. Au début du processus (étape I) les particules de polymère sont dispersées dans l'eau. À mesure que l'eau s'évapore, les particules s'approchent, les touchant entre elles et formant une structure compacte, intercalant l'eau (II. étape). Quand l'eau continue à s'évaporer, si les particules sont assez molles, elles commencent à se déformer en formant des structures hexagonales (III. étape). Ensuite, les chaînes situées en particules déformées s'étendent les unes aux autres, les retardant les unes aux autres, obtenant le film continu (IV. étape) [3].
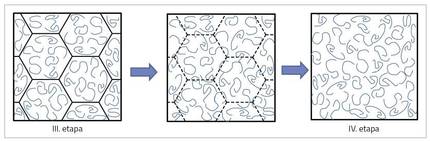
Pour que le revêtement ait de bonnes propriétés, il faut que le film soit très bien formé et qu'il y ait moins d'erreurs. C'est pourquoi il est indispensable III. et IV. développer correctement la transition entre les étapes. La formation de nuances est plus simple lorsque la mobilité des chaînes de polymères est élevée. Le problème est que la mobilité des chaînes est très liée à la dureté du polymère, et en général, à mesure que la mobilité des chaînes augmente, le polymère est plus souple. Cela représente un grand défi pour obtenir des films de bonne qualité mais avec une bonne dureté à partir de dispersions aquatiques.
Pour faire face à ces limites, il existe différentes options, comme l'incorporation de fonctionnalités supplémentaires au polymère. Par exemple, la pénétration des chaînes de polymères améliore les propriétés mécaniques du revêtement, ainsi que la résistance aux solvants, à l'eau et à l'abrasion. La chimie de pénétration des polymères est déjà connue [4], mais il faut garder à l'esprit qu'il n'est pas facile d'obtenir le film à partir d'une dispersion des polymères déjà emboîtée, car la pénétration empêche également la mobilité des chaînes. Par conséquent, la seule possibilité est que la pénétration se produit pendant ou après la formation filmique.
Plusieurs stratégies peuvent être utilisées pour atteindre cet objectif. Dans ce travail, l'utilisation d'alcooliques monomères a été étudiée. Ces monomères sont spéciaux car ils ont deux types de fonctionnalités ou groupes réactifs. D'une part, ils présentent un double lien qui peut participer à la polymérisation par radical libre, représenté en rouge dans les structures indiquées dans la figure 4. Ce groupe leur permet de réagir avec les autres monomères qui formeront la chaîne polymère, formant des chaînes fonctionnalisées comme celles indiquées à la figure 5 (a).
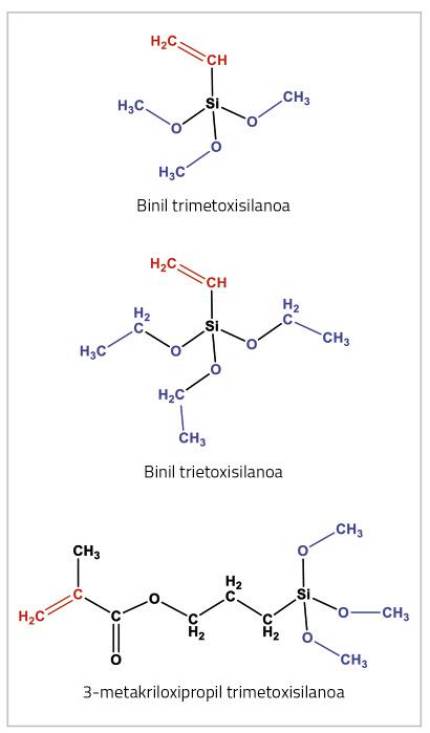
D'autre part, il y a trois groupes d'alcool représentés en bleu dans la figure 4. Les groupes alcooliques peuvent réagir avec l'eau du milieu par des réactions appelées hydrolyse [5]. Dans le cas des trialcoxisylans, trois groupes d'alcool par molécule peuvent réagir avec 3 molécules d'eau. En conséquence de cette réaction, les groupes d'alcool qui font partie de la chaîne deviennent des groupes de silanol (groupes -OH) liés au silicium, qui sont affichés en rouge dans la figure 5 (b).
Les groupes de silanol nouvellement créés sont capables de réagir entre eux par des réactions appelées condensations. À la suite de la réaction de condensation, une molécule d'eau est libérée au milieu et les deux groupes de silanol sont réunis pour former des liaisons appelées siloxanes. Comme le silano fait partie de la chaîne polymère, cette réaction rend les chaînes jointes les unes aux autres, comme le montre la figure 5 (c) en vert.
Après les réactions de condensation, les chaînes de polymères ne seront plus relâchées, mais dans la structure du réseau. Parmi les caractéristiques des polymères grillagés, il est important que les solvants ne soient pas capables de distribuer les chaînes qui forment le réseau. Par conséquent, pour quantifier l'efficacité des réactions de pénétration, il est très pratique de savoir quelle fraction du polymère ne se dissout pas. L'analyse de la solubilité peut être effectuée de manière qualitative, en immergeant le film polymère dans le solvant et en analysant s'il est dissous ou non, comme le montre la figure 6. Mais non seulement cela, l'extraction permet de mesurer quantitativement le pourcentage de polymère dissous. La fraction de polymère qui reste sans dissoudre est appelée teneur en gel. Si le silano est très efficace, le degré de pénétration sera plus élevé et donc la teneur en gel.
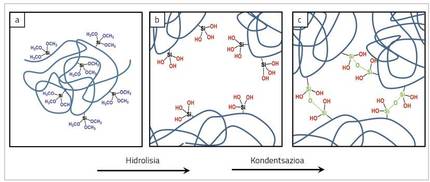
L'hydrolyse est une étape indispensable pour que se produisent ultérieurement des réactions de condensation et donc des pénétrations. C'est pourquoi, comme l'alcool silencieux est hydrolysé, plus de groupes avec une capacité de pénétration se forment. En d'autres termes, lorsque le niveau d'hydrolyse du silano est plus élevé, la capacité de pénétration du polymère sera également plus grande. Tous les alcooliques ne sont pas hydrolisés à la même vitesse et, selon la structure chimique du groupe alcoolique, la réaction est plus rapide ou plus lente. En général, plus la taille du groupe d'alcool est grande, plus l'hydrolyse est lente.
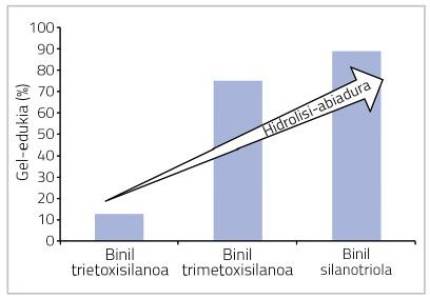
Dans ce travail, on a observé que lorsque l'on utilise du silano avec une hydrolyse lente on obtient de petits contenus de gel, tandis que lorsque l'on utilise du silano avec une vitesse d'hydrolyse rapide on obtient une teneur élevée en gel. De plus, si on utilise du silane hydrolysé dès le début (vinyle silanotriola), la teneur en gel est encore plus élevée, comme le montre le graphique de la figure 7.
Cependant, l'utilisation d'alcools a plus de défis. Le silano confère au polymère une capacité supplémentaire (et peut-être non souhaitable). Dans les systèmes conventionnels, une fois extraits du réacteur, les propriétés du polymère ne varient pas avec le temps, mais cela ne se produit pas dans les dispersions aqueuses de polymères modifiés avec du silano. En raison de la présence d'eau, les réactions d'hydrolyse peuvent également se produire pendant le stockage du polymère et, une fois les groupes de silanol formés, des réactions de condensation peuvent commencer à se produire dans un état de dispersion avant le séchage du film. Cela signifie qu'au fil du temps la structure du polymère en dispersion variera pendant le stockage et donc les propriétés du film changeront.

Cette évolution a été étudiée en mesurant les propriétés mécaniques du film sec. On a observé qu'en principe, à mesure que le temps de stockage de la dispersion polymère s'écoule, on obtient un film avec de meilleures propriétés mécaniques, car en avançant les réactions d'hydrolyse et de condensation on obtient un niveau de pénétration plus élevé. Cependant, à partir d'un certain temps de stockage, le polymère est déjà très tressé en état de dispersion et, comme indiqué au début, des dispersions de polymère treillis ne peuvent pas obtenir des films de bonne qualité. En conséquence, les propriétés mécaniques diminuent.
Mais toutes ne sont pas de mauvaises nouvelles. En fait, la vitesse des réactions d'hydrolyse et de condensation peut être contrôlée en modifiant le pH du milieu. Lorsque le pH est proche de 7, les réactions d'hydrolyse et de condensation sont très lentes, de sorte que le polymère ne présente pas d'évolution significative. Cependant, l'acidification ou la basification du pH accélère les réactions. Cela permet, en sélectionnant les silanes monomères et le pH appropriés, d'ajuster le temps de disponibilité du revêtement et d'obtenir une efficacité maximale du silane.
La lutte contre l'effet de serre et le changement climatique est un défi pour toute la société et les solutions doivent venir de tous les secteurs de la technologie. Bien qu'en principe il ne semble pas, les revêtements ont une importance capitale, car en augmentant la survie des structures réduisent l'exploitation des ressources naturelles. Dans ce domaine, les monomères d'alcool silencieux offrent une occasion unique de remplacer les revêtements actuellement utilisés (ou en développement) par de nouveaux revêtements durables à base d'eau, qui améliorent leurs propriétés et réduisent l'utilisation de solvants.
Références
Travail présenté aux prix CAF-Elhuyar.





