Angiogénesis tumoral
Farmazian doktorea. Biofarmazia, Farmakozinetika eta Farmazia-teknologiako irakasle kolaboratzailea
Farmazia Fakultatea UPV-EHU, Vitoria-Gasteiz
Nos últimos 30 anos, moitos grupos de investigación de moitos países dedicaron os seus esforzos a curar esta enfermidade. Iso si, aínda que é una das alteracións máis estudadas e estudadas desde un punto de vista biolóxico e molecular, aínda hai moitas dúbidas que resolver e está a piques de atopar o tratamento de moitos tipos de cancro. De feito, a diversidade de tipos de cancro fai que o descubrimento dunha ‘bala máxica’ ou, o que é o mesmo, o desenvolvemento dun tratamento contra todo tipo de cancro sexa practicamente imposible. Por iso, os obxectivos científicos diríxense, por unha banda, á procura de solucións específicas paira cada tipo de cancro e, por outro, ao desenvolvemento de novas estratexias terapéuticas que complementen ou substitúan ás técnicas actuais de cirurxía, quimioterapia e radioterapia.
Una destas novas estratexias contra o cancro é a terapia contra a angiogénesis. Esta estratexia de crecente importancia baséase na inhibición da creación de novos vasos sanguíneos que alimentan e visten o tumor (Folkman, 1971). Neste traballo, ademais de incidir na importancia da angiogénesis no desenvolvemento do cancro, analizaranse as posibilidades terapéuticas que ofrecen as súas inhibicións.
Que é a angiogénesis tumoral?
Os factores que interveñen na creación e difusión do cancro son numerosos. Estes factores, tanto hereditarios como epigenéticos, modifican o material xenético das células, especialmente o relativo á súa capacidade reprodutiva. Por tanto, una célula que antes se dividía de forma controlada e limitada faia infinita. Con todo, o crecemento do cancro non se debe unicamente á inmortalidade celular.
No cancro de próstata, por exemplo, a fracción de células que se dividen é só un 2% (Berges, 1995), e o 90-99% das células tumorales xeradas morren por falta de nutrientes. Que significa isto? Que moitos tipos de cancro necesitan dun novo suceso paira manter a poboación celular en desenvolvemento. Este fenómeno é a angiogénesis.
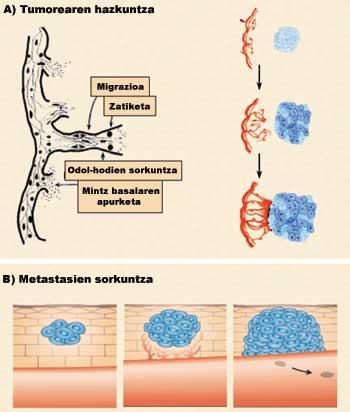
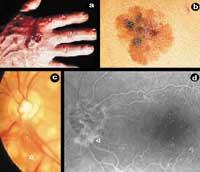
A angiogénesis, por tanto, é o proceso de formación de novos vasos sanguíneos a partir dos xa existentes. Os novos vasos sanguíneos, ademais de alimentar o tumor, permitirán o seu metástasis, é dicir, a súa extensión ás novas partes do corpo. Para que un pequeno pobo convértase en cidade, como as estradas que comunican casas á parte das novas, o cancro necesita, ademais de células, vasos sanguíneos paira alimentarse, crecer e expandirse. Con todo, a angiogénesis non é só un fenómeno relacionado co cancro, senón que tamén é un proceso que se produce en certas situacións fisiológicas (ciclo menstrual e cicatrización) e fisiopatológicas (psoriasis e retinopatía diabética) (Figura 1).
Inicio, fases e efectos da angiogénesis tumoral
A formación de novos vasos sanguíneos é un reflexo da necesidade de nutrientes e osíxeno do tumor. Cando aparece esta necesidade, as células tumorales segregan sustancias chamadas “factores angiogénicos” ou “reguladores positivos”. Estes factores afectan as células endoteliales dos vasos sanguíneos e inician a angiogénesis.
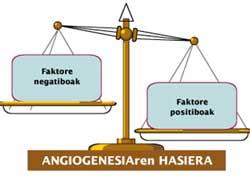
En condicións normais, a concentración destes factores está en equilibrio coa concentración doutros con efecto adverso. Estas últimas denomínanse ‘antiangiogénicas’ ou ‘reguladores negativos’. O cancro, fomentando a concentración relativa de reguladores positivos que excitan a formación de novos vasos sanguíneos (Figura 2), rompe este equilibrio.
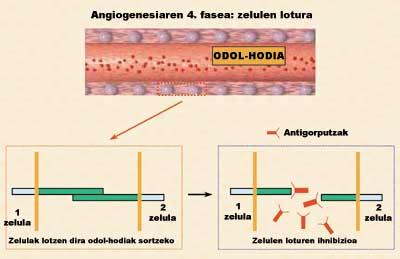
A angiogénesis divídese en catro fases (figura 3). Nunha primeira fase rompe a membrana basal dos vasos sanguíneos xa existentes (1ª fase: rotura da membrana basal). Como consecuencia diso, as células endoteliales son expulsadas do vaso sanguíneo e dispersas á zona tumoral (2ª fase: migración). Neste camiño as células van dividíndose (Fase 3: División). Finalmente, as células únense entre si a través de diferentes proteínas adhesivas formando un novo vaso sanguíneo (Fase 4: unión de células).
O desenvolvemento destas catro etapas ten dúas consecuencias principais: por unha banda, o crecemento tumoral debido aos nutrientes, o osíxeno e os factores estimulantes (figura 3.a), e por outro, a introdución de células tumorales nos vasos sanguíneos, que por vía sanguínea esténdense a outras partes do corpo e provocan novos tumores (figura 3.b).
Inhibición da angiogénesis tumoral
Actualmente é coñecida a relación entre a vitalidade da angiogénesis tumoral, a frecuencia de metástasis e a redución da esperanza de vida dos pacientes (Pluda, 1997). Por iso, a inhibición efectiva da angiogénesis converteuse no obxectivo de moitos científicos. Sobre todo, evitar a formación de novos vasos sanguíneos, xa que ademais de inhibir a metástasis, reducirá o tamaño do tumor, facilitando a erradicación do cancro mediante quimioterapia ou cirurxía.
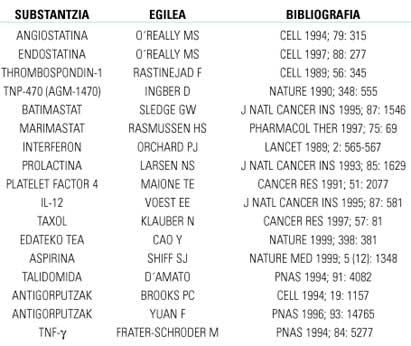
Tendo en conta o anteriormente exposto, una forma sinxela de inhibir a angiogénesis sería dirixila cara aos equilibrios reguladores negativos dos factores. Isto pódese conseguir de dúas formas: inhibindo os factores positivos ou fomentando os negativos. Tamén se pode inhibir calquera fase da angiogénesis si bloquéanse as encimas e/ou proteínas implicadas. Na táboa 1 móstranse os fármacos máis eficaces contra a angiogénesis investigados en animais de laboratorio. Deles, só os que mellores resultados e máis seguridade ofrezan tentarán en humanos con sesións clínicas.
Das catro fases da angiogénesis, una das máis interesantes é a que menos se estudou desde un punto de vista terapéutico. Por iso, o laboratorio de Farmacia e Tecnoloxía Farmacéutica da Facultade de Farmacia (UPV/EHU) iniciou un novo estudo de inhibición da angiogénesis paira bloquear esta cuarta fase. O obxectivo da investigación foi inhibir algunhas proteínas adhesivas que permiten a unión entre células endoteliales. Paira inhibir ou bloquear estas proteínas utilizáronse células que segregaban anticorpos específicos (Figura 4). Con todo, se as células administrásense como talles, eliminaría rapidamente os sistemas inmunológicos dos animais por consideralos descoñecidos.
Paira solucionar este problema, agrupámolos en esferas poliméricas de pequeno tamaño que protexe as células fronte ao sistema inmunológico. Este proceso coñécese como microencapsulación celular (Orive G, 2000). Dentro destas pequenas cápsulas, as células, ademais de crecer, segregaban o anticorpo que nos interesaba. Esta nova estratexia anti-angiogénesis ten dúas vantaxes principais: por unha banda, a inhibición dunha proteína pouco estudada e por outro, a secreción continuada e prolongada de anticorpo por parte das células.
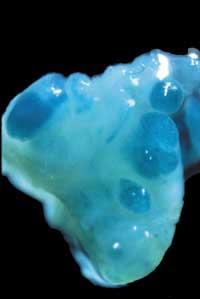
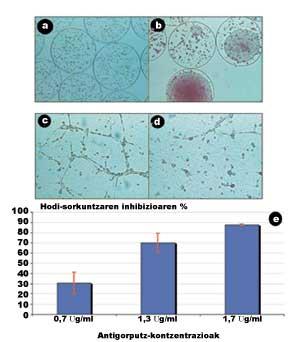
Na figura 5 preséntanse algúns dos resultados obtidos neste estudo (Orive G, 2001). Nas seguintes imaxes, obtidas mediante o microscopio, obsérvase que as células crecen e divídense rapidamente no interior das cápsulas, dando lugar á formación de agregados violentos (Figuras 5.a e 5.b).
Noutra sesión analizamos a capacidade dos anticorpos segregados paira bloquear a unión entre células endoteliales. Paira iso, as células endoteliales foron estimuladas por factores de crecemento. Estes factores estiraron as células e facilitaron as unións entre elas, creando vasos sanguíneos inmaturos (tubulos), é dicir, estruturas previas aos vasos sanguíneos que alimentarán o tumor. Como se observa na figura 5.c, en ausencia de anticorpos, as relacións entre células endoteliales son moi notables.
Pola contra, cando se introduciu a disolución de anticorpos cunha concentración de 1,7 µg/ml, as unións intercelulares e, por tanto, a formación de tubulos inhibíronse case por completo (Figura 5.d). Cal é o seu significado? Que o anticorpo que segregan as células encapsuladas ten a capacidade de inhibir a angiogénesis e que o bloqueo de proteínas adhesivas é una boa estratexia paira inhibir a angiogénesis tumoral. Ademais, nunha última sesión demostrouse que a relación entre a tracción concertística anticorpo e a capacidade de inhibir a angiogénesis é directamente proporcional (Figura 5.e).
Estes esperanzadores resultados iniciais leváronnos a unha nova investigación na que utilizaremos a terapia génica como base paira inhibir a angiogénesis tumoral.
Fin
A partir da década dos 90 a angiogénesis foise facendo cada vez máis interesante tanto paira os científicos como paira a industria. De feito, máis de 25 fármacos contra a angiogénesis están a ser tratados en sesións clínicas (Kerbel, 2000). O interese actual céntrase non só no descubrimento de novos fármacos, senón tamén na combinación de estratexias antiangiogénesis e estratexias convencionais contra o cancro (quimioterapia, radioterapia e cirurxía).
Esta última idea ten una gran importancia tendo en conta que a combinación de varias estratexias pode predicir efectos sinérgicos, é dicir, efectos máis beneficiosos que os logrados individualmente por devanditas estratexias. Ademais, novas estratexias de administración (anticorpos monoclonales, terapia génica, etc.). ), permiten novas solucións paira inhibir a angiogénesis e así controlar os cancros.
En definitiva, aínda que aínda queda moito por investigar, o traballo diario e o soño máis doce de todos os científicos é facer súas as malas enfermidades.