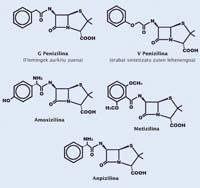
Penicilina, buena imitación

En 1928, en un laboratorio de Londres, intentaba crecer una colonia de bacterias. Lo intentó, pero no lo consiguió, y no hubo un problema de comida, ya que el biólogo Alexander Fleming alimentaba bacterias para su uso experimental. Sin embargo, las bacterias tenían un problema de crecimiento.
No podían aumentar la pared exterior a medida que iban creciendo. Y la razón era que las bacterias no podían añadir una de las moléculas que forman la pared, el dímero de la alanina. En lugar de tomar este dímero, las proteínas que estaban construyendo la pared recibían otra molécula y quedaban bloqueadas. Por lo tanto, la pared de las bacterias no aumentaba a la velocidad de crecimiento de la propia bacteria. Y como tenían la pared exterior incompleta, la ósmosis provocaba que las bacterias explotaran.
Fleming no lo vio todo, no sabía que las bacterias no podían construir la pared. Pero descubrió que junto a la colonia de bacterias había un hongo de la especie Penicillium notatum. Todas las bacterias que rodean el hongo estaban muertas, por lo que el hongo debía ser un asesino. Además, se dio cuenta de que el arma del hongo debía ser un producto químico, una molécula. Fleming le llamó penicilina.
El viaje de la penicilina
Si un hongo utilizaba penicilina para matar bacterias, ¿por qué el hombre no lo usó? Fleming envió algunas de sus culturas a la Universidad de Oxford. Allí, Howard W. Florey y Ernst B. El equipo de Chain comenzó a realizar pruebas clínicas con penicilina. Muy buenos resultados. La penicilina mataba muchos tipos de bacterias, era un antibiótico de gran espectro.
A partir de entonces muchos investigadores comenzaron a trabajar con la penicilina, sobre todo en la industria farmacéutica. El objetivo era, por un lado, aclarar cuál era la estructura de la molécula --para comprender el funcionamiento de la penicilina y poder sintetizar la misma molécula en el laboratorio- y, por otro, la necesidad de encontrar una forma de producir grandes cantidades de penicilina a partir del hongo.

La Segunda Guerra Mundial comenzó y el acceso a la penicilina adquirió una gran importancia. Según algunos historiadores, la investigación de la penicilina tuvo más importancia que el propio Proyecto Manhattan y, sin duda, el antibiótico salvó más vidas que las bombas atómicas.
El primer paciente tratado con penicilina fue un policía del Reino Unido en 1941. Una infección producida en una herida bucal se extendió a los ojos y a los pulmones. Pero el efecto del antibiótico mejoró muy rápidamente su estado. Sin embargo, tenían poca cantidad de penicilina y aunque intentaron recuperar el antibiótico de la orina del paciente, finalmente el hombre murió. Paradójicamente, el tratamiento resultó exitoso: el hombre podía ser tratado con el nuevo antibiótico.
Imitación
El secreto de la influencia de la penicilina es la imitación. La pared de las bacterias es una estructura muy compleja, formada por glúcidos y péptidos. Pero basta con poner un obstáculo a un solo componente de estas complejas estructuras para frenar el crecimiento de toda la pared. Un único componente, pero no cualquiera. Lo que imita y, en consecuencia, representa las penicilinas es el dímero de la alanina.
La penicilina se asemeja muy al dimero de la alanina, con los mismos átomos (más otros átomos adicionales) en el mismo orden y en la misma estructura geométrica que se encuentran en la alanina. Precisamente, los átomos adicionales que contiene la penicilina sustentan a los demás para que tengan una estructura geométrica recta.
La geometría es muy importante. Si la penicilina no tuviera la misma geometría que el dimero de la alanina, las proteínas de las bacterias no la cogerían. No se puede engañar a las bacterias si no se ha utilizado sus armas. De hecho, la alanina que forma parte de la pared de las bacterias no es la misma que utiliza la mayoría de los seres vivos.
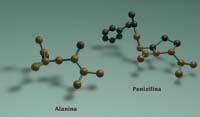
La alanina, y la mayoría de los aminoácidos, son moléculas asimétricas con dos formas principales: las formas izquierda y derecha. L-alanina y D-alanina, respectivamente. El problema es que en las proteínas de la mayoría de los seres vivos sólo aparece L-alanina. Pero las bacterias utilizan otra forma en la pared, la D-alanina.
Es un arma propia de las bacterias, ya que otros seres vivos no pueden interrumpir los péptidos formados por aminoácidos en forma de D. Los péptidos de los L-aminoácidos son destruidos por las proteasas convencionales. Y en eso consiste el don de la penicilina: Es la imitación de la d-alanina. Por eso funciona contra las bacterias.
Es más, funciona contra muchas bacterias. En todas las bacterias la pared es diferente, algunos componentes varían de una especie a otra, pero la D-alanina aparece en la mayoría de los casos, por lo que la penicilina es un antibiótico de gran espectro.
Un anillo
La penicilina funciona, pero no fue fácil averiguar cómo es. Los investigadores estaban motivados, la Segunda Guerra Mundial estaba en marcha, la penicilina era escasa y muy necesaria, y una de las esperanzas era poder sintetizar esta molécula en el laboratorio. Lo que conseguía tenía buenas razones para soñar con el premio Nobel.

Sin embargo, al finalizar la Segunda Guerra Mundial, tardaron doce años más en sintetizarse la penicilina en el laboratorio. John C lo consiguió en 1957. Los estadounidenses Sheehan, en el MIT. Una vía de síntesis pasa por conocer primero cómo es la molécula que se quiere sintetizar; el trabajo cristalográfico del británico Dorothy Crowfoot Hodgkin reveló la estructura de la penicilina.
Era la estructura propuesta por Florey y Chain (del equipo de Oxford). La base de la molécula está formada por dos ciclos en los que el secreto del éxito de la penicilina era el más pequeño.
Es un ciclo de cuatro átomos, tres de carbono y un nitrógeno. Un carbono junto al nitrógeno tiene asociado un oxígeno mediante un doble enlace. Los químicos llaman amida a esta combinación de átomos y lactama a las amidas en forma de ciclo. Los de cuatro átomos se denominan beta-lactama. De hecho, todas las penicilinas (meticilina, amoxicilina, etc.) son antibióticos debido al ciclo de beta-lactama en la estructura, ciclo que da a la molécula la misma geometría que la alanina. Por ello, este tipo de antibióticos se denominan betalactámicos.
Respuesta bacteriana
El éxito de la penicilina y de todos los antibióticos betalactámicos no siempre está garantizado. Son poderosas armas durante la guerra intermicrobiana, pero las bacterias también tienen la capacidad de desarrollar armas de defensa contra los antibióticos. El propio Fleming descubrió que si el hongo no mataba toda la colonia bacteriana, con el paso del tiempo la penicilina no afectaba a los ejemplares supervivientes. Desarrollaban la resistencia al antibiótico.
De hecho, las bacterias producen nuevas proteínas, beta-lactamasa, que descomponen el ciclo de la betalactam. Deshecho el ciclo de los cuatro átomos, el antibiótico no funciona.

El hongo no puede hacer nada en contra de esta resistencia. Todas las bacterias de la colonia deben morir desde el principio. Y el hombre también debería hacerlo, pero no ha ocurrido. Muchas bacterias han desarrollado resistencia a la penicilina. Un problema importante es la bacteria Staphilococcus aureus resistente a la meticilina. En los hospitales lo conocen perfectamente y es o puede ser un problema grave. Pero el hombre no es un hongo y ha desarrollado química sintética para avanzar en la guerra contra las bacterias.
Entre otras cosas, se pueden sintetizar medicamentos contra beta-lactamas, como el ácido clavulánico, que parece una paradoja, pero cuya molécula tiene un ciclo beta-lactama en su estructura.
Por otro lado, pequeños cambios químicos en la penicilina han permitido sintetizar nuevos antibióticos que la bacteria no puede reducir. Por supuesto, estas nuevas moléculas también tienen que ser una buena imitación del dímero de la alanina, pero por ello, los químicos tienen muchas posibilidades de hacer nuevas penicilinas. Eso sí, con el tiempo, algunas bacterias desarrollarán resistencia contra la nueva penicilina y el juego volverá a empezar.
Pero, ¿hasta cuándo? Las bacterias se reproducen muy rápido, evolucionan muy rápido, lo que significa que pueden desarrollar la resistencia rápidamente. El ser humano tiene la capacidad de responder, pero no tan rápido como lo tienen las bacterias.
Último recurso
A veces es clave cambiar la estrategia y utilizar otros tipos de antibióticos, como los que no tienen beta-lactama. Reaparición de bacterias resistentes pero menos rápido.
En este juego se considera la bancomicina antibiótica como la última opción para los casos más graves. La bancomicina y otros antibióticos de su familia atacan también la pared de las bacterias, pero no imitando la alanina. Sin embargo, algunas cepas bacterianas también han desarrollado su resistencia a la bancomicina. Y lo peor es que no saben cómo es el mecanismo de ciertas resistencias.
El descubrimiento de la penicilina ha salvado muchas vidas, pero metió al hombre en una guerra química y no está claro quién ganará esa guerra.