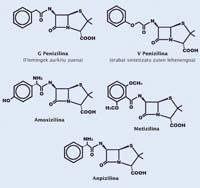
Penicil·lina, bona imitació

En 1928, en un laboratori de Londres, intentava créixer una colònia de bacteris. Ho va intentar, però no ho va aconseguir, i no va haver-hi un problema de menjar, ja que el biòleg Alexander Fleming alimentava bacteris per al seu ús experimental. No obstant això, els bacteris tenien un problema de creixement.
No podien augmentar la paret exterior a mesura que anaven creixent. I la raó era que els bacteris no podien afegir una de les molècules que formen la paret, el dímer de l'alanina. En lloc de prendre aquest dímer, les proteïnes que estaven construint la paret rebien una altra molècula i quedaven bloquejades. Per tant, la paret dels bacteris no augmentava a la velocitat de creixement del propi bacteri. I com tenien la paret exterior incompleta, l'osmosi provocava que els bacteris explotessin.
Fleming no ho va veure tot, no sabia que els bacteris no podien construir la paret. Però va descobrir que al costat de la colònia de bacteris hi havia un fong de l'espècie Penicillium notatum. Tots els bacteris que envolten el fong estaven mortes, per la qual cosa el fong havia de ser un assassí. A més, es va adonar que l'arma del fong havia de ser un producte químic, una molècula. Fleming li va dir penicil·lina.
El viatge de la penicil·lina
Si un fong utilitzava penicil·lina per a matar bacteris, per què l'home no el va usar? Fleming va enviar algunes de les seves cultures a la Universitat d'Oxford. Allí, Howard W. Florey i Ernst B. L'equip de Chain va començar a realitzar proves clíniques amb penicil·lina. Molt bons resultats. La penicil·lina matava molts tipus de bacteris, era un antibiòtic de gran espectre.
A partir de llavors molts investigadors van començar a treballar amb la penicil·lina, sobretot en la indústria farmacèutica. L'objectiu era, d'una banda, aclarir quina era l'estructura de la molècula --per a comprendre el funcionament de la penicil·lina i poder sintetitzar la mateixa molècula en el laboratori- i, per un altre, la necessitat de trobar una manera de produir grans quantitats de penicil·lina a partir del fong.

La Segona Guerra Mundial va començar i l'accés a la penicil·lina va adquirir una gran importància. Segons alguns historiadors, la recerca de la penicil·lina va tenir més importància que el propi Projecte Manhattan i, sens dubte, l'antibiòtic va salvar més vides que les bombes atòmiques.
El primer pacient tractat amb penicil·lina va ser un policia del Regne Unit en 1941. Una infecció produïda en una ferida bucal es va estendre als ulls i als pulmons. Però l'efecte de l'antibiòtic va millorar molt ràpidament el seu estat. No obstant això, tenien poca quantitat de penicil·lina i encara que van intentar recuperar l'antibiòtic de l'orina del pacient, finalment l'home va morir. Paradoxalment, el tractament va resultar reeixit: l'home podia ser tractat amb el nou antibiòtic.
Imitació
El secret de la influència de la penicil·lina és la imitació. La paret dels bacteris és una estructura molt complexa, formada per glúcids i pèptids. Però n'hi ha prou amb posar un obstacle a un sol component d'aquestes complexes estructures per a frenar el creixement de tota la paret. Un únic component, però no qualsevol. El que imita i, en conseqüència, representa les penicil·lines és el dímer de l'alanina.
La penicil·lina s'assembla molt al dimero de l'alanina, amb els mateixos àtoms (més altres àtoms addicionals) en el mateix ordre i en la mateixa estructura geomètrica que es troben en l'alanina. Precisament, els àtoms addicionals que conté la penicil·lina sustenten als altres perquè tinguin una estructura geomètrica recta.
La geometria és molt important. Si la penicil·lina no tingués la mateixa geometria que el dimero de l'alanina, les proteïnes dels bacteris no l'agafarien. No es pot enganyar als bacteris si no s'ha utilitzat les seves armes. De fet, l'alanina que forma part de la paret dels bacteris no és la mateixa que utilitza la majoria dels éssers vius.
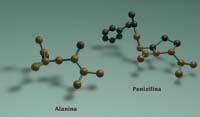
L'alanina, i la majoria dels aminoàcids, són molècules asimètriques amb dues formes principals: les formes esquerra i dreta. L-alanina i D-alanina, respectivament. El problema és que en les proteïnes de la majoria dels éssers vius només apareix L-alanina. Però els bacteris utilitzen una altra forma en la paret, la D-alanina.
És una arma pròpia dels bacteris, ja que altres éssers vius no poden interrompre els pèptids formats per aminoàcids en forma de D. Els pèptids dels L-aminoàcids són destruïts per les proteasas convencionals. I en això consisteix el do de la penicil·lina: És la imitació de la d-alanina. Per això funciona contra els bacteris.
És més, funciona contra molts bacteris. En tots els bacteris la paret és diferent, alguns components varien d'una espècie a una altra, però la D-alanina apareix en la majoria dels casos, per la qual cosa la penicil·lina és un antibiòtic de gran espectre.
Un anell
La penicil·lina funciona, però no va ser fàcil esbrinar com és. Els investigadors estaven motivats, la Segona Guerra Mundial estava en marxa, la penicil·lina era escassa i molt necessària, i una de les esperances era poder sintetitzar aquesta molècula en el laboratori. El que aconseguia tenia bones raons per a somiar amb el premi Nobel.

No obstant això, en finalitzar la Segona Guerra Mundial, van trigar dotze anys més a sintetitzar-se la penicil·lina en el laboratori. John C ho va aconseguir en 1957. Els estatunidencs Sheehan, en el MIT. Una via de síntesi passa per conèixer primer com és la molècula que es vol sintetitzar; el treball cristalográfico del britànic Dorothy Crowfoot Hodgkin va revelar l'estructura de la penicil·lina.
Era l'estructura proposada per Florey i Chain (de l'equip d'Oxford). La base de la molècula està formada per dos cicles en els quals el secret de l'èxit de la penicil·lina era el més petit.
És un cicle de quatre àtoms, tres de carboni i un nitrogen. Un carboni al costat del nitrogen té associat un oxigen mitjançant un doble enllaç. Els químics criden amida a aquesta combinació d'àtoms i lactama a les amidas en forma de cicle. Els de quatre àtoms es denominen beta-lactama. De fet, totes les penicil·lines (meticilina, amoxicilina, etc.) són antibiòtics a causa del cicle de beta-lactama en l'estructura, cicle que dóna a la molècula la mateixa geometria que l'alanina. Per això, aquest tipus d'antibiòtics es denominen betalactámicos.
Resposta bacteriana
L'èxit de la penicil·lina i de tots els antibiòtics betalactámicos no sempre està garantit. Són poderoses armes durant la guerra intermicrobiana, però els bacteris també tenen la capacitat de desenvolupar armes de defensa contra els antibiòtics. El propi Fleming va descobrir que si el fong no matava tota la colònia bacteriana, amb el pas del temps la penicil·lina no afectava els exemplars supervivents. Desenvolupaven la resistència a l'antibiòtic.
De fet, els bacteris produeixen noves proteïnes, beta-lactamasa, que descomponen el cicle de la betalactam. Desfet el cicle dels quatre àtoms, l'antibiòtic no funciona.

El fong no pot fer res en contra d'aquesta resistència. Tots els bacteris de la colònia han de morir des del principi. I l'home també hauria de fer-lo, però no ha ocorregut. Molts bacteris han desenvolupat resistència a la penicil·lina. Un problema important és el bacteri Staphilococcus aureus resistent a la meticilina. Als hospitals ho coneixen perfectament i és o pot ser un problema greu. Però l'home no és un fong i ha desenvolupat química sintètica per a avançar en la guerra contra els bacteris.
Entre altres coses, es poden sintetitzar medicaments contra beta-lactamas, com l'àcid clavulánico, que sembla una paradoxa, però la molècula de la qual té un cicle beta-lactama en la seva estructura.
D'altra banda, petits canvis químics en la penicil·lina han permès sintetitzar nous antibiòtics que el bacteri no pot reduir. Per descomptat, aquestes noves molècules també han de ser una bona imitació del dímer de l'alanina, però per això, els químics tenen moltes possibilitats de fer noves penicil·lines. Això sí, amb el temps, alguns bacteris desenvoluparan resistència contra la nova penicil·lina i el joc tornarà a començar.
Però, fins quan? Els bacteris es reprodueixen molt ràpid, evolucionen molt ràpid, la qual cosa significa que poden desenvolupar la resistència ràpidament. L'ésser humà té la capacitat de respondre, però no tan ràpid com ho tenen els bacteris.
Últim recurs
A vegades és clau canviar l'estratègia i utilitzar altres tipus d'antibiòtics, com els que no tenen beta-lactama. Reaparició de bacteris resistents però menys ràpid.
En aquest joc es considera la bancomicina antibiòtica com l'última opció per als casos més greus. La bancomicina i altres antibiòtics de la seva família ataquen també la paret dels bacteris, però no imitant l'alanina. No obstant això, alguns ceps bacterians també han desenvolupat la seva resistència a la bancomicina. I el pitjor és que no saben com és el mecanisme de certes resistències.
El descobriment de la penicil·lina ha salvat moltes vides, però va ficar a l'home en una guerra química i no és clar qui guanyarà aquesta guerra.