¿Cómo se limpian las prendas en la lavadora?
Un poco de historia
El jabón se utilizó por primera vez hace unos 5.000 años. Los babilonios fueron los primeros en obtener el jabón, cocidos en polvo con varias grasas, que al parecer se utilizaban para decorar el cabello. Desde entonces, los jaboneros han estado presentes en las civilizaciones de todos los tiempos. En Egipto, por ejemplo, hace tiempo

3.500 años, personas de alto nivel se bañaban asiduamente con grasas animales y vegetales y jabones a base de sales alcalinas. También los romanos y griegos usaban con frecuencia jabones para la limpieza y la medicina.
Según diversas leyendas, los romanos dieron la palabra jabón al producto que limpiaba tan bien. Parece que en el monte Sapo se quema el ganado sacrificado y que las cenizas generadas posteriormente se mezclan fácilmente con las grasas animales vertidas. No sé cómo, estas mezclas se vertían al río Tiber y llegaban al lugar donde las mujeres lavaban la ropa. Según estas mujeres, la ropa se limpiaba más fácilmente en la cima del monte tras verter esta curiosa mezcla al río.
En la Edad Media se fabricaba jabón con aceite de oliva en España, Francia e Italia. La producción moderna de jabón comenzó en 1811, cuando el químico francés Michel Eugene Chevreul investigó las características y química de las grasas, los ácidos grasos y la glicerina.
Pero el detergente es más nuevo. Apareció en el mercado por primera vez en 1907 de la mano de la empresa alemana Persil. Este detergente, además de los jabones tradicionales, contenía perborato sódico, silicato sódico y carbonato sódico (perborato + silicato = PERSIL).
La diferencia más evidente entre detergentes y jabones es su origen. Los detergentes son sintéticos y se obtienen a partir de las fracciones de petróleo. Los jabones son naturales. A pesar de ser muy buenos limpiadores, el rendimiento de los jabones disminuye considerablemente en presencia de agua y sales minerales. Los detergentes, por su parte, aumentan en las mismas condiciones.
Mecanismos de limpieza
Para comprender cómo se produce la limpieza se debe prestar atención a la interacción de tres elementos: el de lavado, en este caso el tejido; la suciedad o mancha, es decir, el de lavado a 100 (grasa en general); y la disolución acuosa en la que está disuelto el detergente.
La clave de la limpieza está en la relación adecuada entre los tres, pero no ha sido fácil conocer los detalles de la relación. El comportamiento de los detergentes se ha entendido gracias a la investigación llevada a cabo en las últimas décadas, a pesar del centenario de su primera utilización. De hecho, al igual que ocurre con muchos cosméticos, los fabricantes no conocen la función de muchos componentes. Sin embargo, saben que los productos sirven y cumplen bien su cometido.
Para facilitar la explicación del proceso de limpieza se pueden dividir los pasos que se dan en la lavadora en dos partes. En la primera, en la limpieza del tejido se extraen del tejido las gotas de manchas que manchan el tejido. En la segunda, el reto es doble: conseguir que estas gotas permanezcan dispersas en solución de detergente y no vuelvan al tejido. Está claro que la segunda parte es tan importante como la primera, ya que en la segunda, si las cosas no se hacen bien, los tejidos seguirán sucios.
Hay que tener en cuenta que el mecanismo de limpieza no es el único. Hay muchos tipos de tejidos y suciedad, y no todos actúan igual, por lo que es imposible encontrar una sola teoría o mecanismo que explique bien el proceso de limpieza.
Si la interacción entre la mancha y el tejido es química, por ejemplo, el enlace covalente debe romperse mediante uniones químicas adicionales entre ambas. Para ello se utilizan enzimas o lejías. Por ejemplo, las enzimas proteasa y amilasa rompen las cadenas de almidón y proteínas de las manchas de chocolate, leche o hierba, y fragmentan y reducen completamente la mancha. Pero si la mancha y el tejido están adheridos por fuerzas electrostáticas o débiles fuerzas de atracción intermoleculares, el mecanismo de limpieza es totalmente distinto. Es el caso de las partículas sólidas y las gotas de grasa. En estos casos se utilizan surfactantes para ayudar a las manchas a sacarlas del tejido.
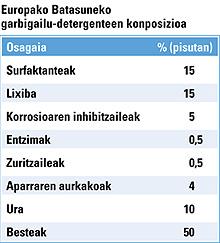
Los surfactantes, también llamados moléculas tensioactivas, son uno de los componentes más importantes de los detergentes y tienen varias obligaciones. Reducen la tensión superficial del tejido y de la mancha y reducen el trabajo de extracción de la misma del tejido; además, los surfactantes tienden a colocarse sobre la superficie de la mancha, por lo que la emulsionan con gran facilidad en el agua. Por último, las gotas de grasa se protegen bien unas de otras para evitar que vuelvan a unirse.
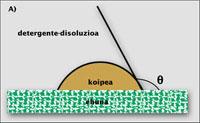
Si la mancha es líquida, el proceso de limpieza puede explicarse matemáticamente de una forma sencilla. Pongamos una gota de aceite o grasa sobre un tejido o una fibra. La gota forma un ángulo con el tejido, que es el ángulo de contacto (q). Este ángulo indica la dificultad de limpiar el tejido: si es pequeño, la superficie de contacto entre la mancha y el tejido es elevada, lo que dificulta su limpieza. Si el ángulo es alto, ocurre al revés. Es lógico ya que hay que hacer un trabajo físico para llevar la gotita de grasa desde la superficie del tejido a la solución acuosa.
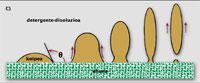
El menor trabajo se realiza cuando el ángulo q entre el tejido y la gotita es 0. Entonces, los dos se tocan en un punto y la limpieza es instantánea. Por encima de cero, el trabajo sólo aumenta. Sin embargo, si el ángulo es menor de 90º (B), la cuestión no es tan complicada, ya que la ayuda de los surfactantes suele ser suficiente para sacar la mancha del tejido. Sin embargo, si el ángulo oscila entre 90º y 180º (C), sólo una parte de la gota de aceite abandona el tejido y la ropa permanece sucia al salir de la lavadora. En este caso, el lavado de la ropa requiere otro mecanismo, como la disolución de gotas de aceite.
Una vez limpia, proteger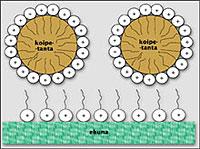
Una vez extraídas las gotitas de manchas del tejido, se deben mantener dispersas en el agua para que la limpieza no sea un trabajo de desaliento. Para ello hay que proteger las gotas del tejido y el tejido de las gotas. En este proceso también es imprescindible la colaboración de los surfactantes.
Los surfactantes tienden a colocarse sobre las superficies de las gotas y tejidos de grasa, proporcionando a ambas superficies el mismo tipo de carga. En consecuencia, las fuerzas de repulsión permiten que las gotas de las manchas no coincidan entre sí y se mantengan lo más alejadas posible del tejido. Además de provocar repulsión eléctrica, las moléculas tensoactivas también interfieren físicamente con cadenas de alto peso molecular. Las moléculas tensoactivas también se colocan en las superficies del tejido y de la gota de grasa, y sus cadenas largas y rizadas ayudan a mantener las superficies alejadas entre sí.
ExtrasComo aditivos se utilizan polímeros y otros productos. La carboxil celulosa sódica, por ejemplo, una vez limpiadas las fibras de celulosa, crea una capa protectora en la superficie de la fibra que impide la reposición de las gotas de grasa.
Los detergentes contienen componentes que no tienen como objetivo ahuyentar la mancha. Los silicatos y fosfatos, por ejemplo, mejoran el rendimiento de los detergentes, formando complejos solubles con los iones Ca+2 y Mg+2 presentes en el agua para evitar la formación de sedimentos calcáreos en las tuberías de agua. Sin embargo, su impacto sobre el medio ambiente se ve afectado por la búsqueda de aditivos que sustituyan a los fosfatos en los últimos años.
Los colorantes fluorescentes aportan mejor brillo y aspecto a la ropa blanca. Absorben la luz ultravioleta y emiten un color azul claro que, gracias a este truco, oculta el amargo que puede tener la ropa.
Una vez hecho todo este camino, la ropa debería salir limpia de la lavadora y, a pesar de que haya muchas mejoras —todos conocemos una mancha que parece pegarse una vez a una prenda y quedarse en ella para siempre—, normalmente es así. Ahí dentro, más que un milagro, hay mucho en juego la química.
Materiales que se limpian sin jabón


Algunos químicos alemanes, copiando las características de la hoja de la planta lotus, han desarrollado piedras, papel o tejidos que sólo se limpian. Las hojas de Lotus son superhidrófobas (odio en griego al agua), donde las gotas de agua se resbalan totalmente. Incluso en días lluviosos las hojas se mantienen completamente secas. Esta delicadeza es muy interesante, ya que las gotas de lluvia arrastran la suciedad que se encuentra encima de las hojas (polvo, polen, etc.). ).
El botánico Wilhelm Barthlott descubrió el porqué a principios de los 90. Las hojas de lotus deben su acidez a los picores de 5-10 micrómetros de superficie. Las almohadas permiten que las gotas de agua sólo estén en contacto con la superficie de las hojas en algunos puntos y no puedan quedar sobre ellas. Caen por su cuenta.
En la imagen de la izquierda aparecen dos superficies superhidrófobas no naturales. En ambos casos, las gotas que se deslizarán con facilidad son perfectamente redondas. Estas superficies pueden, por tanto, limpiarse sin jabón o aditivo, sólo gracias al movimiento de la gota. El efecto de la hoja de lotus se consigue mediante el tratamiento químico de las superficies. El método fue patentado por el propio Barthlott con la marca Efecto Lotus (BASF) y ya se ha utilizado para limpiar fachadas.
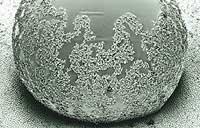
El efecto Lotus permite modificar las características superficiales de muchos materiales y facilita mucho la limpieza. Como se puede apreciar en la imagen, las gotas de agua, a medida que se mueven y caen, recogen el polvo y la suciedad y las llevan consigo.
Suavizantes textiles

Los suavizantes textiles también tienen una gran importancia en el proceso de limpieza. Son uno de los componentes de los detergentes de ropa, pero a menudo se añaden los tejidos después de limpiarlos. Los componentes activos de los suavizantes son surfactantes. Se pegan sobre la superficie de los tejidos, colocando las cabezas con carga positiva hacia el tejido negativo en el agua y las colas hacia el exterior. Producen en la superficie de las fibras textiles una capa suave que, además de proteger las fibras, confiere a la ropa una consistencia suave.
BIBLIOGRAFÍA
- Kaoru Tsujii Surface Activity, Principles, Phenomena and Applications, Academic Press (1998).
- D. J. Shaw Introduction to Colloid and Surface Chemistry, 4th Ed, Butterworth-Heinemann Ltd (1992).
- Efecto Lotus: O.E. Erbil, S.L. Demirel, et al. Science 299, 1377, 2003.
Gracias a Idurre Furones por sus enmiendas.