Miles de millóns paira detectar

Cando observan a auga, os ollos humanos ven un líquido transparente. Pero se miramos cos ollos pequenos dos químicos todo cambia. A auga non é auga, senón una complexa mestura de millóns de sustancias químicas. Do mesmo xeito, o viño non é viño, un anaco de queixo non é queixo e un deportista non é un deportista. Son mesturas de moitas moléculas.
O caso da auga está indicado, por exemplo, na etiqueta das botellas de auga. Ademais da auga, o líquido contén iones de cloruro, sulfatos, nitratos, etc., e moitas outras sustancias que non se especifican na etiqueta. E ás veces tamén están representados os iones que non se consideran na auga. "Auga sen sodio". Que significa iso? Que non hai ningún ion de sodio? Normalmente non, significa que o sodio, si existe, non é detectable. Na práctica é o mesmo, o que non se pode detectar non existe. Pero quizais o problema sexa a técnica utilizada paira a análise.
Os químicos non detectan una soa molécula. Non poden. Nin dúas moléculas; ou dez; ou mil. Deben conter polo menos mil millóns de moléculas paira detectar una sustancia. Parece mil millóns, pero é una bobada se falamos de moléculas. Hai moitas máis moléculas en case calquera lugar.
Pequenos e numerosos
Un exemplo é un ensaio cheo de auga. A molécula de auga é pequena, pero moi abundante. Paira poder visualizar as moléculas de auga, deberiamos multiplicar a sesión por dez millóns de veces, de dez centímetros a mil quilómetros como mínimo. Si uno dos extremos dun programa deste tamaño estivese en Bilbao, por exemplo, o outro estaría en Cádiz, aproximadamente. Si as moléculas de auga aumentasen na mesma proporción, terían una lonxitude de dous milímetros. Iso si, sería difícil separar as moléculas porque se moverían moi rápido. Pero serve paira facer una idea: pensa cantos moléculas de dous milímetros entran nun ensaio de mil quilómetros de lonxitude.
O físico Amadeo Avogadro atopou a cantidade: 18 mililitros de auga a 6,023 x 10 23 moléculas, case un cuatrilión. Un millón ten seis ceros e un billón ten doce ceros, mentres que o número de Avogadro, redondeado, ten vinte e tres ceros. É un número moi grande; si elimínase una pinga dun billón de moléculas, parece que non se notaría o cambio (nunha pinga de auga hai aproximadamente dezasete moléculas de trillón).
A verdade é que a molécula da auga é moi pequena, as moléculas orgánicas son moito máis grandes e con todo ocorre o mesmo: si a unha loncha de xamón quítaselle un billón de moléculas, o dono non sería consciente do perdido. Neste sentido, a detección de mil millóns de moléculas parece un milagre.
Separación de moléculas
Seguindo o mesmo exemplo de auga, pódese analizar o problema do límite de detección. Imaxinade que nesta selva de moléculas de auga mestúranse átomos de chumbo, é dicir, que a auga está contaminada a unha concentración de 50 ppm (50 gramos de chumbo nun millón de gramos de mostra). Coñecendo os pesos da auga e do chumbo, pódese estimar que existen ao redor de 231.100 moléculas de auga por cada átomo de chumbo. Ademais, as moléculas de auga son máis grandes que os átomos de chumbo. Por tanto, a detección de chumbo parece case imposible. Como se pode facer?
Está claro que ver moléculas non é o método de detección adecuado --e si existen técnicas de visualización-, xa que neste caso, ademais de localizar átomos de chumbo, habería que saber cantas moléculas de auga corresponden a cada una delas.
Pero tamén se pode facer outra cousa: antes de empezar a detectar, dividir as moléculas en grupos. Depende do tamaño, da carga eléctrica, do comportamento químico, etc. Una vez divididas as moléculas en grupos, cada grupo terá menos moléculas que identificar e poderase realizar una detección máis detallada que coa mostra inicial.
É o que se fai nos métodos de detección máis precisos existentes na actualidade: mesturar a mostra cun líquido ou un gas e introducila nun cromatógrafo. O cromatógrafo é una ferramenta de separación molecular na que as moléculas teñen que realizar un percorrido cheo de "trabas"; unhas moléculas forman o percorrido rapidamente e outras ven custadas. Á saída do percorrido, as moléculas aparecen divididas en grupos en función do tempo que tiveron que completar o percorrido. A instalación dun detector nesta saída permite realizar análise a cada grupo a medida que salga.
Líquido ou gas
Canto maior sexa a distribución, máis preciso é a análise posterior. Trátase de pescudar que cromatógrafo fará a mellor separación. A dúbida prodúcese entre o cromatógrafo de gases e líquidos. Crese que a mestura da mostra co gas e a gasificación da propia mostra é mellor opción que a mestura co líquido. En definitiva, una mostra dun determinado volume contén menos moléculas se se trata de gas.
Pero, como en todo, pode haber problemas. Non todas as moléculas son aptas paira estar en estado gaseoso, por exemplo si son moi grandes. Ademais, paira transformala en gas é necesario quentar a mostra e non todas as moléculas superan este proceso: degrádanse moito antes de evaporarse. Neste sentido, o líquido é máis útil. Una disolución é sinxela ao seleccionar o disolvente apropiado.
Por tanto, dependendo da sustancia a detectar, a distribución realízase mediante un cromatógrafo ou outro. O mesmo ocorre cos detectores. Elixir a máis adecuada en función da sustancia a detectar. Algúns detectores son moi especializados, serven paira detectar una determinada sustancia, pero con outros non son precisos ou non serven.
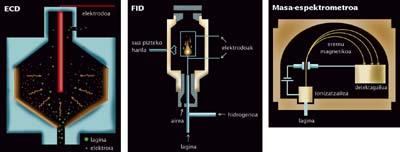
No ranking de detección das menores cantidades de sustancias, na actualidade hai que citar tres: FID, ECD e espectrómetro de masas. Detrás destes nomes atópanse os detectores máis precisos do mundo, os mellores detectores que existen paira buscar trazas moleculares. O tres utilízanse conxuntamente con cromatógrafos de gases. Pero non sempre. A parella formada polo espectrómetro de masas e a cromatografía de líquidos tamén está a alcanzar un gran éxito nos últimos tempos.

Inexacta
Catro métodos ofrecen resultados sorprendentes. Por diferentes motivos é difícil comparar o catro, pero si tivésemos que elixir o máis rechamante sería o cromatógrafo de gases/par ECD. O detector ECD é un detector extremadamente preciso: pode detectar só algúns piccogramas dunha sustancia (un pícogramo é o dun billón dun gramo). Si, por exemplo, utilizásemola paira detectar o cloruro de vinilo, bastarían ao redor de mil millóns de moléculas paira detectar ECD.
As parellas que forman os FID e o espectrómetro de masas con cromatógrafo de gases son menos precisas. Os nanogramos "só" chegan a detectarse, por exemplo, necesitan un billón de moléculas paira atopar as pegadas do cloruro de vinilo.
E que éxito ten o cromatógrafo de líquidos? Normalmente, en lugar de dar o peso que o cromatógrafo pode detectar, os vendedores dan concentración. Os datos máis optimistas son sorprendentes: algúns equipos son capaces de atopar concentracións de 500 granulomas por litro, é dicir, mantendo o exemplo do cloruro de vinilo, detectarían dez millóns de moléculas nun litro de disolución.
Versión de usuario

Os números deben tomarse con moito coidado. Estes datos son datos dos vendedores que indican os límites de detección do método. Pero a realidade sempre é máis complexa.
Cada método proporciona límites de detección en determinadas condicións. E mediante a medición de determinadas moléculas. O detector ECD é moi bo con sustancias halogenadas (por iso o cloruro de vinilo é un bo exemplo polo seu contido en cloro). Pola súa banda, o FID detecta moléculas carbonadas (moitas son pero moitas non conteñen carbono).
Con todo, tamén se pode dicir o contrario. As técnicas actuais satisfán a necesidade social de precisión na detección de sustancias.