Possibilité d'EPO par cellules encapsulées
Farmazian doktorea. Biofarmazia, Farmakozinetika eta Farmazia-teknologiako irakasle kolaboratzailea
Farmazia Fakultatea UPV-EHU, Vitoria-Gasteiz
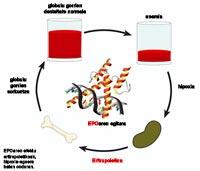
L'anémie est principalement due à la pénurie ou l'absence totale d'une hormone appelée érythropoïétine (EPO). Cette hormone favorise la création de globules rouges. Il est sécrété dans les reins, le foie, l'utérus, les cellules musculaires, les cellules endothéliales et les cellules productrices d'insuline, en fonction du degré d'oxygène des tissus. Lorsque le niveau d'oxygène des tissus est réduit, le régulateur HIF-1 s'écoule, ce qui augmente considérablement la production d'EPO.
La sécrétion des hormones EPO en quantités appropriées est essentielle. Ceci est dû au fait que si on sécrète moins que ce qui correspond, le nombre de globules rouges dans le sang est inférieur à suffisant et, par conséquent, il y a le risque que les patients souffrent d'une série d'altérations comme la fatigue, l'hypoxie tissulaire, la moindre tolérance au sport et l'hypertrophie cardiaque, l'augmentation de la taille des tissus cardiaques.
L'option la plus efficace pour traiter toutes ces modifications est de prendre l'EPO. Actuellement sur le marché se trouve le médicament avec EPO recombinant humain. Les patients souffrant d'anémie chronique reçoivent cette hormone 2 ou 3 fois par semaine, soit environ 1 000 à 9 000 unités par semaine. En outre, il a été récemment publié sous le nom de Darbepoetine une dérivée de l'EPO: eritropietine. Le principal avantage de ce nouveau dérivé est sa durée. Sa persistance dans l'organisme est prolongée, de sorte que sa fréquence est beaucoup plus faible.
Cependant, l'importance et le grand intérêt de l'érythropoïétine ne sont pas limités à l'anémie. Des études récentes indiquent que l'EPO peut être efficace pour traiter d'autres maladies chroniques telles que la thalassémie, l'arthrite ou le myélome. En outre, il peut être utile dans les troubles du système nerveux central, tels que les maladies de Parkinson ou Alzheimer, et dans les ischémies cérébrales (lorsque l'alimentation en sang est interrompue dans le cerveau) en raison de propriétés anti-inflammatoires et neuroprotectrices.
D'autre part, diverses études ont montré que l'hormone EPO est capable de moduler l'intensité de la réponse immunitaire et est également angiogénique, qui est, favorise la formation de vaisseaux sanguins.
C'est pourquoi il est facile de comprendre l'intérêt de nombreux groupes de recherche et entreprises biotechnologiques pour étudier en profondeur la molécule d'EPO et pour développer de nouveaux médicaments avec elle. L'objectif de ces efforts est d'améliorer les propriétés de l'hormone pour traiter efficacement ces maladies.
Cellules musculaires sécrétant EPO
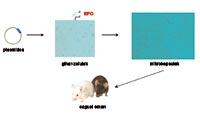
Compte tenu des propriétés et des caractéristiques de l'hormone EPO, il a commencé à travailler sur le développement d'une nouvelle stratégie de gestion EPO dans le laboratoire de pharmacie et de technologie pharmaceutique de Vitoria-Gasteiz. Pour atteindre cet objectif, nous avons utilisé la technologie des cellules microencapsulées. Tout d'abord, nous avons fabriqué des cellules musculaires qui sécrètent EPO, nous les avons placées en capsules de conception et de taille appropriée, et nous avons finalement donné les cellules encapsulées aux animaux.
Les capsules protègent les cellules musculaires de la réponse immunitaire. Il faut garder à l'esprit que ces cellules sont étranges pour l'organisme et donc détruire les systèmes immunitaires. Cependant, une préparation adéquate des capsules empêche la réponse du système immunitaire et, en se protégeant à l'intérieur des capsules, les cellules sont capables de circuler l'hormone pendant de longues périodes de temps. Par conséquent, il faut “les prendre” moins et le traitement est plus confortable pour le patient.
En plus de tout cela, compte tenu des propriétés angiogéniques de l'EPO et de la capacité de moduler l'intensité de la réponse immunitaire, des essais ont été effectués par différentes formes d'administration des capsules. Bien qu'il ait choisi la voie intraperitoneal traditionnelle, il a également testé la voie sous-cutanée avec de mauvais résultats en général dans cette technologie. Ce dernier chemin est beaucoup plus confortable, il serait donc d'un grand intérêt – et une grande avancée pour la technologie – si les capsules émises par cette voie permettaient de maintenir à long terme les effets thérapeutiques de l'EPO.
Résultats et débat
Les cellules à fournir ont été extraites de la souris de type C3H, puis transformées en laboratoire pour la sécrétion d'EPO. Ces cellules transformées ont été encapsulées et de nouveau incorporées aux souris.
Idéalement, plus de produits thérapeutiques circulant dans les cellules, moins de cellules et, en définitive, moins de capsules à incorporer aux animaux pour un même effet pharmacologique. Afin d'obtenir un moyen approprié, chaque capsule a déposé un maximum de 300-400 cellules. Des capsules de 480 micromètres ont ensuite été préparées et la production d'EPO des cellules internes a été mesurée.
Pour éviter qu'aucun type de réponse immunologique ne se produise chez les animaux après leur implantation, les capsules ont été soigneusement préparées. Nous les avons fait avec de l'alginate épuré, de surface lisse et de même taille. Ces caractéristiques sont très importantes du point de vue de la biocompatibilité pour éviter la réponse du système immunitaire.
Nous incorporons les capsules à deux types de souris, CH3 et Balb/c. Comme les cellules sont sortis des premières, ils ont les mêmes caractéristiques génétiques, mais les secondes ne, de sorte que leur probabilité de réponse immunitaire est plus élevé. La détermination de la dose aux animaux était une étape critique. En fait, si la dose était excessive, on risquait de voir apparaître des effets toxiques, même mortels d'animaux, alors que s'il était trop petit, on risquait de ne pas avoir d'effets thérapeutiques.
Les premières expériences ont été menées sur la souris C3H, pour laquelle 20 souris ont été divisées en 4 groupes (un groupe de contrôle par voie et un autre dans lequel les capsules ont été recueillies par voie). Pour connaître les émissions d'EPO, on a mesuré l'hématocrite animal, pourcentage de globules rouges dans le sang, pendant 100 jours par semaine.
Les résultats montrent clairement que l'hématocrite animal a considérablement augmenté dans les deux groupes, tant dans la collecte des capsules par voie intraperitoneal chez les souris que dans l'insertion sous-cutanée des capsules. Les valeurs de l'hématocrite étaient en outre supérieures à 80% tout au long, donc statistiquement significative par rapport aux groupes de contrôle.
Cependant, pour connaître la vraie valeur des cellules microencapsulées, il fallait fournir et démontrer leur efficacité aux êtres vivants qui ne possèdent pas leurs caractéristiques génétiques. Pour ce faire, nous avons réalisé la même expérience précédente avec 20 souris de type Balb/c et les résultats sont devenus statistiquement significatifs dans tous les cas: l'hématocrite animal est resté au-dessus de 75% pendant les 100 jours d'étude.
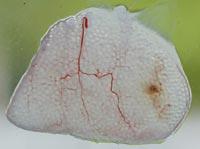
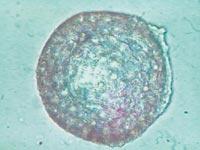
À partir de toutes ces données, nous tirons deux conclusions principales. D'une part, les capsules ont pu ralentir ou au moins réduire la réponse immunitaire des souris. D'autre part, l'introduction de cellules sous la peau peut être une occasion de développer un traitement chronique avec des capsules.
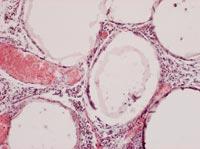
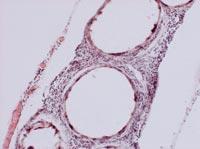
Pour analyser l'état des capsules, le 150e jour ont été tués certains animaux de chaque groupe et les capsules ont été récupérées. L'état et la structure des capsules étaient différents selon la voie d'administration des cellules. Ainsi, la plupart des capsules récupérées intraperitoneal étaient isolées et peu avaient une fibrose superficielle causée par une réponse immunitaire. Par ailleurs, les capsules appliquées par la voie sous-cutanée constituaient une structure ajoutée qui ne présentait aucune indication de fibrose par réponse immunitaire. Ces structures, en outre, étaient pleines de capillaires, en raison de la capacité de l'hormone EPO à produire la croissance des vaisseaux sanguins.
Au vu de ces résultats positifs initiaux, nous nous posons une nouvelle question: Pendant combien de temps les cellules émetteraient EPO avec une seule administration de capsules et sans utiliser de médicaments qui inhibent la réponse immunitaire? Pour répondre à cette question, nous avons réutilisé les souris Balb/c et les résultats ont été très significatifs. En fait, les cellules sous-cutanées ont sécrété l'EPO pendant 210 jours. Et cette durée est la plus longue qui ait jamais été atteinte par cette voie. Une des explications que nous donne l'hormone EPO elle-même pour obtenir des résultats positifs avec différents types de souris et différentes voies d'administration. En fait, l'hormone EPO a la capacité de promouvoir les vaisseaux sanguins et exerce diverses fonctions dans la réponse immunitaire.
En résumé, nous pouvons donc affirmer que l'encapsulation des cellules qui sécrètent cette hormone est une alternative technologique adaptée à l'administration chronique de l'EPO. Nos prochains objectifs seront d'allonger le traitement et d'ajuster la concentration d'EPO et donc l'hématocrite aux niveaux physiologiques.
Si vous voulez en savoir plusOrive, G. et autres 'Long-term expression of erythropoitein from myoblasts immobilized in biocompatible and ne73cularized microcapsules' Moléculaire therapy Approuvé pour publication Schneider, B.L. et d'autres 'prevention of the initial host immuno-inflammatory response determines the long-term survival of encapsulated myoblasts genetically engineered for erythropoiesis delivery' Molecular therapy 7: 506-514. (2003). |