CRISPR, technique d'édition du génome : bénéfices et inquiétudes
« Je ne l’utilise pas encore, mais je vais certainement commencer cette année », affirme le génétique de l’UPV José Antonio Rodríguez Pérez. Rodríguez veut utiliser la technique CRISPR pour étudier une mutation liée à la leucémie. Pour étudier l'effet de cette mutation, vous avez besoin de cellules mutées. « Jusqu’à présent, la seule option était de prendre des cellules des patients, mais c’est très difficile. Il est beaucoup plus facile de mettre cette mutation dans les cellules que nous avons en laboratoire”. Vous pouvez le faire avec CRISPR.

La technique CRISPR permet d'éditer l'ADN avec une grande précision. Vous pouvez retirer les fragments d'ADN où vous le souhaitez et les remplacer par de nouveaux fragments. Ce n'est pas nouveau, il y avait déjà d'autres techniques pour le faire. «Le plus important, c’est qu’il a beaucoup simplifié et embrassé les choses», a souligné Rodríguez.
D'autres instruments très similaires au CRISPR, comme TALEN et ZFN. “Ces appareils font la même chose que le CRISPR, mais pour les utiliser, vous devez concevoir et assembler une protéine qui est très cher. Avec le CRISPR vous devez concevoir une molécule d'ARN qui est très bon marché. Supposons qu’il faut 100 euros pour cela, car avec les techniques précédentes il faudrait des milliers d’euros.»
Démocratisation et démocratisation
Faciliter tant les choses ouvre beaucoup de possibilités. « Vous pouvez essayer des choses différentes. Beaucoup de projets sont basés sur des tests et si vous devez investir 5000 euros, vous n’allez pas commencer, mais si vous êtes 200 euros, vous pouvez essayer”, explique Rodríguez. En outre, «il a démocratisé ces expériences, qui pourront être réalisées par beaucoup de gens qui ne pouvaient pas auparavant. Auparavant, nous ne pouvions pas faire ce genre de petits projets laboratoires, mais maintenant oui avec CRISPR. C’est pourquoi il s’est étendu si vite et de cette façon exponentielle.»
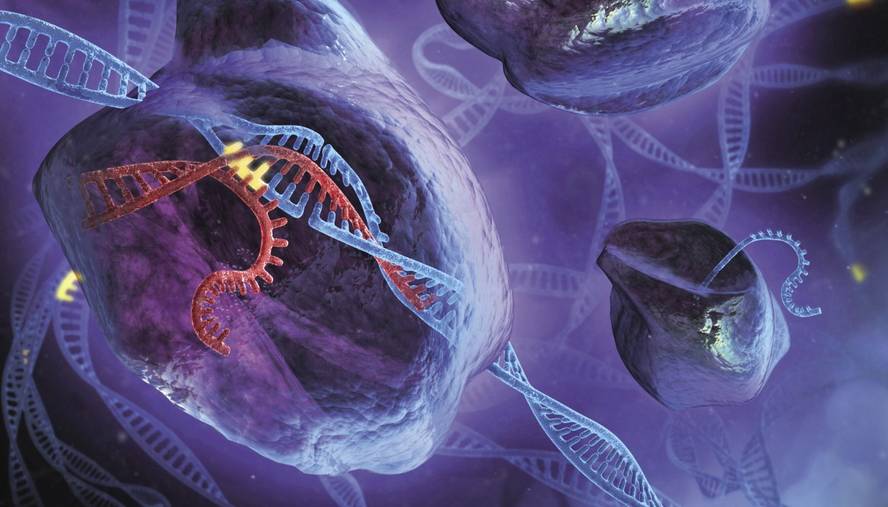
En 2012 a été publié Sciencen Jennifer Doudna et Emmanuelle Charpentier que le complexe enzymatique CRISPR-Cas9 de bactéries pourrait être utilisé comme outil d'édition génétique. Ce complexe est formé par un guide RNA et l'enzyme Cas9. L'enzyme coupe l'ADN à l'endroit qui vous donne le guide ARN. De cette façon, vous pouvez modifier le génome où vous le souhaitez, synthétisant l'ARN complémentaire à l'endroit.
Il offre d'énormes possibilités de recherche de base et ses applications peuvent être multiples. La thérapie génique est l'un des plus encourageants. « Un pas géant a été franchi », affirme la génétique de l’UPV Ana Aguirre Escobal. “Jusqu'à présent, avec la thérapie génique, en plus d'être très cher, on obtenait très peu de bons résultats, parce que la technique n'était pas bonne. Maintenant, cependant, on s’attend à ce que ces résultats s’améliorent beaucoup.»
Rodríguez accepte: « Dans certaines maladies, cela peut être très important. Dans de nombreuses maladies monogéniques, le gène et les défauts sont bien identifiés et comment les corriger. Mais jusqu'à présent, on ne pouvait pas corriger un gène. Si un gène était mal, une autre copie directe de ce gène était introduite. Cette copie était introduite par un vecteur et insérée aléatoirement dans le génome, et il fallait attendre que ce gène remplisse sa fonction. Maintenant, vous pouvez entrer la copie correcte à la place qui correspond à ce gène, en supprimant la précédente. « Maintenant les gènes peuvent être vraiment corrigés », nuance Rodríguez.
Travailler le chemin vers la thérapie
En 2014, des chercheurs du MIT ont utilisé pour la première fois la technique CRISPR pour soigner une maladie chez les animaux adultes. Elle a été employée sur la souris pour corriger la mutation qui produit la maladie hépatique appelée tyrosinémie chez l'homme. Ils ont réussi à guérir le mal, mais en même temps, ce travail a montré que la technique avait également quelques problèmes à résoudre.
D'une part, la technique utilisée pour introduire l'enzyme Cas9 et le guide ARN dans les cellules du foie, l'injection à haute pression, ne convient pas pour être appliquée chez l'homme. Et d'autre part, seulement dans l'une des 250 cellules ont réussi à corriger la mutation. Dans ce cas, il suffit de guérir la maladie, mais il est très probable que ce ne soit pas dans de nombreuses autres maladies.
D’autre part, « le CRISPR a encore des effets inspécifiques – ajoute Rodriguez –, parfois on peut associer l’ARN ailleurs dans le génome. La technique reste optimisée, mais il y a la possibilité de l'améliorer. Par exemple, l’enzyme Cas-9 a été utilisée jusqu’à présent, mais d’autres testent et peuvent être plus spécifiques.»
L'équipe du MIT qui a réussi à guérir la tyrosinémie chez les souris a déjà réussi à améliorer la technique. En Février, il a publié un moyen plus sûr et efficace pour atteindre les cellules du foie des souris. Le guide de l'ARN et le fragment direct d'ADN ont été introduits par un virus et un ARN messager codant l'enzyme Cas9 par des nanoparticules. Ainsi, dans une cellule sur 16, la correction a été obtenue. Et ils ont à peine détecté des effets non spécifiques.
Il y a d'autres exemples, par exemple, qu'en décembre trois groupes de recherche ont montré dans des articles publiés simultanément dans Science qu'ils ont réussi à améliorer la dystrophie musculaire Duchenne. La question va vite, mais Rodríguez pense qu'il faudra encore du temps pour l'appliquer aux humains: « Je ne pense pas que nous sommes en mesure de le faire l’année prochaine, mais dans quelques années, je pense qu’il sera possible de faire des changements avec une grande précision chez les humains. Ensuite, nous devrons vérifier si elle est autorisée ou comment elle est contrôlée”.
Préoccupations sur la table
En fait, comme la capacité de la technique est devenue claire, et compte tenu de la rapidité avec laquelle elle s'étend, les préoccupations éthiques ont également augmenté. «La simplicité est la partie positive de cette technique, mais aussi le négatif, car «jouer» avec cet outil est facile», a souligné Rodríguez. « Je vois surtout des aspects positifs. Et c’est que les risques de la technique sont là, mais ceux d’autres techniques sont comme il y a longtemps.»
D'autres, pour leur part, accordent une plus grande importance aux risques. En mars 2015, un groupe d'experts s'est opposé au CRISPR et aux autres techniques de transformation des embryons humains dans un article publié dans la revue Nature. Ces experts croyaient que cela pouvait arriver bientôt. Et un mois plus tard, des chercheurs de l'Université de Sun Yats en Chine ont publié la transformation des embryons humains par la technique CRISPR. Ils ont utilisé des embryons qui ne pouvaient pas se développer, mais l'expérience a mis fin aux préoccupations existantes.
Face à cette situation, les académies de science et de médecine américaines, la Royal Society de Londres et l'Académie chinoise des sciences ont organisé une réunion pour parler de ces préoccupations. En décembre, 500 experts du monde entier se sont réunis à Washington et sont parvenus à un accord provisoire : ne pas interdire l'édition du génome humain de recherche, mais l'utilisation d'embryons modifiés pour les grossesses.

« Une bonne chose de la science est que tout est très public. On parle et on écoute et on prend des décisions en fonction de ce qui se passe », affirme Aguirre. Aguirre est ancien président du Comité d'éthique de la recherche sur les questions biologiques et les organismes génétiquement modifiés de l'UPV/EHU, et le débat qui a maintenant été généré à l'occasion du CRISPR n'a pas été nouveau. « Je me souviens que dans les années 70, lorsque les premières techniques d’ingénierie génétique sont apparues, les experts se sont réunis à Asilomar (Californie). Ils ont décidé d'imposer un moratoire. Il a fallu attendre quelques années pour vérifier que les techniques étaient sûres. Maintenant quelque chose de semblable s'est passé, ils ont parlé et convenu: « Avant de commencer à parler des applications, faisons des cuisines en laboratoire pour améliorer, optimiser et rendre le plus sûr possible. »
Le débat est ancien. « Des choses qui jusqu’à présent étaient lointaines ou très théoriques, ont maintenant été plus proches et réalisables, ce qui a fait naître un vieux débat semi-mort ces dernières années. » En outre, Aguirre estime qu'il ya un autre facteur qui a fait augmenter la préoccupation: « Certains ont averti que de nombreuses lois régissant et régulant les organismes génétiquement modifiés, telles qu’elles sont rédigées, excluent la technique CRISPR. » En fait, dans ces lois on parle de la recombinaison et de l'ADN étrange, mais dans la technique du CRISPR il n'y en a pas. «Je n’ai aucun doute que ces lois s’adapteront pour réguler la nouvelle technique, mais il est vrai qu’en ce moment elle n’a pas eu lieu».
Cependant, sa régulation ou sa régulation varie beaucoup de pays à pays. Dans des pays comme le Japon, la Chine et l'Inde, il existe des normes qui interdisent la transformation génétique en embryons humains, mais elles n'ont pas d'effets juridiques. La réglementation en Russie et en Argentine est très ambigue.Aux États-Unis, le financement avec de l'argent public est interdit, mais la loi n'interdit pas l'application clinique. Et en Europe, en général, elle est interdite à la clinique et limitée à la recherche. Récemment, au Royaume-Uni, les chercheurs de l'Institut Francis Crick ont été autorisés à utiliser la technique CRISPR pour étudier le développement des embryons humains.
Peurs et attentes
Les préoccupations et les peurs que le CRISPR a engendrées sont de toujours. « Fondamentalement, en ce qui concerne les animaux et les plantes, il faut bien analyser si ces transformations sont sûres ou non, si les organismes qui sont générés peuvent représenter un risque pour l’être humain ou les écosystèmes », a expliqué Aguirre. « Quant à l’être humain, je crois qu’aux questions de sécurité s’ajoute le concept d’individu. Quand on parle de changer la séquence d’ADN, on devient nerveux parce qu’il nous semble qu’elle va en quelque sorte influencer notre individualité.»
Cependant, Aguirre considère que dans la pratique le débat passe à un autre plan: Si nous avons une personne avec une maladie génétique à proximité et qu'il y a une chance de la guérir, alors c'est ce qui nous importe. Je pense que quand vous voyez que vous avez des applications réelles, qui peuvent améliorer la vie des gens, que la société verra mieux ces techniques.”
C'est ce qui s'est passé avec de nombreuses avancées scientifiques. « Cela a eu lieu avec une fécondation assistée. Au début, il était méprisable, mais peu à peu la société l’a demandé, et les enfants nés avec la fécondation déjà assistée ne se voient plus comme des démons, comme on voyait les initiales ».
Cependant, la transformation génétique peut avoir des applications plus discutables que la guérison des maladies, comme la transformation des embryons pour améliorer certaines caractéristiques. Cependant, Aguirre ne voit pas pour le moment trop de raisons de s'inquiéter, “Bien qu'il semble plus proche parce qu'il peut permettre la technique, je pense que c'est encore une utopie, une peur théorique”.
En outre, il souligne que le contrôle est rigoureux: “Toute technique de changement génomique, comme la thérapie génique, nécessite de passer par différents comités. Dans l'État espagnol, par exemple, il y a une commission nationale très exigeante et il faut obtenir son autorisation. Mais de plus, si l'on veut faire des tests dans un hôpital, il faut aussi passer par les comités éthiques de cet hôpital et de la communauté autonome. Il existe déjà une structure et, en tout cas, ce contrôle durcira dès maintenant, car je ne crois pas que l'amélioration génétique ait un support social. Je ne pense donc pas qu’il y ait des motifs de préoccupation.»
Risque de transformation des écosystèmes
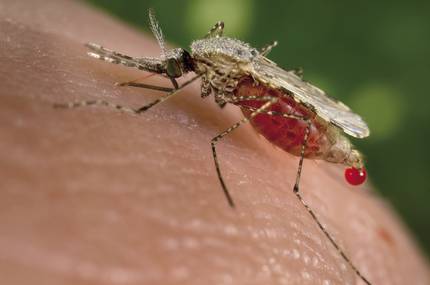
Une autre préoccupation est l'effet que les êtres vivants génétiquement modifiés peuvent avoir sur les écosystèmes. Et ces inquiétudes ont été suscitées par un autre travail publié en novembre. Des scientifiques de l'Université de Californie ont créé des moustiques transgéniques résistants au parasite responsable du paludisme. En outre, grâce à la technique CRISPR, 99% des descendants de moustiques modifiés héritent du gène de l'anticorps et le gène est actif dans ces moustiques. Ainsi, ils ont estimé que 10 générations seraient suffisantes pour se développer dans une population.
La capacité d'incidence sur la population a suscité une grande préoccupation. Aguirre fait également confiance aux contrôles stricts qui existent. « D’autres moustiques transgéniques contre le paludisme, réalisés par une autre technique, ont déjà été libérés. Mais pour cela, il a fallu 10 ans de contrôles. L'obtention de ce type d'autorisation nécessite de nombreuses et très profondes études et évaluations qui permettent de connaître les risques et les avantages. Il est vrai que dans ces cas, le risque zéro n'existe pas. Dans ce cas, après avoir mis tous les rapports sur les risques et les avantages sur la table, et compte tenu de l'énorme niveau de paludisme, les politiciens ont décidé de libérer les moustiques transgéniques. En définitive, c’est un outil qui met la science à la portée de la société et que celle-ci doit décider quoi faire avec elle ».





