Ils ont réussi à réduire de 90% les tumeurs de vessie avec des nanorrobots
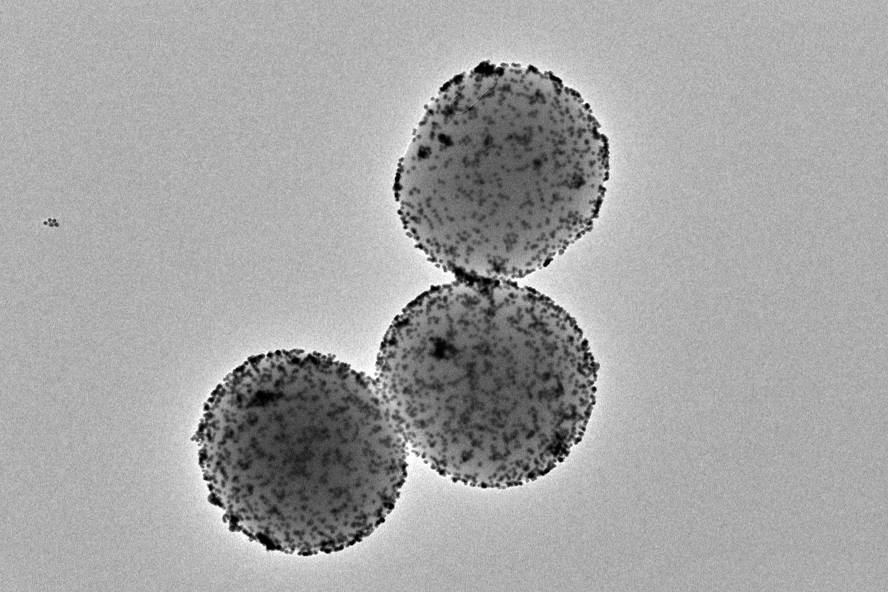
Ils ont réussi à réduire de 90% les tumeurs de vessie sur la souris, avec une dose unique de nanorrobots. Ces petites nanomachines sont propulsées avec de l'eau d'urine, atteignent la tumeur et sont attaquées avec un radio-isotope superficiel. Ce travail, mené par l'Institut catalan de bioingénierie et CIC biomaGUNE, a été publié dans la revue Nature Nanotechnology.
Le cancer de la vessie est l'une des tumeurs les plus répandues au monde et la quatrième tumeur chez les hommes. Bien que sa mortalité ne soit pas élevée, elle est l'une des plus difficiles à guérir et près de la moitié des tumeurs réapparaissent à cinq ans. Dans les traitements actuels, les médicaments sont administrés directement à l'intérieur de la vessie, mais malgré de bons taux de survie, l'efficacité thérapeutique est faible.
Ainsi, l'utilisation de nanoparticules est une option prometteuse, car ils sont capables de transmettre directement l'agent thérapeutique à la tumeur. Ils mettent en évidence les nanorrobots, nanoparticules capables de se déplacer dans le corps.
Les nanorobots utilisés dans cette étude ont une sphère poreuse de silice avec plusieurs composants de fonction spécifique en surface. L'une d'elles est l'enzyme uréase, une protéine qui réagit avec l'urée présente dans l'urine et qui confère à la nanoparticule la capacité de la propulser. Un autre élément clé est l'iode radioactif, un radio-isotope fréquemment utilisé pour le traitement localisé des tumeurs.
L'étude sur les souris montre qu'avec une seule dose, le volume de la tumeur diminue de 90%. Il est beaucoup plus efficace étant donné que les patients atteints de ce type de tumeurs doivent fréquenter l'hôpital 6 à 14 fois. On étudie actuellement la réapparition de ces tumeurs après le traitement.
Jusqu'à l'intérieur de la tumeur
Des études antérieures ont montré que la capacité d'autopropulsion des nanorrobots permet d'atteindre tous les murs de la vessie. Ce nouveau travail va plus loin en vérifiant que les nanoparticules se déplacent dans la vessie et s'accumulent spécifiquement dans la tumeur. En outre, ils ont vu qu'en plus d'atteindre la tumeur, ils pénètrent à l'intérieur, ce qui augmente l'influence du radiopharmaceutique.
Le défi était de clarifier pourquoi les nanorrobots sont capables de pénétrer à l'intérieur de la tumeur. Les nanorrobots n'ont pas d'anticorps spécifiques pour reconnaître la tumeur et le tissu tumoral est généralement plus rigide que le tissu sain.
Il a été observé que ces nanorrobots ont la capacité de décomposer la matrice extracellulaire de la tumeur, car ils élèvent localement le pH par une réaction chimique d'autopropulsion. Ainsi, les chercheurs sont arrivés à la conclusion que les nanorrobots se heurtent à l'urothélium comme si d'un mur était traité, mais dans la tumeur, étant plus enflammé, entrent et s'accumulent sur lui.
En outre, l'administration localisée de nanorrobots transportant le radioisotope réduit le risque d'effets indésirables et l'accumulation élevée dans le tissu tumoral augmente l'effet thérapeutique.
Les chercheurs ont expliqué que ce travail a ouvert les portes à l'utilisation d'autres radio-isotopes ayant une plus grande capacité d'incidence thérapeutique.