Han aconseguit reduir en un 90% els tumors de bufeta amb nanorrobots
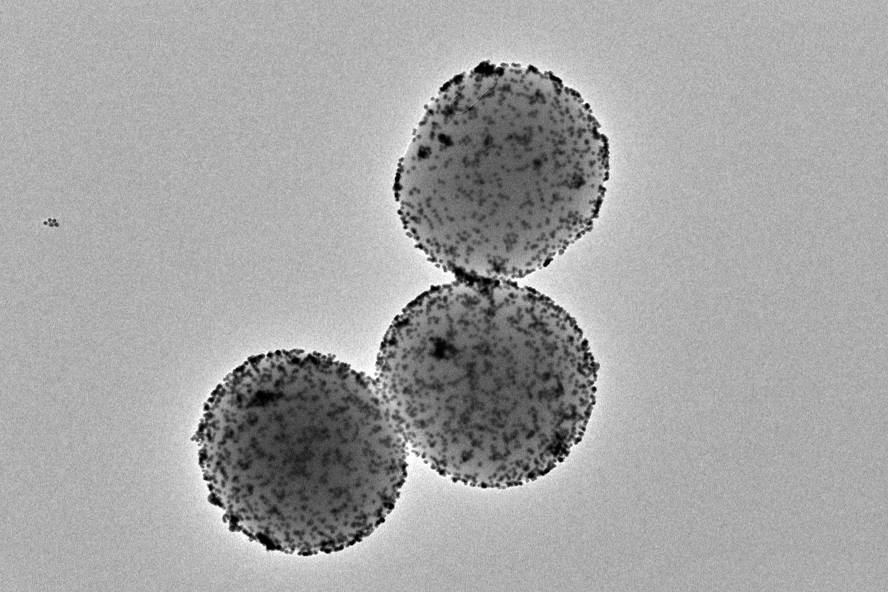
Han aconseguit reduir en un 90% els tumors de bufeta en el ratolí, amb una sola dosi de nanorrobots. Aquestes petites nanomaquinas es propulsen amb aigua d'orina, arriben al tumor i són atacades amb un radioisòtop superficial. Aquest treball, liderat per l'Institut Català de Bioingeniería i CIC biomaGUNE, ha estat publicat en la revista Nature Nanotechnology.
El càncer de bufeta és un dels tumors amb major taxa d'incidència del món i el quart tumor més freqüent en els homes. Encara que la seva mortalitat no és alta, és una de les més difícils de curar i gairebé la meitat dels tumors reapareixen als cinc anys. En els tractaments actuals, els fàrmacs s'administren directament a l'interior de la bufeta, però malgrat les bones taxes de supervivència, l'eficàcia terapèutica és baixa.
Així, la utilització de nanopartícules és una opció esperançadora, ja que són capaces de transmetre directament l'agent terapèutic al tumor. Destaquen els nanorrobots, nanopartícules capaces de moure's dins del cos.
Els nanorobots utilitzats en aquest estudi tenen una esfera porosa de sílice amb diversos components de funció específica en superfície. Una d'elles és l'enzim ureasa, una proteïna que reacciona amb la urea present en l'orina i que confereix a la nanopartícula la capacitat de propulsar-la. Un altre component clau és el iode radioactiu, un radioisòtop utilitzat sovint per al tractament localitzat de tumors.
En l'estudi amb els ratolins s'observa que amb una sola dosi el volum del tumor disminueix un 90%. És molt més eficient tenint en compte que és freqüent que pacients amb aquesta mena de tumors hagin d'acudir a l'hospital de 6 a 14 vegades. Ara s'està estudiant la reaparició d'aquests tumors després del tractament.
Fins dins del tumor
En estudis anteriors s'ha observat que la capacitat d'autopropulsió dels nanorrobots permet arribar a totes les parets de la bufeta. Aquest nou treball va més enllà en comprovar que les nanopartícules es mouen en la bufeta i s'acumulen específicament en el tumor. A més, han vist que, a més d'arribar al tumor, penetren a l'interior, la qual cosa augmenta la influència del radiofàrmac.
El repte va ser aclarir per què els nanorrobots són capaços de penetrar a l'interior del tumor. Els nanorrobots manquen d'anticossos específics per a reconèixer el tumor i, generalment, el teixit tumoral és més rígid que el teixit sa.
S'ha observat que aquests nanorrobots tenen la capacitat de descompondre la matriu extracelul·lar del tumor, ja que eleven localment el pH mitjançant una reacció química d'autopropulsió. Així, els investigadors han arribat a la conclusió que els nanorrobots xoquen amb l'urotelio com si d'una paret es tractés, però en el tumor, en ser més inflamat, entren i s'acumulen en ell.
A més, l'administració localitzada de nanorrobots que transporten el radioisòtop redueix el risc d'efectes adversos i l'elevada acumulació en el teixit tumoral augmenta l'efecte terapèutic.
Els investigadors han explicat que aquest treball ha obert les portes a la utilització d'altres radioisòtops amb major capacitat d'incidència terapèutica.