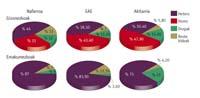
Evolución de las terapias en 25 años
Samuel Broder es uno de los investigadores que colocó la primera piedra en la lucha contra el sida. Durante estos veinticinco años publicó en julio en la revista Science Translational Medicine un artículo que explica la trayectoria de la investigación anti-sida. Ha intercalado en el artículo sus vivencias y las convicciones y sentimientos de la sociedad, con detalles sobre los medicamentos. Fue uno de los especialistas que trató a algunos de los pacientes antiguos afectados por el SIDA.
"Los médicos saben que ahora tienen varios medicamentos que administrar a sus pacientes, pero muchos no recuerdan cuál era la situación en aquella época", ha afirmado Broader. Tampoco estaba claro si existían retrovirus patógenos para el hombre.
Sin embargo, "el hecho de considerar que detrás del SIDA había un retrovirus no solucionó mucho: los retrovirólogos, en general, consideraban más importante buscar una vacuna antivirus que desarrollar terapias antirretrovirales. Se consideraba que las terapias antirretrovirales serían inútiles y los pacientes, médicos e investigadores estaban descontentos".
A pesar de que esta convicción ralentizó las investigaciones sobre antirretrovirales, algunos investigadores decidieron seguir este camino. Entre otros, Broader. Trabajando en el Instituto Nacional del Cáncer de Estados Unidos, por primera vez pudieron demostrar que un determinado medicamento inhibía parcialmente la replicación del VIH. Fueron los primeros resultados de un trabajo conjunto realizado por diversas compañías farmacéuticas privadas y centros académicos.
Los resultados se dieron a conocer el 28 de junio de 1985. No pasaron dos años desde esta presentación hasta que fue aceptada como tratamiento por la Administración de Alimentos y Medicamentos (FDA) de Estados Unidos. La farmacia fue bautizada como TR. De hecho, se trataba de un medicamento creado en 1964 y confinado en un laboratorio. Fue utilizado en algunas pruebas contra el cáncer y posteriormente descartado por su toxicidad. En cuanto al tratamiento del sida, los beneficios eran mayores que los daños.
Este buen resultado animó a los investigadores a seguir en el camino abierto. La sociedad también estimuló a investigadores y administraciones a buscar la curación de esta enfermedad. "Fueron especialmente los grupos de gays estadounidenses los que presionaron, ya que en ellos se detectó primero la enfermedad y murieron muchos", explica Daniel Zulaika, coordinador del Plan de Sida de Osakidetza. "Esta presión social aceleró enormemente los pasos habituales en los ensayos clínicos. El camino que recorre un fármaco durante dos o tres años era el resultado --dio-- de antirretrovirales que se llevaban a cabo durante varias semanas o meses, lo que permitió el éxito de estas terapias". Zulaika asumió la labor de coordinador del Plan de Sida en 1987, y en la actualidad continúa.
Repentización
Aprovecharon el rápido desarrollo de los tratamientos y, según ha escrito Broder, "para 1990 teníamos bastante claro que el sida dejaría de ser una enfermedad mortal y podría ser tratable".
Pero la verdadera revolución vino en 1996. Zulaika recuerda: "En un congreso de Vancouver se dieron los resultados de una investigación: Un grupo de pacientes moribundos de 33 kilos de peso resucitaron al recibir el tratamiento que se estaba investigando. Como es normal, inmediatamente, ese mismo año y en 1997, los pacientes comenzaron a recibir esta terapia en casi todos los sistemas sanitarios. En la CAPV, por ejemplo, contamos con 2.200 pacientes que tomaban esta terapia para finales de 1997".
Este avance repentino se debió a dos motivos: el desarrollo de un nuevo tipo de medicamentos que combinaron con otros ya desarrollados. De este modo, los tratamientos se hicieron mucho más eficientes.
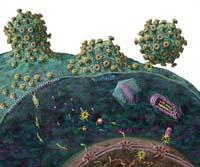
La clave de la terapia combinada es atacar al virus en más de un momento del proceso infeccioso. Para que se produzca la infección, los virus entran primero en la célula. A continuación comienza el proceso de introducción de sus genes en el genoma de la célula huésped. Al tener la información almacenada en una cadena de ARN, realizan una copia de la misma y la convierten en una doble cadena de ADN. Esta copia se genera mediante la enzima denominada transcriptasa inversa del virus.
El siguiente paso es introducir la cadena de ADN copiada en el genoma de la célula huésped y, por último, cuando la célula genera cadenas de proteínas a partir de la información de estos genes, se cortan para producir proteínas funcionales. De hecho, varias proteínas se sintetizan a partir de los genes unidas. Estos dos últimos pasos son realizados por otras dos enzimas del VIH, la integrasa y la proteasa, respectivamente. A partir de ahí, los virus sólo tienen que unir correctamente los componentes de los nuevos virus y sacarlos de la célula para completar el ciclo.
Cada medicamento, una tarea
Cada medicamento antirretroviral tiene como objetivo interrumpir un paso concreto en el proceso infeccioso y ya existen seis familias de medicamentos. Los primeros que se desarrollaron, como AZTI, afectan a la enzima transcriptasa inversa. En definitiva, utilizando la cadena de ARN como modelo, esta enzima va formando la cadena de ADN, añadiendo nucleótidos. Pues bien, estos medicamentos tienen una estructura parecida a los nucleótidos y sustituyen a los verdaderos nucleótidos en la cadena de ADN. Así, bloquean la cadena y rompen la síntesis del ADN. Existen análogos de los cuatro nucleótidos que forman cadenas de ADN y más de uno para cada nucleótido.
Los medicamentos de otra familia también tienen la función de interrumpir la transcriptasa inversa, pero actúan de otra manera: se asocian a la enzima y distorsionan su estructura tridimensional. Esto hace que la enzima no funcione correctamente.
Esta revolución en el tratamiento anti-sida se produjo cuando se desarrollaron medicamentos contra las proteínas. Al no poder generar proteínas funcionales, es imposible completar el ciclo a los virus. La FDA aprobó en diciembre de 1995 el primer medicamento contra las proteínas, el Saquinavir. Desde entonces se han desarrollado otros fármacos con el mismo efecto, así como potenciadores que permiten a estos inhibidores permanecer más tiempo en la sangre.
Recientemente (a partir de 2006) han empezado a aparecer medicamentos con otros efectos. Dos familias de medicamentos tienen la función de evitar que el virus entre en la célula huésped y otra de convertir la integrasa en una enzima inutilizable. Cada una de estas familias tiene comercializado un medicamento y hay muchos estudios en marcha para avanzar en estas vías.
Para Zulaika, "ha sido muy importante no haber dejado de investigar y seguir siendo investigaciones punteras y dinámicas". Veinticuatro medicamentos antirretrovirales ya existen en el mercado y, como ya se ha dicho, se combinan de diferentes efectos para atacar el virus con mayor dureza.
De los centros de investigación a los usuarios
Los medicamentos comercializados por centros de investigación, compañías farmacéuticas u otros han demostrado su eficacia en el momento de su lanzamiento. A partir de ahí, los profesionales que han trabajado con estos medicamentos transmiten sus experiencias en sociedades científicas, congresos, etc. "en los que se define la mejor combinación de medicamentos en términos de coste y eficacia", explica Zulaika.

A partir de estas experiencias se publican las guías clínicas. En ellos se recomienda la combinación de este tipo de medicamentos, evitar su administración de una vez por todas, incluso apuntando a tener en cuenta en función del estado clínico de los pacientes, etc. Cada país tiene sus propias guías. Existe una guía europea y las sociedades científicas utilizan sus guías...
La Asociación Clínica Europea del Sida (EADS), por ejemplo, dispone en su página web de una guía para el tratamiento de pacientes adultos infectados por el VIH. La guía ofrece diferentes opciones de tratamiento de pacientes. En general, recomienda utilizar análogos de dos nucleótidos junto con otro inhibidor de la transcriptasa inversa o de la proteasa potenciada.
Dado que hay más de un medicamento por tipo, ofrece diferentes combinaciones posibles y determina en qué casos hay que utilizar o evitar cada uno de ellos. Se tiene en cuenta la situación clínica de los pacientes, es decir, si están embarazadas, tienen riesgo cardiovascular, han desarrollado otra enfermedad, etc.
"Sin embargo, se puede decir que todas las guías son equivalentes --explica Zulaikak--. Si las guías son equivalentes, diría que todos los países desarrollados utilizan terapias más o menos iguales". Tampoco ha notado diferencias significativas en el proceso de introducción de medicamentos en los sistemas sanitarios: "A veces Estados Unidos ha estado un poco más avanzado que el resto de países, pero otras veces no".
También en las administraciones se ha ido desarrollando la lucha contra el sida. Prueba de este desarrollo es el "gasto en tratamientos antirretrovirales", señala Zulaika: En 1997 se invirtieron 9 millones de euros en la CAPV y en 2009 36,9 millones. Esta cantidad supone el 1% del gasto total del departamento de sanidad. "Es terrible --dice Zulaikak--. Ten en cuenta que el departamento de sanidad gasta un tercio de los presupuestos generales de la CAPV. Pues todo ese dinero se invierte en 4.600 pacientes".
El gasto anual por paciente se ha duplicado prácticamente en este periodo: Pasa de 4.100 euros a 8.015 euros. "Cada vez hay más pacientes y los tratamientos son cada vez más caros. Son más caros en la medida en que son más eficientes".
Este gasto ha mejorado la supervivencia y la calidad de vida de los pacientes, en la medida en que hace 25 años no se podía imaginar. Hay que tener en cuenta que "al principio se pensaba que los tratamientos servirían para poco", dice Zulaika. Pues gracias a ellos, el sida es ahora una enfermedad crónica. Es cierto que no se ha conseguido eliminar el virus del cuerpo infectado. Sin embargo, manteniendo controlada la cantidad de virus, el sistema inmunológico de los pacientes no se reduce, por lo que no aparecen otras enfermedades que acababan provocando la muerte de los pacientes.