Farmacogenética, base de la medicina personalizada
EHUko Genetika, Antropologia Fisikoa eta Animalien Fisiologia Saila; EHUko Genetika, Antropologia Fisikoa eta Animalien Fisiologia Saila; Farmakologia
Medikamenduen Garapen, Balioztatze eta Erabilera Arrazionala masterreko ikaslea; EHUko Farmakologia Saila eta Centro de Investigación Biomédica en Red de Salud Mental, CIBERSAM
EHUko Genetika, Antropologia Fisikoa eta Animalien Fisiologia Saila; EHUko Genetika, Antropologia Fisikoa eta Animalien Fisiologia Saila; Farmakologia
Medikamenduen Garapen, Balioztatze eta Erabilera Arrazionala masterreko ikaslea; EHUko Farmakologia Saila eta Centro de Investigación Biomédica en Red de Salud Mental, CIBERSAM
Askaiturrieta Ostolaza, Ziortza
EHUko Genetika, Antropologia Fisikoa eta Animalien Fisiologia Saila; EHUko Genetika, Antropologia Fisikoa eta Animalien Fisiologia Saila; Farmakologia
Medikamenduen Garapen, Balioztatze eta Erabilera Arrazionala masterreko ikaslea; EHUko Farmakologia Saila eta Centro de Investigación Biomédica en Red de Salud Mental, CIBERSAM
EHUko Genetika, Antropologia Fisikoa eta Animalien Fisiologia Saila; EHUko Genetika, Antropologia Fisikoa eta Animalien Fisiologia Saila; Farmakologia
Medikamenduen Garapen, Balioztatze eta Erabilera Arrazionala masterreko ikaslea; EHUko Farmakologia Saila eta Centro de Investigación Biomédica en Red de Salud Mental, CIBERSAM
¿Has pensado alguna vez por qué el café no afecta igual a todas las personas? Algunos no pueden tomar el café a partir de una hora, porque lo mantienen durante mucho tiempo en el cuerpo, y luego no pueden dormir. A menudo escuchamos frases como "una aspirina no me hace nada", "el ibuprofeno me viene mejor" o "Tengo que tomar un ibuprofeno de 600 mg para notar el efecto". Además, es habitual que el médico cambie la dosis del fármaco y aconseje su devolución la semana siguiente. Esto significa que cada individuo responde de forma diferente a los fármacos y que necesitamos dosis diferentes.
Farmacogenética
Es sabido que muchos fármacos no son eficaces en una parte de la población, y este es uno de los retos que se está dando en la actualidad en medicina. Por ejemplo, los fármacos antihipertensivos muy utilizados, como los betabloqueantes, son parcialmente eficaces o ineficaces en el 70% de los pacientes. La administración a pacientes no afectados por estos fármacos es perjudicial (por sus efectos secundarios) e inútil, tanto en términos de efecto como económicos. Sin embargo, no hay pruebas que permitan predecir quién responde tras la administración del fármaco, por lo que los clínicos siguen utilizando aproximaciones proba-error.
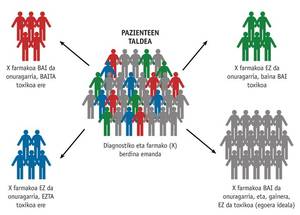
El objetivo principal de la farmacogenética es optimizar el tratamiento individual y lograr una terapia personalizada eficaz y segura, determinando la influencia de la genética de cada persona en la respuesta de los fármacos. Este conocimiento puede cambiar la forma de recetar fármacos en la práctica clínica diaria. La farmacogenética permite realizar una preselección de los pacientes que respondan a un tratamiento y de la dosis más adecuada de los mismos. Es decir, permitirá seleccionar el fármaco adecuado a la dosis adecuada para el paciente al que pertenece (Figura 1). De esta forma se puede evitar el uso innecesario y los efectos secundarios de los medicamentos.
La genética: fuente de la diversidad
Al igual que ocurre con el café, en el caso de los fármacos, clasificamos a los individuos en tres grupos: metabolizadores rápidos, que eliminan sustancias a gran velocidad; metabolizadores comunes, que las expulsan a una velocidad adecuada; y metabolizadores lentos, que eliminan algunas sustancias de forma ineficiente. En este último caso, las sustancias permanecen más tiempo del necesario en el cuerpo. En el caso del café, esto provoca la incapacidad de dormir, mientras que en el caso de los fármacos puede provocar efectos tóxicos. En el ser humano se encargan de metabolizar el café y muchos fármacos. Entre estas enzimas, las familias CYP2 y CYP3 tienen especial importancia a la hora de metabolizar los fármacos. Estas dos familias de enzimas presentan pequeñas variaciones de un individuo a otro. Estas variaciones pueden ser debidas a pequeñas variaciones en la secuencia génica (SNP, polimorfismos mononucleótidos) o a la duplicación o pérdida de genes enteros (CNV, variaciones en el número de copias). Estas variaciones pueden dar lugar a la formación de diferentes proteínas o a la modificación de la cantidad de proteínas. Como consecuencia, la efectividad del metabolismo de los fármacos varía y su efecto dura más o menos tiempo. En otras palabras, las diferencias individuales que se producen en la actividad del citocromo P450 serán las responsables de la eficacia y seguridad de un fármaco. Esto depende en parte de la cantidad de fármaco presente en la sangre. Los Citocromo P450 además del café, metabolizan los fármacos utilizados en cáncer, enfermedades psiquiátricas, etc. Actualmente existen chips comerciales que nos permiten conocer la secuencia CYP de cada individuo y determinar el tipo de metabolizador.
Un chip de ADN se basa en una superficie sólida (vidrio, plástico, silicio) con micropozos. En cada pozo, a través de los dispensores automáticos, se sitúa la conocida secuencia de ADN. En el caso de las investigaciones farmacogenéticas, en estos pozos se establecen secuencias de ADN que pueden tener individuos y que afectan a la respuesta de los fármacos. Para el análisis del ADN de un individuo basta con una muestra de tejido (sangre o saliva). Una vez obtenida la muestra, se rompen las células y se extrae el ADN del núcleo. Posteriormente, este ADN se marca con moléculas fluorescentes y se coloca en pozos. Pero sólo se pegará en pozos con la misma secuencia. Entonces, estos pozos emitirán brillo y, dado que la secuencia correspondiente a cada pozo es conocida, podremos conocer también la secuencia individual.
Variabilidad de la respuesta
Además de estos genes, existen genes relacionados con la velocidad de absorción y eliminación (farmacocinética), así como con la respuesta de un fármaco a las diferentes partes del cuerpo (farmacodinámica). Por ello, las diferentes respuestas a los fármacos pueden ser causadas por cuatro hechos. Por un lado, cambios en las secuencias génicas de los metabolizadores de las enzimas; por otro, cambios en los transportadores y receptores de los fármacos; y por último, cambios en las proteínas que tienen cierta relación con la respuesta del fármaco.
Éxito de la farmacogenética
Un ejemplo del éxito de la terapia personalizada es el tratamiento de Trastuzumab en cáncer de mama. En el 20% de los cánceres de mama que se diagnostican en la actualidad, el gen HER2 ( epidermal growth factor receptor 2) está duplicado. Esto supone que el receptor de los factores de crecimiento que codifica el gen esté superpuesto y aumente el número de receptores. Trastuzumab bloquea a los receptores y han demostrado que sólo prolonga su supervivencia en pacientes con HER2 duplicado.
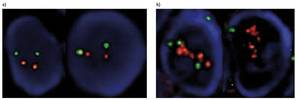
Existen diferentes métodos para detectar pacientes con aumento de proteínas. Una de ellas es la hibridación fluorescente in situ (FISH), en la que el gen se ve marcado fluorescentemente. De esta forma, en lugar de existir dos copias del gen, se pueden detectar casos en los que existen numerosas copias (figura 2). En pacientes que no tienen el gen HER2 duplicado, Trastuzumab no tiene ningún beneficio, pero sí un alto coste.
En cuanto a la seguridad, se sabe que un 15% de los pacientes sufren efectos secundarios derivados del fármaco. En pacientes con cáncer colorrectal, por ejemplo en pacientes con variante de gen UGT1A1, el fármaco Irinoteca se metaboliza mal. Como consecuencia de ello, la administración de dosis normales a estos pacientes conllevará la acumulación de Irinotecan en el cuerpo y la neutropenia (disminución de neutrófilos). Los estudios farmacogenéticos han permitido determinar la dosis adecuada. Un análisis del ADN nos permite conocer en unas pocas horas la variación del gen y determinar la dosis adecuada.
Como se ha visto, la farmacogenética es fundamental para identificar el fármaco eficaz para el paciente y determinar su dosis, evitando así los efectos secundarios. Lo que hace unos años parecía un sueño, hoy en día es una realidad. La Asociación de Alimentos y Medicamentos de Estados Unidos (FDA) ya recomienda la inclusión de información farmacogenética en la etiqueta de los envases de los fármacos. En concreto, en la página web del FDA se incluye un listado de 116 fármacos en los que se indican en sus envases las acciones específicas de información genética a tener en cuenta. (http://www.fda.gov/Drugs/ScienceResearch/ResearchAreas/Pharmacogenetics/ucm083378.htm).
Nuestro equipo de investigación trabaja en la farmacogenética de los cánceres infantiles y en concreto en la leucemia linfoblástica aguda (LLA). En esta enfermedad se trata de localizar indicadores genéticos que influyen en la toxicidad del metotrexato antineoplásico, uno de los fármacos más importantes utilizados en el tratamiento de estos niños. De hecho, este fármaco se utiliza en altas dosis, ya que la mayoría de los niños lo soportan bien y se ha demostrado que esta dura forma de administración aumenta su supervivencia. Sin embargo, a algunos niños estas dosis les producen efectos tóxicos muy graves hasta llegar a ser letales. Por ello, uno de nuestros objetivos es encontrar indicadores genéticos que nos permitan predecir los efectos secundarios.
Bibliografía
Agradecimiento
Los autores del presente trabajo han recibido subvenciones del Gobierno Vasco (IT-199/07, SAIOTEK S-PE10UN14) y de la Universidad del País Vasco (UFI 11/35). Gracias a Maialen Martin Arruti (Anatomía Patológica, Hospital Universitario Donostia).