Fundamentos xenéticos do adenocarcinoma pulmonar ovino
ABA é un cancro producido por un retrovirus
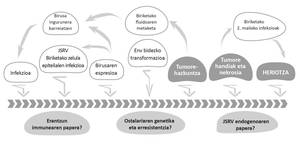
Os retrovirus constitúen una familia numerosa de virus RNA variados que infectan a numerosas especies de hóspedes. Entre eles atópase o retrovirus das ovellas Jaagsiekte do xénero Betaretrovirus (Jaagsiekte Sheep Retrovirus; JSRV), axente da ABA. Aínda que afecta especialmente ás ovellas, tamén poden padecer esta enfermidade os caprinos e as especies de ovellas silvestres. A transmisión do JSRV prodúcese principalmente a través do aparello respiratorio en contacto directo con animais contaminados (Figura 1).
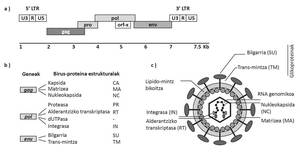
O JSRV é especial entre os virus xa que as súas células diana (neumocitos tipo II e células Klara) son células epiteliales pulmonares. Ademais, tendo en conta que o JSRV ten un xenoma simple que codifica exclusivamente proteínas esenciais, tamén é especial o mecanismo utilizado paira causar cancro. Converte células diana en células cancerosas de proteínas Env da embalaxe do virus (Figura 2). O desenvolvemento da ABAO é lento e só na fase final da enfermidade aparecen síntomas clínicos, entre os que se atopan as dificultades respiratorias dos animais a medida que aumenta o tamaño dos tumores pulmonares e acumúlase o fluído propio da ABAO.
Por que sabemos tan pouco sobre ABA?
En xeral, investigouse pouco a base xenética das enfermidades ovinas en comparación con outras especies de animais domésticos de maior interese económico. Por tanto, a información e os recursos dispoñibles a miúdo son escasos.
Ademais, os investigadores que comezaron a estudar ABA atopáronse cun problema. No xenoma da ovella hai máis de 30 copias moi similares a JSRV, endóxenos JSRV (enJSRV). Estes elementos, como consecuencia dunha antiga colonización do JSRV, convertéronse en parte do xenoma do host. Tanto o JSRV como os enJSRV tiveron que caracterizarse paira poder levar a cabo as investigacións. Aínda que hai moi poucos datos sobre a resposta inmune ao JSRV, hai una cousa clara: Una das características de ABA é a ausencia dunha resposta anticorpo contra o JSRV. Crese que a expresión dalgunhas das enJSRV fixo que as ovellas sexan inmunológicamente toleradas co JSRV.
Control e importancia
As infeccións dos retrovirus son difíciles de controlar. No caso de ABA, a única forma de controlar é a eliminación de animais infectados e enfermos, pero ten outra dificultade. E é que, ao non xerarse un anticorpo contra o JSRV, non se poden utilizar os tests serológicos convencionais paira a súa detección. Só están dispoñibles métodos moleculares mediante PCR (reacción encadeada da polimerasa), pero como o número de virus no sangue adoita ser baixo, non sempre son fiables. En consecuencia, un animal con resultado negativo no test pode introducir un virus no rabaño.
ABA está moi estendida na actualidade: Australia, Nova Zelandia e Islandia son os únicos países aparentemente libres da enfermidade. ABA é o proceso de cancro máis frecuente nas ovellas e as posibles perdas poden ser significativas (Figura 3). Afecta sobre todo ás ovellas adultas novas, o que ocasiona perdas económicas pola diminución da produción e a morte prematura dos animais. Ademais, é una preocupación en relación ao benestar animal, xa que non se pode evitar a morte dos animais.
No caso do JSRV non se puido desenvolver una vacúa ou tratamento eficaz, xa que non se coñece que xenes ou procesos inmunológicos poden estar relacionados coa resistencia. Tanto nestes casos como nos casos nos que os patógenos desenvolven a súa resistencia ás vacinas, aínda que existe outra estratexia que pode ser utilizada, a selección de animais con resistencia propia, que tamén require a identificación de marcadores xenéticos necesarios paira a selección de individuos resistentes.
A investigación de ABA non só pode ser beneficiosa paira as ovellas, senón tamén paira os seres humanos. De feito, os aparellos respiratorios de ambas as especies son moi similares, polo que a ovella pode servir de exemplo paira a investigación de moitas enfermidades humanas. ABA parécese claramente a un cancro humano concreto, o carcinoma broncoalveolar. Como a incidencia deste último vai en aumento, é necesaria a presenza de marcadores xenéticos que permitan identificar quen pode estar en risco de desenvolver cancro. Por tanto, a investigación do ABA pode axudar tamén a coñecer mellor a carcinogénesis pulmonar humana.
Procura de xenes de resistencia ou sensibilidade
A interacción entre os hostaleiros e os virus é complexa e, a miúdo, non se coñecen do todo os detalles desa interacción. Os hostaleiros desenvolveron mecanismos paira protexerse dos ataques de virus e outros patógenos, como a inmunidade intrínseca e adaptativa. Nalgunhas poboacións humanas e animais demostrouse que existe una variable xenética que determina a sensibilidade/resistencia a certas enfermidades, a miúdo influenciada polos polimorfismos dos xenes de resposta inmune.
A pesar das escasas investigacións levadas a cabo ao redor da ABAO, a variable xenética do hóspede parece influír no desenvolvemento da infección e a enfermidade. Nalgunhas razas ou familias de ovino observouse a prevalencia de JSRV e os diferentes niveis de mortalidade por ABA. Paira comprender mellor a patogénesis da ABAO é necesario aclarar cal é a base xenética que pode dar resistencia á infección e ao desenvolvemento do cancro.
As análises asociativas son una forma de identificar os xenes que achegan resistencia/sensibilidade. Neste tipo de análise analízanse os marcadores polimórficos dos xenes seleccionados en función (xenes candidatos) en animais enfermos e de control. A presenza de diferenzas nas frecuencias pode indicar que son xenes que poden dar sensibilidade/resistencia á enfermidade.
Tomando una poboación de ovellas latxas, dos datos obtidos nun estudo realizado por Xenómica e Sanidade Animal do Departamento de Xenética da UPV/EHU, despréndese que a patogénesis da ABAO pode estar influenciada polos xenes implicados en funcións como a inmunidade intrínseca e a inmunidade adaptativa.
A Histocompatibilidad Complexa Principal (DHC) foi estudada en profundidade pola súa gran variabilidade e pola súa función: a codificación de receptores paira a presentación de antígenos a células inmunitarias. Ademais, algúns traballos suxerían que os xenes da DCA influíron no desenvolvemento da ABAO. O noso traballo asociou determinadas variantes de xenes de ovella latxa co desenvolvemento do cancro, incluíndo tres alelos que codifican o punto de unión do antígeno do xene DRB1. Os polimorfismos deste lugar poden afectar á unión e presentación de antígenos.

Ademais, describiuse por primeira vez a asociación paira ambas as candidaturas génicas. Por unha banda, relacionamos as variacións do xene MX1 (Myxovirus Resistance-1) coa sensibilidade. A función deste xene é limitar o ciclo dos virus, aínda que no caso da ovella e o JSRV non sabemos exactamente que pasos limita. Como se viu noutras especies, os polimorfismos deste xene poden afectar á eficacia da proteína MX, podendo ter un efecto similar nas ovellas. Doutra banda, asociamos a resistencia CCR5 (C-C chemokine receptor type 5). O CCR5 ocúpase do quimiotaxi ou movemento das células de resposta inmune, polo que é importante na loita contra as enfermidades infecciosas. Sábese que os polimorfismos afectan á expresión do xene. Ademais, o CCR5 asociouse a outras enfermidades retrovirales, incluída Visna/Maedi, outra enfermidade pulmonar contaxiosa das ovellas.
Así, estes resultados obtidos na análise asociativa, aínda que deberán ser replicados noutras mostras ou razas ovinas, poden servir de base en futuros deseños de vacinas ou terapias ou en programas de selección de animais resistentes.
Bibliografía
Agradecemento
Quero agradecer ás institucións que financiaron este traballo, á directora Begoña Mollo, aos compañeiros do laboratorio (Koldo Garcia, Maialen Sistiaga e Aitor Esparza) e Imanol Salegi.