Ardien biriketako adenokartzinomaren oinarri genetikoa
ABA erretrobirus batek eragindako minbizia da
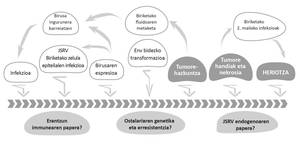
Erretrobirusek askotariko RNA birusen familia ugaria osatzen dute, zeinek ostalari-espezie anitz infektatzen baitituzte. Horien artean, Betaretrovirus generoko Jaagsiekte ardien erretrobirusa (Jaagsiekte Sheep Retrovirus; JSRV) dago, hain zuzen, ABAren eragilea. Bereziki ardiei eragiten dien arren, ahuntzek eta ardi-espezie basatiek ere izan dezakete gaixotasun hori. JSRVaren transmisioa arnas aparatuaren bidez gertatzen da batez ere, kutsatutako animaliekin kontaktu zuzena izanez gero (1. irudia).
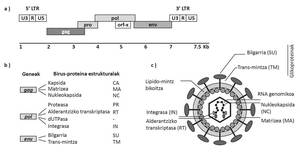
JSRVa berezia da birusen artean, biriketako zelula epitelialak baitira bere itu-zelulak (II motako pneumozitoak eta Klara zelulak). Horrez gain, kontuan izanda JSRVak soilik proteina esentzialak kodetzen dituen genoma sinplea daukala, berezia da, halaber, minbizia eragiteko erabiltzen duen mekanismoa. Birusaren bilgarriaren Env proteinak bihurtzen ditu itu-zelulak minbizi-zelula (2. irudia). ABAren garapena geldoa da, eta gaixotasunaren azken fasean soilik agertzen dira sintoma klinikoak; besteak beste, biriketako tumoreen tamaina handitu eta ABAren berezkoa den fluidoa metatu ahala, animaliek arnasa hartzeko izaten dituzten zailtasunak.
Zergatik dakigu hain gutxi ABAri buruz?
Oro har, gutxi ikertu izan da ardien gaixotasunen oinarri genetikoa, interes ekonomiko handiagoa duten beste etxe-abere espezie batzuekin alderatuta. Hortaz, eskuragarri dagoen informazioa eta baliabideak urriak izan ohi dira sarritan.
Horrez gain, ABA aztertzen hasi ziren ikerlariek arazo batekin egin zuten topo. JSRVaren oso antzeko 30 kopia baino gehiago daude ardiaren genoman, JSRV endogenoak (enJSRVak). Elementu horiek, JSRVaren antzinako kolonizazio baten ondorioz, ostalariaren genomaren parte bihurtu ziren. JSRVa zein enJSRVak, biak, karakterizatu behar izan ziren ikerketak egin ahal izateko. JSRVaren aurkako erantzun immunearen inguruko datu oso gutxi dauden arren, gauza bat argi dago: ABAren ezaugarrietako bat da JSRVaren aurkako antigorputz-erantzun bat falta dela. Uste da enJSRVetako batzuen espresioak JSRVarekiko immunologikoki jasanbera bihurtu dituela ardiak.
Kontrola eta garrantzia
Erretrobirusen infekzioak zailak dira kontrolatzen. ABAren kasuan, animalia infektatuak eta gaixoak kentzea da kontrolatzeko modu bakarra, baina badu beste zailtasun bat. Izan ere, JSRVaren aurkako antigorputzik sortzen ez denez, ezin dira erabili ohiko test serologikoak hura detektatzeko. Soilik PCR (polimerasaren erreakzio kateatua) bidezko metodo molekularrak daude eskuragarri, baina, odolean birus-kopurua baxua izan ohi denez, ez dira beti fidagarriak izaten. Ondorioz, testean emaitza negatiboa eman duen animalia batek birusa sar dezake artaldera.
ABA oso hedatuta dago gaur egun: Australia, Zeelanda Berria eta Islandia dira, ustez, gaixotasunetik libre dauden herrialde bakarrak. ABA da minbizi-prozesu ohikoena ardietan, eta eragin ditzakeen galerak nabarmenak izan daitezke (3. irudia). Ardi heldu gazteei erasaten die, batik bat, eta horrek galera ekonomikoak eragiten ditu, ekoizpena murriztu eta animaliak behar baino lehen hiltzen direlako. Gainera, animalien ongizateari dagokionez ere ardura bat da, animalien heriotza ezin delako ekidin.
JSRVaren kasuan, ezin izan da txerto edo tratamendu eraginkorrik garatu, ez baita ezagutzen zer gene edo prozesu immunologiko egon daitezkeen erlazionatuta erresistentziarekin. Horrelako kasuetan nahiz patogenoek txertoekiko erresistentzia garatzen dutenean, erabil daitekeen beste estrategia bat baden arren, hots, berezko erresistentzia duten animaliak hautatzea, estrategia horrek ere indibiduo erresistenteak aukeratzeko behar diren markatzaile genetikoak identifikatzea eskatzen du.
ABAren ikerketa ardientzat ez ezik gizakientzat ere onuragarria izan daiteke. Izan ere, bi espezieen arnas aparatuak oso antzekoak dira, eta, hortaz, ardia eredutzat erabil daiteke giza eritasun asko ikertzeko. ABAk giza minbizi jakin baten antz nabarmena du, kartzinoma bronkoalbeolarrarena hain zuzen. Azken horren intzidentzia handituz doanez, markatzaile genetikoen premia dago, minbizia garatzeko arriskuan nor egon daitekeen identifikatu ahal izateko. Beraz, ABA ikertzea lagungarria izan daiteke gizakien biriketako kartzinogenesia hobeto ezagutzeko ere.
Erresistentzia- edo sentikortasun-geneen bilaketa
Ostalarien eta birusen arteko elkarrekintza konplexua da, eta, sarritan, ez dira elkarrekintza horren xehetasunak guztiz ezagutzen. Ostalariek zenbait mekanismo garatu dituzte birusen eta beste patogeno batzuen erasoetatik babesteko, berezko immunitatea eta immunitate adaptatiboa kasu. Zenbait giza eta animalia-populaziotan, frogatu da gaixotasun batzuekiko sentikortasuna/erresistentzia zehazten duen aldagai genetikoa dagoela, sarritan, erantzun immuneko geneetako polimorfismoek eragina.
ABAren inguruan ikerketa oso gutxi egin diren arren, badirudi ostalariaren aldagai genetikoak eragina izan dezakeela infekzioaren eta gaixotasunaren garapenari dagokionez. Zenbait ardi-arraza edo familiatan, JSRVaren prebalentzia eta ABAk eragindako hilkortasun-maila desberdinak behatu dira. ABAren patogenesia hobeto ulertzeko, beharrezkoa da infekzioari eta minbiziaren garapenari erresistentzia eman diezaiokeen oinarri genetikoa zein den argitzea.
Erresistentzia/sentikortasuna ematen duten geneak identifikatzeko modu bat dira asoziazio-analisiak. Analisi-mota horretan, funtzioan oinarrituz hautatutako geneetako (gene hautagaiak) markatzaile polimorfikoak aztertzen dira animali gaixoetan eta kontrolekoetan. Maiztasunetan aldeak egoteak adieraz dezake gaixotasunari sentikortasuna/erresistentzia eman diezaioketen geneak direla.
Ardi latxen populazio bat hartuta, EHUko Genetika Saileko Animalien Osasuna eta Genomikak egindako ikerketa batean lortutako datuetatik ondoriozta daitekeenez, hainbat funtziotan, hala nola berezko immunitatean eta immunitate adaptatiboan, parte hartzen duten geneek eragina izan dezakete ABAren patogenesian.
Histobateragarritasun Konplexu Nagusia (HKN) sakon aztertu izan da, bere aldakortasun handiagatik, eta duen funtzioagatik: antigenoak inmunitate-zelulei aurkezteko, hartzaileak kodetzea. Gainera, HKNko geneek ABAren garapenean eragina dutela iradokitzen zuten zenbait lanek. Gure lanak ardi latxen HKNko geneetako aldaki jakinak asoziatu ditu minbiziaren garapenarekin, DRB1 geneko antigenoaren lotura-gunea kodetzen duten hiru alelo barne. Leku horretako polimorfismoek antigeno-loturari eta aurkezpenari eragin diezaiokete.
Horrez gain, lehen aldiz deskribatu dugu bi gene-hautagaientzako asoziazioa. Batetik, MX1 (Myxovirus Resistance-1) geneko aldakiak sentikortasunarekin erlazionatu ditugu. Gene horren eginkizuna birusen zikloa mugatzea da, ardiaren eta JSRVaren kasuan zehazki zer pauso mugatzen duen ez dakigun arren. Beste espezie batzuetan ikusi denez, gene honetako polimorfismoek MX proteinaren eraginkortasunari eragin diezaiokete, eta baliteke ardietan ere antzeko efektu bat izatea. Bestetik, CCR5 (C-C chemokine receptor type 5) erresistentziarekin asoziatu dugu. CCR5a erantzun immuneko zelulen kimiotaxiaz edo mugimenduaz arduratzen da, eta, beraz, garrantzia du gaixotasun infekziosoen aurkako borrokan. Jakina da polimorfismoek genearen espresioari eragiten diotela. Gainera, CCR5 beste gaixotasun erretrobiral batzuekin lotu izan da, ardien biriketako beste gaixotasun kutsakor batekin, Visna/Maedi, barne.
Hala, bada, asoziazio-analisian lortutako emaitza horiek, beste lagin edo ardi-arrazaren batean erreplikatu beharko diren arren, oinarritzat erabil daitezke etorkizunean txertoen edo terapien diseinuan nahiz animalia erresistenteen hautaketa-programetan.
Bibliografia
Eskertza
Eskerrak eman nahi dizkiet lan hau finantzatu duten erakundeei, Begoña Jugo zuzendariari, laborategiko lankideei (Koldo Garcia, Maialen Sistiaga eta Aitor Esparza) eta Imanol Salegiri.
Idatzi zuk zeuk Gai librean atalean
Gai librean aritzeko, bidali zure artikulua aldizkaria@elhuyar.eus helbidera
Hauek dira Gai librean atalean Idazteko arauak