Cannabis: el secreto de maria
Las primeras noticias sobre las propiedades curativas del cannabis se extendieron antiguamente. a.C. En el año 2737, el emperador Sheng Nung en China señaló en su libro Pen Tsao que el cannabis es bueno para prevenir o curar el dolor, la gota, la malaria y ciertas enfermedades (Figura 1). En 1890 Sir Russel Reynolss, médico de la reina Victoria de Inglaterra, ordenó un cannabis para aliviar los dolores de la regla.

Por ello, en el primer número de la revista The Lancet, este mismo médico escribió sobre el cannabis: "... cuando es puro y preocupado, es uno de los medicamentos más apreciados de los que disponemos...". El cáñamo llegó a Europa traído de Egipto por Napoleón y entró en la farmacopea. Sin embargo, años después, tras una serie de estudios sobre los efectos nocivos, se retiró de la farmacopea mundial. Debido a sus efectos psicoactivos, se utilizaba para jugar al deporte, por lo que en 1835 Baudelaire y otros artistas fundaron el club Hashichines.
El cáñamo es una planta anual que, por su dimorfismo sexual, tiene floraciones totalmente diferentes entre el macho y la hembra. El cáñamo se encuentra dentro de la especie Cannabis sativa y hay tres subespecies diferentes: indica, sativa y rudelaris, cada una con sus características (Figura 1). La subespecie sativa se puede encontrar en todo el mundo, pero la mayor concentración de cannabinoideos crece en el trópico.
Indica
La subespecie es una planta arbustiva situada en el Himalaya, más dura por el tiempo que la que nace en el trópico. La estructura formada por las hojas y pistilos de la hembra de cáñamo segrega resina, utilizada para la formación de hachís. La subespecie Rudelaris se encuentra en las repúblicas de la antigua Unión Soviética, pero la concentración de cannabinoides es más baja que en otras subespecies.
Canabinoides: responsables de los efectos

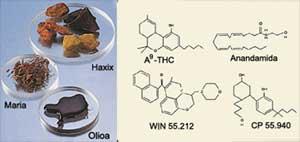
Los cannabinoideos son ácidos carboxílicos derivados de Cannabis sativa y sus productos. La presencia de cannabinoides en la planta está condicionada sobre todo por factores genéticos, pero también por el clima (luz, temperatura), la época de recolección, el sexo y las partes de la planta recolectada. En el cáñamo hay unos sesenta y un cannabinoidos, de los cuales sólo tres son responsables de los efectos psicoactivos. El más importante de los componentes, por sus efectos psicoactivos, es el tetrahidrocannabinol P 9 (Figura 2). El resto de los cannabinoides, como P 8 tetrahidrocanabinol y canabinol, presentan efectos psicoactivos más débiles. Sin embargo, el cannabinoideo produce otro tipo de efectos no psicoactivos.
Las vías de aplicación de los cannabinoides son abundantes y, al ser solubles en lípidos, atraviesan rápidamente las membranas del organismo. Fumar es la vía de consumo más conocida. Entre las diferentes formas que puede adoptar el cáñamo, la más utilizada es la resina propiamente dicha ( hachís ), pero también se utiliza bastante la preparación con hojas y ojos de cáñamo ( maría ) y el aceite de cáñamo (con mayor concentración de THC) (Figura 2).
Parece que la combustión del cáñamo hace que el ácido THC en crudo se convierta en THC libre. Este THC libre se respira junto con el humo y, atravesando las membranas de los alveolos pulmonares, llega a los capilares pulmonares. Desde allí, el THC es transportado rápidamente al corazón y directamente al cerebro; el proceso es tan rápido como la administración intravenosa. El efecto aparece inmediatamente después de quemarse y dura poco. Por otra parte, la vía utilizada para la aplicación del cáñamo es la vía oral, ya que se mantienen los efectos farmacológicos, aunque la absorción es variable.
La ingesta crónica del cáñamo no altera la eliminación de los cannabinoides: se elimina la misma cantidad. Además, debido a las características lipofílicas anteriormente citadas, los cannabinoides tienen capacidad de almacenamiento en depósitos hidrofóbicos como el tejido adiposo. Por tanto, es posible encontrar metabolitos en el análisis de la orina durante varias semanas. Por vía rectal, la absorción es muy buena y la biodisponibilidad obtenida es mayor que la vía oral. Además, de este modo, el fármaco entra directamente en la circulación sanguínea y evita el metabolismo hepático.
¿Son sustancias psicoactivas los cannabinoides?Diversos estudios han demostrado que los efectos del THC son bastante variables dependiendo del fumador y de las características de la droga. Depende de la dosis, de la vía administrativa, de la experiencia del usuario, de la sensibilidad a los efectos psicoactivos y de las situaciones de fumar. La intoxicación del cannabis provoca un grave desequilibrio entre el humor, la comprensión y la motivación. Sin embargo, en la mayoría de los casos el fumador sólo busca un efecto incentivador. Parece que el cangrejo separa estos efectos estimulantes de los provocados por opiáceos y estimulantes.
El fumador habitual percibe un efecto incentivador durante dos horas, aunque hay que tener en cuenta que la eficacia del cáñamo depende de la dosis. Diversos estudios han demostrado que, mientras la droga está sometida a efectos agudos, al usuario se le deteriora bastante la cognición, la percepción, el tiempo de reacción, la capacidad de aprendizaje y la memoria. Además, la falta de coordinación de los movimientos corporales continúa durante varias horas después de que el efecto incentivador haya desaparecido. Esta perturbación se debe a la imposibilidad de conducir vehículos y de trabajar.
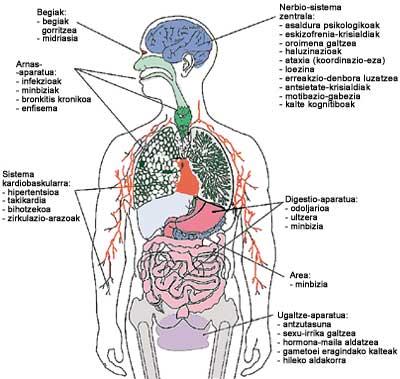
El consumo crónico de cannabis modifica totalmente el comportamiento del drogadicto y en direcciones complejas como el apetito (figura 3). A pesar de que algunos fumadores han reivindicado que consiguen relaciones sexuales de mayor satisfacción, no se ha confirmado científicamente. Sin embargo, ha quedado demostrado que tras la quema del cannabis aparecen efectos como alucinaciones, crisis de pánico y psicosis.
Según las encuestas realizadas a los usuarios, entre un 50-60% de los fumadores de cáñamo han sufrido más de una vez una crisis de ansiedad. Estas reacciones se suelen observar con las dosis más altas de vía oral, ya que fumar permite dominar la dosis según la percepción de los efectos. Por otra parte, no se ha confirmado la relación entre el cannabis y el riesgo de la esquizofrenia, sino que algunas publicaciones clínicas han puesto de manifiesto que a pacientes con antecedentes de esquizofrenia, si se quema el cáñamo, la psicosis puede reaparecer más rápidamente.
Uno de los efectos más controvertidos que los cannabinoideos parecen producir cronicamente es el síndrome de la falta de motivación. Cabe destacar que este síndrome no aparece así en las guías diagnósticas, pero el término indica bien la situación de quienes abandonan las actividades sociales y no muestran interés en la escuela. Aunque no se demuestre por sí misma una relación de causalidad con el consumo, el cannabis suele ser considerado como el origen de este síndrome, especialmente si su uso es duro. Tampoco se ha podido asegurar que el cáñamo dañe las neuronas o produzca cambios funcionales definitivos. De hecho, los estudios realizados en ensayos clínicos con animales de laboratorio y humanos han demostrado que el abandono de los cannabinoides supone una recuperación progresiva del daño del proceso de aprendizaje en unas semanas.
En general, la dependencia comprende tres hechos: tolerancia, dependencia física y dependencia psíquica.
Tolerancia.
La tolerancia consiste en la desaparición de los efectos que un determinado fármaco puede causar por su administración repetida. En animales de laboratorio se ha demostrado que la administración crónica de ciertos agonistas canabinoides produce tolerancia a la analgesia, a la inhibición de la actividad motora, a la hipotermia, etc. En humanos, los estudios clínicos también han confirmado la tolerancia a los efectos farmacológicos del THC. Además, el desarrollo de la tolerancia está relacionado con la dosis de THC ingerido, por lo que a medida que aumenta el consumo de THC aumenta la tolerancia.
No obstante, cabe destacar que las dosis empleadas para inducir la tolerancia en los animales de laboratorio son muy superiores a las utilizadas normalmente por el hombre. De hecho, la dosis de tolerancia en los animales debe ser de 20-50 mg/kg por día y, sabiendo que un cigarrillo de marihuana tiene entre 30-60 µg de cannabinoideo, un ser humano debería quemar entre 300 y 1.500 cigarros por día para poder llevar a cabo este fenómeno. Cabe destacar, por otra parte, que el desarrollo de la tolerancia a los cannabinoideos puede ser responsable tanto del sistema interior cannabinoide como del opioideo.
Dependencia física.
La dependencia física se debe a que el organismo se acostumbra a funcionar bajo los efectos de la droga. Según diversos estudios, tras 6 días de administración de THC (20 mg/kg) a los animales de laboratorio, una vez cesada la aplicación de este canabinoideo, se observa un síndrome de abstinencia lento y los signos clínicos más representativos sólo aparecen tras la administración del antagonista canabinoideo. Parece que este suceso está relacionado con el largo ciclo de vida (tiempo necesario para alcanzar la mitad de la concentración) de la eliminación del THC. De hecho, al ser el agonista cannabinoideo WIN 55212 menos intenso, al dejar de tomarlo se produce un síndrome de abstinencia más evidente.
En los animales, la mayoría de los signos clínicos que reflejan el síndrome de abstinencia de los cannabinoides están relacionados con la alteración del control del movimiento. Entre otras cosas, se producen ataxias, sacudidas del tronco, temblor de las piernas, posturas anormales y disminución de la actividad motriz. Cabe destacar que los signos clínicos vegetativos (hipotermia y pérdida de peso, por ejemplo) que aparecen en el síndrome de abstinencia de los opiáceos no se ven en el caso de los cannabinoides.
En los seres humanos, al igual que en los animales de laboratorio, se observa un síndrome de abstinencia lento tras 3 semanas de tratamiento del THC. Los signos clínicos que aparecen en este caso son la ansiedad, la anorexia, el insomnio y la irritabilidad y las señales más evidentes aparecen en los primeros días.
Dependencia psíquica.
La dependencia psíquica de los cannabinoides es el principal componente de la dependencia, ya que, al igual que ocurre con el alcohol, la heroína y el resto de drogas, indica la dificultad de abandonar libremente la droga. La necesidad urgente de la persona drogadicta para conseguir y quemar el cannabis se basa en una raíz neurobiológica concreta, el sistema dopaminérgico del SNC. Sin embargo, ha sido un trabajo laborioso relacionar la influencia de los cannabinoides con la dopamina neurotransmisora, especialmente con los casos de cocaína, nicotina y opiáceos. Hasta el conocimiento de las características farmacocinéticas del receptor CB1 y de los cannabinoides, en la última década no se desarrolló toda la teoría neurobiológica.
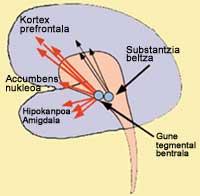
En la actualidad tenemos bastante claro que, tomando como modelo las investigaciones conductuales y neurofisiológicas, los cannabinoides activan la vía mesolínica (Figura 4). Este sistema mesolínico se denomina red de recompensas, ya que funciona como un estímulo potenciador que mantiene las acciones de supervivencia, como la alimentación y el sexo. Cabe destacar que en las zonas de esta red participan no sólo la dopamina, sino también el glutamato, el GABA y los neurotransmisores peptídicos. Estos tienen gran importancia para conseguir nuevos remedios.
De todos los efectos que puede producir el cannabis, los más útiles y estudiados actualmente son dos: el efecto antiemético y el aumento del apetito en pacientes con sida o cáncer. De hecho, el derivado sintético del THC disminuye el vómito atribuido a la quimioterapia. Esta sustancia no está disponible en España, pero sí en Estados Unidos, Canadá y Gran Bretaña.
En la última década las investigaciones sobre el cannabis han aumentado considerablemente y se han propuesto numerosos usos terapéuticos. Entre ellas destacan la analgesia, el tratamiento de un cáncer específico de SNC, la prevención de alteraciones del movimiento en enfermedades degenerativas, la disminución de la presión intraocular y los efectos anticonvulsivos.
Analgesia.
Numerosas publicaciones científicas han demostrado que los agonistas canabinoides tienen un efecto analgésico. Esta influencia se debe principalmente a los receptores cannabinoides situados en la médula espinal y en las zonas supraespinales. Parece que lo más importante pendiente de investigación es la combinación de los efectos analgésicos de los cannabinoides y opioides. De hecho, el mecanismo de acción de la analgesia por opiáceos difiere del utilizado por los cannabinoides, por lo que la administración de ambos en pequeñas dosis reduciría los efectos no deseados y aumentaría los efectos beneficiosos (analgesia).

Tumores del sistema nervioso central.
En los últimos años, investigadores de la Universidad Complutense de Madrid han demostrado que el cannabinoide THC en ratas reduce el tamaño del tumor cerebral glioma. De hecho, este canabinoideo evita la duplicación celular por la apoptosis (muerte programada) causada por una sustancia llamada cerámica. Además, el THC parece inhibir la angiogénesis, el desarrollo de vasos sanguíneos necesarios para alimentar y desarrollar el tumor.
Enfermedades degenerativas.
El sistema endocanabinoideo participa en el control del movimiento. De hecho, en el cuerpo estriado, en la zona del SNC relacionada con el control del movimiento, hay muchos receptores CB1. Investigadores como el THC han demostrado que la activación del receptor CB1 supone una inhibición del movimiento. En este sentido, el conocimiento de que el control del movimiento se realiza a través de los receptores CB1 ha abierto muchas vías de investigación, sobre todo en la búsqueda de nuevos remedios en diversas enfermedades relacionadas con el sistema motor, como la enfermedad de Parkinson, corea de Huntington y esclerosis múltiple.
Así, investigadores han demostrado que en los seres humanos afectados por la enfermedad de Parkinson el número de receptores de CB1 es mayor. Por tanto, los antagonistas del receptor CB1 serían el tema de investigación para esta enfermedad. Sin embargo, en la corea de Huntington parece que ocurre lo contrario, es decir, en los ganglios basales el número de receptores canabinoides es menor de lo normal, por lo que en este caso los agonistas del receptor CB1 serían los más útiles terapéuticamente. También se ha demostrado que en personas con enfermedad de Alzheimer este receptor cannabinoideo es menor. Además, los cannabinoides tienen la capacidad de amortiguar las contracciones musculares dolorosas que se producen en la esclerosis múltiple. Este hecho sólo se ha demostrado en animales de laboratorio, pero los pacientes con esclerosis múltiple han confirmado este efecto beneficioso.
Presión intraocular.
Los canabinoideos sintéticos parecen tener la capacidad de bajar la presión intraocular. Sin embargo, los fármacos canabinoideos sintéticos que se han probado hasta el momento producen demasiados efectos no deseados respecto a los beneficiosos.Epilepsia.
Según estudios realizados con animales de laboratorio y seres humanos, tanto el THC como el cannabis ejercen una acción antiepiléptica sobre personas con crisis de grand mal. Además, sabiendo que el cambio no tiene efectos psicoactivos, sería interesante realizar más investigaciones en este campo en el futuro.
Sistema cannabinoide
Durante las décadas de los 80 y 90, cuando se reanudaron las investigaciones sobre el cáñamo, se analizaron la extracción, síntesis, metabolismo, farmacología y psicología de los cannabinoides y se identificaron los receptores cannabinoides. Existen dos tipos de receptores cannabinoides: CB1 en el sistema nervioso central (SNC) y CB2 en los tejidos periféricos.
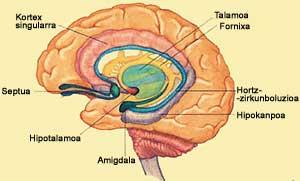
Los receptores CB están asociados a proteínas G y la excitación de la proteína Gi/o adaptada a receptores CB puede modular tres sistemas efectivos: Sistema MAP kinasa (se activa), sistema adenilil ciclasa (se inhibe) y canales de iones (se modifica la membrana potencial) (figura inferior). La distribución de los receptores CB1 es muy amplia en el cerebro y parece estar relacionada con los efectos farmacológicos que aparecen en el SNC tras la aplicación de los cannabinoides. El mayor número de receptores se encuentra en los ganglios basales, donde se pretende controlar los movimientos forzosos. En el hipocampo el número de CB1 también es elevado, lo que pone de manifiesto la influencia de los cannabinoides en la memoria y en los procesos de aprendizaje. Sin embargo, los receptores CB2 se encuentran en el sistema inmunitario, el hígado, los pulmones y los riñones.
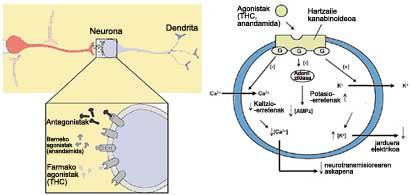
En la última década se han encontrado agonistas internos que se asocian con receptores cannabinoides. La más importante es la llamada anandamida. Estas moléculas, que parecen provenir del ácido araquidónico, tienen la capacidad de unirse a los receptores CB1 y CB2. Su importancia funcional está por desvelar, ya que se dan en los seres vivos y desaparecen rápidamente. Parece que pueden permitir la liberación de neurotransmisores y, en consecuencia, modificar la temperatura, la percepción (colores, oído, vista, etc.), la cognición (sueño, memoria, etc.) y el control del movimiento (coordinación, tono muscular). Hoy en día, una vez encontrados los agonistas internos, sería interesante saber cuál es la función que desempeña el sistema cannabinoide, ya que el conocimiento de la regulación tendría una importancia para la curación de ciertas enfermedades. Por ello, los investigadores buscan nuevas moléculas a partir de las estructuras de los agonistas internos.
Para dar a conocer todo el sistema canabinoideo es necesario explicar los canabinoideos sintéticos. De hecho, los canabinoideos sintéticos son más poderosos que el THC y gracias a ellos, las investigaciones sobre el sistema canabinoideo han recibido un gran impulso. Se han clasificado los receptores CB en función de su afinidad respecto a ciertos canabinoideos sintéticos. Así, entre los más utilizados actualmente en investigación se encuentran los agonistas CB1 CP55940 y WIN55212, y el antagonista CB1 SR14176A. Además, quedan por descubrir nuevas moléculas con mayor afinidad por los receptores CB.
BIBLIOGRAFÍA
Hardman, J.G. y Limbird, L.E.
Goodman Gilman’s
The Pharmacological Basis
Therapeutics.
Ed.
2001 McGraw-Hill,
Londres.
Howowlett, A. C.; Barth, F.; Bonner, T.I. ; Cabral, G.; Casellas, P.; Devane, W.A. ; Felder, C.C. ; Herkenham, M.; Mackie, K.; Martín, B.R. ; Mechoulam, R. y Pertwee, R.G.
International Union of Pharmacology. XXVII. Classification of Cannabinoid Receptors.
2002 Pharmacol Rev; 54 (2): 161-202.
Maldonado, R. y Rodríguez de Fonseca, F.
Cannabinoid addiction; behavioral models and neuronal correlates.
2002 J Neuroscience; 22 (9): 3326-3331.
Pertwee, r.
Cannabinoid Receptors. Ed.
1995 Academic press, London.





