Influència de la pluja àcida en els monuments petris

El fenomen de la pluja àcida i les seves conseqüències són cada vegada més importants en els últims anys. A mesura que augmenta el nivell de contaminació, aquest complex problema té conseqüències incontrolables o incontrolables per al nostre món, encara que moltes vegades reversibles. No hi ha solució senzilla, però és necessari i urgent actuar abans que sigui massa tarda o, desgraciadament, encara que sigui tard.
En moltes ocasions s'ha parlat i escrit sobre l'impacte de la pluja àcida en la naturalesa (boscos, ...). En aquesta ocasió parlarem d'una curiosa influència: el que es fa als monuments de pedra, citant alguns exemples il·lustratius. Però primer veurem en què consisteix la pluja àcida.
Què és la pluja àcida?
A causa del CO? present en l'atmosfera, la pluja és en si mateixa lleugerament àcida. Les fonts de CO? o diòxid de carboni són naturals i antropogèniques (degradació de la matèria orgànica, combustió, ...). Quan es dissol en l'aigua es produeix la següent reacció:
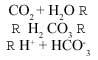
A causa de l'àcid carbònic produït, el pH de la pluja natural és aproximadament de 5,6 (pH = - log [H+]).
D'altra banda, en les zones industrials i urbanes es generen altres gasos àcids, els més importants són els òxids de sofre i nitrogen, sent els majors contaminants el SO2 (diòxid de sofre) i els NOx (òxids de nitrogen (IV) i (II)). La font natural de SO2 és l'oxidació del SH2 (font biogènica) i la font antropogènica és, sobretot, la combustió, sent la importància de totes dues fonts similars. Quant als òxids de NOx, si bé contenen una font natural, la més important és l'antropogènica (especialment la combustió).
El diòxid de sofre (SO2) pot oxirse a l'òxid de sofre (VI) (SO3), reacció que es produeix gràcies a l'oxigen i ozó presents en l'aire i catalitzat per certes substàncies metàl·liques presents en les partícules contaminants de l'aire. En dissoldre's el triòxid de sofre (o òxid de sofre) en l'aigua, pot transformar-se en àcid sulfúric per la reacció:
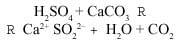
El pH de la pluja depèn de la concentració de SO3 (inversament proporcional), i es produeix principalment en zones urbanes d'alt trànsit i en zones industrials, com s'ha esmentat anteriorment. El pH de l'aire canvia quan plou. Inicialment la concentració de SO3 és màxima (pH més baix). S'ha pogut mesurar el valor de pH=3, la qual cosa suposa un increment del 100% de la concentració de protons respecte a la pluja normal.
Es poden escriure reaccions similars per als òxids de nitrogen, però com s'explicarà més endavant, el major impacte sobre els monuments de pedra és l'H2SO4.
Per a finalitzar aquesta entrada es pot dir que el problema de la deposició àcida no sols apareix en pluja. En l'actualitat es distingeixen dues parts: d'una banda, la deposició seca, és a dir, partícules i gasos (aerosols, metalls, SO4, SO2, ...) i d'altra banda, la deposició humida, en la qual a més de la pluja es poden introduir neu, rosada, boira i calamarsa. La influència d'aquests últims no és lenta, ja que en els núvols s'ha pogut mesurar pH = 1.
Amb quins materials s'han construït els monuments?

Les roques més comunament utilitzades són marbre, calcària, arenisca i granit.
El marbre és una pedra calcària formada per cristal·lins de calcita, forma mineral termodinámicamente estable. El marbre és una pedra metamòrfica que, a altes temperatures i pressions, sofreix un procés de recristalización convertint-se en una roca sedimentària (anomenada calcària). Químicament, el marbre i la calcària són iguals, però morfològicament es diferencien en la mesura i porositat dels cristalls. Els cristalitos de la calcària són més petits, per la qual cosa el marbre és més porós.
La pedra arenisca s'utilitza més per a la construcció d'edificis que en monuments. Aquesta pedra és una pedra sedimentària formada per sorres. La sedimentació d'aquests grans de sorra es pot produir en roca de quars o calcària.
El granit està compost principalment per tres minerals: quars, mica i feldespat. Els grans de granit són generalment bastant grans i la seva porositat és molt petita, per la qual cosa aquest material s'utilitza amb freqüència per a protegir les parts baixes dels edificis de la humitat.
Influència de la pluja àcida en les pedres
Els monuments més vulnerables per la pluja àcida són els de pedra calcària: marbre, calcària i arenisca calcària. La pluja àcida no afecta a areniscas pures ni granits.
La reacció entre una pedra calcària i la pluja àcida es pot expressar de forma simplificada com:
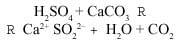
Els mecanismes que controlen la dissolució de la calcita depenen de certes condicions: pH, flux hidrodinàmic, etc. El rang més interessant de pH en aquest tema és 4-6, controlat per transport i cinètica superficial.
Cal destacar que el mal causat per la dissolució química del carbonat càlcic és sobretot un fenomen superficial. Per això, els relleus treballats sobre les superfícies poden quedar fortament deteriorats per la dissolució superficial, no afectant l'estructura inferior del marbre.
El problema de la deterioració dels monuments no resideix únicament en la dissolució de la calcita. En l'equació anterior s'observa que el carbonat càlcic en les pedres reacciona amb l'aparició del sulfat càlcic. El compost cristalizable en forma de dihidrat de sal és: CaSO4. 2 H?O (guix). El guix és bastant soluble en aigua. Per tant, només s'acumula en superfícies que no tenen flux d'aigua directe i han reaccionat.
Per això, els edificis de pedra calcària i els estats de marbre presenten una capa de guix en zones protegides de la pluja. A causa de l'aire contaminat (pols, partícules de carbó, ...) aquesta capa de guix s'ennegreix. Després d'anys en aquesta zona, les pedres calcàries presenten un marcat aspecte blanc-negre, blanc en zones on la pluja neta regularment el guix i negre en zones on la pluja no pot netejar-lo, on la capa fosca de guix ha pegat una deposició seca.
Com s'ha esmentat anteriorment, la pluja àcida no reacciona sobre superfícies arenoses i granítiques. No obstant això, la deposició seca es pega creant un color negre uniforme.

Les sals solubles de sulfat i nitrat (generades en la reacció entre la pluja àcida i les pedres calcàries) es dissolen en la mateixa aigua de pluja. Aquesta solució és absorbida per la pedra mitjançant un mecanisme capil·lar. Quan la pedra s'asseca aquestes sals es cristal·litzen en aquest sistema porós. La pressió generada en aquest procés és suficient per a trencar mecànicament la matriu de la pedra. Per tant, la porositat d'una pedra controla la quantitat de solució que es pot interioritzar i, en definitiva, el temps de durada d'aquesta. El mal causat per aquesta acció mecànica pot ser més seriós que la simple solució química de la pedra.
Alguns exemples
L'Ajuntament de Schenectady (N.I.), edifici històric, va ser construït en 1930 amb el millor marbre de Vermont (equivalent al marbre de Carrara a Itàlia). Ha caigut gairebé per la pluja àcida. L'estructura de l'edifici s'ha afeblit a causa de la guix del marbre.
A Pequín (la Xina) hi ha monuments de marbre de 500 anys que conten la història de l'imperi. Fins fa 40 anys es podien llegir les inscripcions i avui no es poden llegir. Això significa que el mal s'ha produït sobretot en els últims anys.
En les columnes de marbre dels emperadors romans Marcus Aurelius i Traianus es pot observar un fenomen curiós, com s'ha esmentat anteriorment. Els baix relleus tractats en les columnes representen les conquestes d'aquests emperadors. En alguns llocs, aquestes columnes suporten directament sobre elles el flux d'aigua de pluja i el mal descrit varia enormement en funció dels factors que controlen la solució química del marbre. En altres llocs, a causa de la protecció dels edificis circumdants, la superfície roman en bon estat, encara que la columna ha estat construïda amb 1800 anys d'antelació.
Conclusions
La deterioració de les pedres calcàries es produeix principalment mitjançant dos mecanismes.
- Solució química de calcita
- El mal mecànic causat per la recristalización de les sals solubles generades en dissolució en els porus de la pedra.
El primer mecanisme és important quan es tracta de preservar detalls superficials en escultures. El segon mecanisme, no obstant això, pot tenir una gran influència en la deterioració estructural de la pedra. És difícil distingir la influència de cada mecanisme en la deterioració d'un estat o monument.





