Cuando la historia de la casa manda
En la mayoría de los cánceres de origen genético, los genes mutados son genes reparadores. Su función es corregir los defectos del ADN, "por lo que si el reparador está mutado, no puede cumplir su función y entonces aparece el tumor". La explicación es de Karmele Mujika, médico del Departamento de Genética de Onkologikoa. En su sección atienden casos de este tipo y comenta los cánceres más comunes: "son de pecho y ovarios por un lado y de colon por otro".
"Llegan a la consulta personas que tienen muchos de estos cánceres dentro de su familia. Primero hacemos historia: preguntamos cuántos casos hay en la familia, hacemos un árbol genealógico y con ello valoramos el riesgo que tienen las personas de esta familia para tener cáncer", ha explicado Mujika.
A los que tienen un alto riesgo, les ofrecen un estudio genético en sangre con el fin de determinar si tienen alguna variante genética relacionada con el cáncer: "En el cáncer de mama observamos el ADN de los linfocitos de la sangre. Para empezar, hacemos un DGGE ( denaturing gradient gel electrophoresis )".
Según Mujika, este método de estudio es "muy largo y laborioso", pero apropiado para el diagnóstico. "Y luego hacemos secuenciación en sangre. En el cáncer de colon realizamos un estudio molecular en el tumor y observamos el estado de las proteínas. Si están transformados significa que el gen está mutado y entonces miramos en la sangre".
Mujika ha determinado que en el cáncer de mama observan los genes BCRA en sangre y en el de colon, MLH1 y MSH2. "De esta manera, una vez identificada la mutación, podemos valorar el riesgo. Ahora bien, hay que tener en cuenta que no sólo estos genes están expuestos al riesgo, sino que el medio también tiene una gran influencia, así como otros genes como los que regulan la actividad genética. Por eso, entre las hermanas y con la misma mutación, muchas veces ocurre que una tiene un alto riesgo de desarrollar cáncer, mientras que la otra es baja o moderada".
Seguimiento, clave
Implementan medidas preventivas para personas con alto riesgo: "En el cáncer de mama, por ejemplo, es muy importante hacer un seguimiento. Para ello, recomendamos que los más pequeños registren sus pechos y después, a partir de los 20-25 años, realicen mamografías y resonancias".
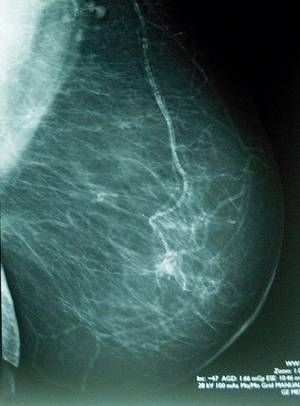
Aunque para mucha gente el método más conocido o más común es la mamografía, tiene algunos aspectos a tener en cuenta. Así, Mujika ha aclarado que esta técnica es especialmente adecuada tras la menopausia. "Antes los pechos son más densos y las lesiones no se ven tan bien. De hecho, tras la menopausia, en el tumor normalmente aparecen microcalcificaciones que se ven muy bien con la mamografía, pero en la juventud las lesiones suelen ser de otro tipo, normalmente nodulosas y no perceptibles. Por ello, a estas edades se realizan resonancias y ecografías".
Además, Mujika considera que la realización de mamografías a lo largo de los años y con frecuencia puede suponer un riesgo: "porque al hacer la mamografía emitimos radiación ionizante. Y aunque controlamos la dosis, no sabemos hasta qué punto puede perjudicar a largo plazo la realización periódica de mamografías, especialmente si es joven y de grupo de riesgo".
También aplican medidas preventivas a las personas con alto riesgo de cáncer de ovario: "A partir de los 30-35 años realizamos un estudio ginecológico y una ecografía vaginal. Además existe un marcador CA-125. Es una proteína, un indicador de cáncer de ovarios que se puede detectar en sangre. Sin embargo, el uso de este test es discutible, ya que este indicador no es muy específico, por lo que el resultado puede ser confuso".
Por otro lado, en el cáncer de ovario, "la prevención no es tan útil como en el cáncer de mama", ha advertido Mujika. "Muchas veces, cuando diagnosticamos el tumor con estas pruebas, está bastante desarrollado, normalmente en el estadio 3 (son 4 estadios desde el 1). Por el contrario, en el sujetador todavía se detectan en el estadio 1. Por eso, el pronóstico del cáncer de ovarios no suele ser tan bueno".
Por último, el riesgo de cáncer de colon aumenta a partir de los 40 años, por lo que se recomienda una colonoscopia anual.
Mujika ha afirmado que todas estas medidas ayudan a realizar un diagnóstico precoz, es decir, con ellas "no se impide" la aparición del cáncer, pero si aparecen, lo hacen inmediatamente. Esto permite tener un mejor pronóstico que los casos que no realizan un seguimiento especial.
Cirugía, sólo en algunos casos
Independientemente de las medidas mencionadas, existe cirugía preventiva. Mujika ha reconocido que no se han realizado estudios aleatorios para probar la eficacia de este método, "sin embargo, en estudios prospectivos hemos visto que esta medida es la que más reduce el riesgo".
"Con las evidencias hasta el momento, no podemos recomendar la cirugía pero sí informar. Además, cuando sospechamos que esta información puede tener una fuerte influencia en la persona, siempre ofrecemos ayuda psicológica", ha añadido Mujika.
Comenta que la cirugía preventiva se realiza en tres casos: masectomía de un pecho sano con cáncer en uno de los pechos y riesgo muy alto de desarrollar cáncer en el otro portador de la mutación; masectomía de ambos pechos, aunque el portador de la mutación sea una mujer sana, cuando el riesgo es alto por su historia familiar; y extirpación de ovarios y trompas de Falopio.
Mujika ve bastantes beneficios a esta última, aunque insiste en que no es posible recomendar la cirugía preventiva: "Hay que tener en cuenta que los ovarios de una mujer que ha sufrido cáncer de mama ya son a menudo estériles por el tratamiento que ha recibido o por la edad. Por lo tanto, la erradicación no tendrá otras consecuencias en este aspecto y, en cambio, impedirá el desarrollo del cáncer, no sólo en los ovarios (y no hay que olvidar que el cáncer de ovario no suele tener buen pronóstico), sino también en los senos. De hecho, en algunos cánceres de mama, el estrógeno contribuye al cáncer, por lo que se favorece la pérdida de producción de estrógenos".
Por el contrario, en el caso de las mujeres sanas, las consecuencias son diferentes. "Con la extirpación de ovarios y trompas anticipamos la menopausia y aumentamos el riesgo de osteoporosis y trastornos del aparato circulatorio", explica Mujika. De ahí que cada caso sea analizado. Abarcan todo el contexto y, además, la cirugía no elimina totalmente el riesgo: "cuando quitamos el pecho porque siempre queda un poco de tejido glandular, y lo mismo ocurre en los ovarios, por lo que queda un pequeño riesgo de carcinoma en el peritoneo".
Además de estas cirugías, en el cáncer de colon a veces se elimina una parte sana, ya que en muchas ocasiones, siendo portador de la mutación, el riesgo de aparecer en la otra parte es muy alto. El cáncer de colon también aumenta el riesgo de desarrollar cáncer de endometrio en mujeres. En estos casos, Mujika aclara que se puede hacer un seguimiento, pero al mismo tiempo reconoce que no hay un método muy bueno de diagnóstico precoz, "eso sí, el pronóstico del cáncer endometrial es mucho mejor que el de los ovarios", matiza.
Profundización en la investigación
Mujika tiene claro que cuanto más sepan de los cánceres de origen genético, más posibilidades tendrán de ayudar a los portadores de mutaciones. "Por ejemplo, se ha observado que la histología de este tipo de cáncer es especial en comparación con otros de etiología diferente. Además, se adaptan mejor a unos tratamientos que a otros, por lo que si bien por el momento no se diferencian en la radioterapia y en este tipo de tratamientos, en el futuro puede darse un tratamiento diferenciado".
Prueba de los esfuerzos realizados en la investigación es una tesis realizada el año pasado. La tesis, titulada "Investigación genética en mujeres con cáncer de mama/ovario hereditario residentes en la CAPV", ha sido realizada por Elena Beristain, Doctora en Biología en la UPV. El director de la tesis ha sido Isabel Tejada, responsable del laboratorio de genética molecular del Departamento de Bioquímica del Hospital de Cruces, en el que ha realizado principalmente su investigación Beristain.
Beristain ha analizado a 274 pacientes de los hospitales de Cruces y Txagorritxu con cáncer de mama o ovario. Además, en el estudio han participado 115 familiares de pacientes y otras 132 mujeres que han realizado labores de control poblacional. Beristain ha separado de forma molecular los genes BRCA1 y BRCA2 de todos ellos, así como parte de la secuencia de otro gen relacionado con la enfermedad.
El estudio ha demostrado que existen variadas variantes en estos genes: patológicas, neutras y de significado desconocido. Entre ellas, la frecuencia de mutación patológica es del 10%, cifra que según Beristain es inferior a la de otras poblaciones europeas.
Por otro lado, teniendo en cuenta la edad, el investigador ha comprobado que entre los familiares de los pacientes portadores de los genes BRCA1 y BRCA2, el riesgo acumulado de cáncer de mama es del 69% o 67% respectivamente. Por sexo, Beristain destaca que el cáncer de mama masculino se relaciona principalmente con las mutaciones del gen BRCA2.
Estos datos y todas las conclusiones obtenidas en la tesis servirán para realizar un seguimiento diferenciado a las personas con cáncer hereditario y a sus familiares. En la actualidad es Técnico Auxiliar de Investigación en la Unidad de Investigación del Hospital de Cruces.







