Vous aussi dessinez des coeurs symétriques ?
De temps en temps, dans une lettre d'anniversaire ou dans la vapeur que la douche a laissé dans le miroir, vous avez certainement dessiné un cœur. Ou cela, vous nous avez dit que c'est un cœur.
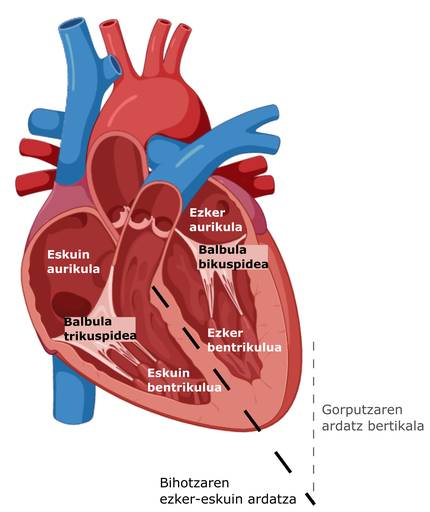
Regardez attentivement (Figure 1). Vous savez, bien sûr, qu'il s'agit d'une simplification de l'organe appelé coeur et que nous l'utilisons en fait pour montrer des concepts plus complexes que ceux qui peuvent être assignés à l'organe. Mais avez-vous déjà pensé au-delà? Quelles sont les caractéristiques qui rendent ce dessin en quelque sorte un mensonge rond? À partir d'aujourd'hui, vous pouvez dessiner des coeurs simplifiés mais au moins asymétriques comme geste de reconnaissance à votre cœur.
Asymétrie gauche-droite du corps humain
Nous avons tendance à penser que les visages et les corps symétriques sont plus beaux, mais l'asymétrie est une caractéristique enracinée dans le corps humain en termes d'anatomie interne. Il se produit à deux niveaux: en ce qui concerne l'emplacement général et les organes isolés. Prenons comme exemple le volume du corps dans son ensemble et dessinons un axe gauche-droite (figure 2).
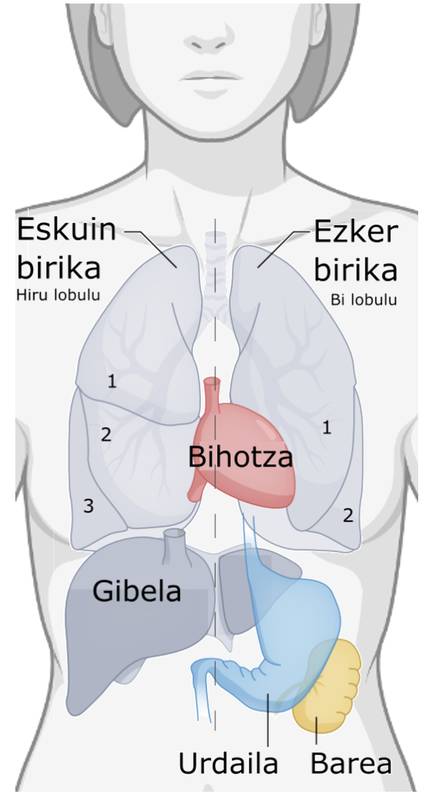
À ce stade, il convient de noter que dans le langage médical, la droite et la gauche s'installent du point de vue du corps décrit. Si nous regardons une personne face à face (comme dans la figure 2), la droite de l'individu se trouve sur notre gauche et vice versa. Compte tenu de cela, dans la figure 2, nous pouvons voir que le foie se situe sur la droite, l'estomac et la rate sur la partie gauche. Par exemple, si nous regardons les organes internes seuls, les poumons ont trois lobes sur le côté droit et deux sur le côté gauche. Le cœur est asymétrique pour les deux critères. D'une part, le plus grand volume sur la rive gauche. En outre, il présente une inclinaison, c'est-à-dire que l'axe gauche-droite du cœur n'est pas parallèle à l'axe vertical du corps (figure 3). D'autre part, malgré quatre caméras, les caméras de droite et de gauche sont différentes, à la fois par leur histologie et par les liaisons routières (artères et veines). Il convient de noter, par exemple, que la valve trimaxi sépare l’oreillette droite du ventricule droit, c’est-à-dire qu’elle se compose de trois segments, et que la valve (ou mitrale) entre l’oreillette gauche et le ventricule se compose de deux segments.
Importance physiologique de l'asymétrie cardiaque
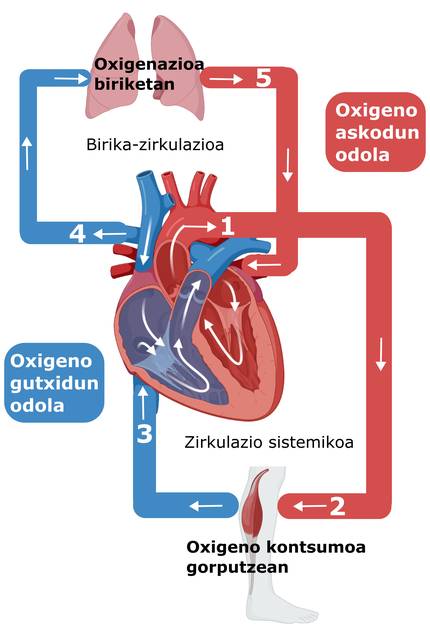
Bien sûr, l'attention à l'asymétrie va bien au-delà de souligner les caractéristiques évidentes, car elle a une grande importance physiologique. La structure asymétrique du cœur est nécessaire pour établir ce que nous appelons la double circulation, et ainsi l'organe remplit sa fonction: propager le sang oxygéné à toutes les parties du corps (Figure 4).
Le ventricule gauche pompage avec force le sang oxygéné à l'aorte (numéro 1 de la figure 4), qui se ramifiera encore et encore jusqu'à former des artères plus petites et capillaires qui atteindront toutes les cellules (numéro 2). Lorsque les cellules ont pris de l'oxygène, le sang faible en oxygène revient au cœur à travers les veines cava (numéro 3). Ce premier cycle est appelé circulation systémique à la dispersion du sang oxygéné dans le corps et à la restitution du sang au cœur de “déchets” à faible teneur en oxygène. Une fois le sang faible en oxygène atteint l'oreillette droite, il passe au ventricule droit par lequel il est pompé à travers l'artère pulmonaire (numéro 4) pour que le sang soit oxygéné dans les poumons et retourne à l'oreillette gauche dans les veines pulmonaires (numéro 5). Ce deuxième cycle, c'est-à-dire le déplacement vers les poumons pour rétablir l'oxygénation, est appelé circulation pulmonaire.
Revenons donc au rôle dans lequel joue l'asymétrie pour que la double circulation se produise correctement. D'une part, en ce qui concerne les caractéristiques histologiques, il est nécessaire que le ventricule gauche soit plus musclé, car la force de pompage doit fournir une pression suffisante sur le sang pour atteindre les cellules les plus éloignées du corps (et, au contraire, la force de pompage du ventricule droit ne doit être que suffisante pour atteindre le poumon du cœur). D'autre part, cette artère de caméra, comme expliqué dans toutes les connexions d'attente de caméra, ne doit se produire que de cette manière, afin que la circulation soit adéquate.
Genèse de l'asymétrie dans le développement embryonnaire
En se référant aux trois axes qui définissent l'espace tridimensionnel, l'axe gauche-droite est le dernier défini dans le développement embryonnaire. Un embryon est au début une sphère parfaite dans laquelle les cellules sont placées de manière homogène. Il grandit, doublant les cellules, mais ce n'est qu'une masse sans ordre connu. S'il n'y a pas d'asymétrie, aucun axe ne peut être défini ou, mieux dit, les axes peuvent être définis de toute façon. Tout au long du développement, certains signaux moléculaires permettent l'apparition de structures caractéristiques sur l'embryon qui définissent l'axe supérieur inférieur et l'axe d'avancement. Entre autres, la création de la ligne primitive laisse cette structuration établie [1] (figure 5).
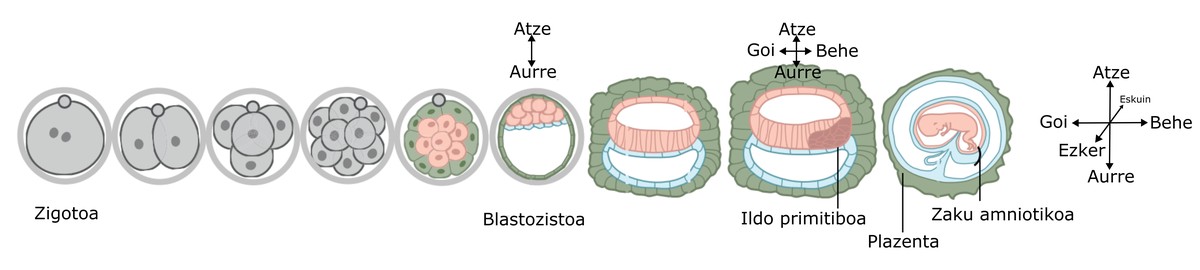
Lorsque deux axes ont été définis, le troisième est établi avec force, puisqu'il n'existe qu'une seule façon d'établir une troisième ligne perpendiculaire à deux lignes droites dans l'espace. À ce moment-là, la partie gauche et droite de l'organisme sont définies, mais, pour l'instant, elles sont totalement symétriques. Au cours de la troisième semaine de développement de l’embryon humain, les cellules précurseurs du cœur commencent à former un tube cardiaque au centre de l’axe gauche et droit de l’embryon [2], [3]. Ce tuyau est situé au début de manière droite et verticale. Il commence ensuite à se plier jusqu'à adopter la forme de boucle (boucle en anglais) (Figure 6). Ce fait est d'une grande importance car (1) il établit une forme précurseur du cœur (morphologie), qui est le premier organe fonctionnel qui se produit dans l'organisme, et (3) est la première asymétrie de gauche à droite observée dans l'embryon.
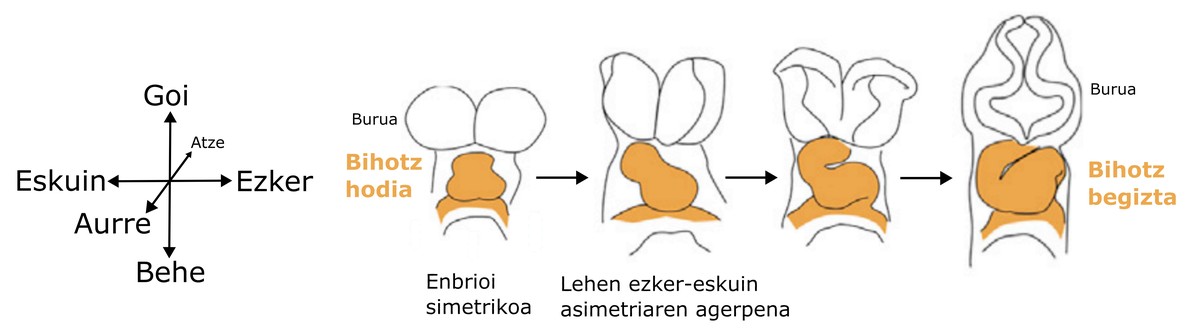
Au fur et à mesure que la boucle cardiaque se développe, un cœur mûr avec l'anatomie exacte décrite ci-dessus se produit. En outre, tous les organes asymétriques mentionnés ci-dessus créeront leur propre forme et développeront leurs propres caractéristiques asymétriques. Tous ces processus sont étudiés dans la science embryonnaire - morphogénique et ont une importance non seulement parce qu'ils nous fournissent des informations de base sur notre origine, mais aussi parce qu'ils nous aident à comprendre les causes d'un développement erroné.
Défauts de développement et symptômes pathologiques
Ce qui est décrit jusqu'à présent est une explication de ce qui se passe chez les êtres humains sains. Dans le langage médical, nous utilisons l'expression latine situs solitus pour nous référer à la distribution d'organes d'un être humain qui s'est développée régulièrement (Figure 7). Dans le développement embryonnaire peuvent apparaître des défauts qui modifient l'asymétrie de gauche à droite. La fréquence moyenne est de 1 cas pour 2000 habitants [2]. Ces troubles peuvent avoir un impact systémique, c’est-à-dire qu’ils peuvent provoquer des malformations dans tous les organes asymétriques du corps, ou dans certains cas. Si un déplacement total se produit, c’est-à-dire si un individu est déplacé à gauche et à droite, nous le décrivons comme une image miroir avec l’expression situs inversus totalis. Si les organes eux-mêmes et les autres ne se déplacent pas de manière confuse et sans concordance, nous trouverons un état de situation ambigu ou hétérotaxe [4].
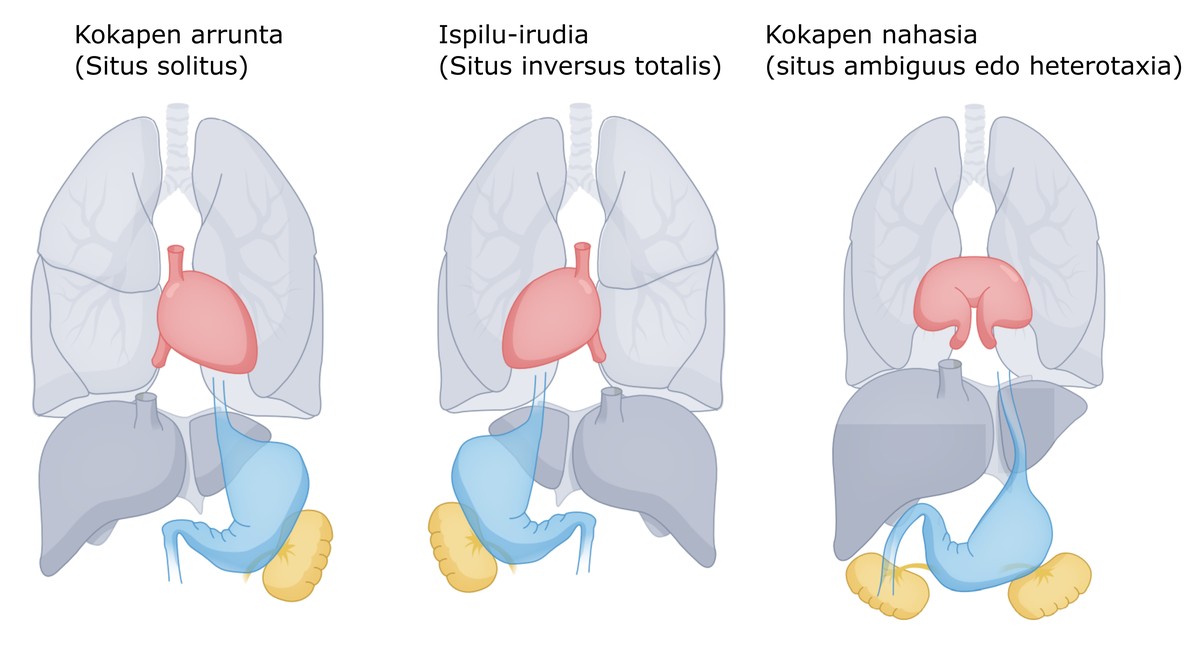
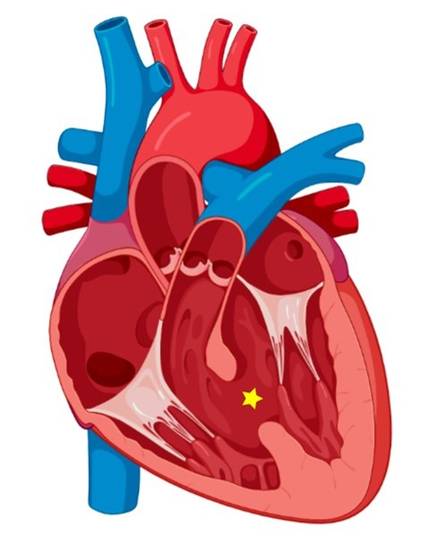
Nous avons décrit de manière générale les pathologies possibles des organes internes, mais le même principe peut être appliqué concrètement au cas du cœur. Si un individu présente des situs inversus totalis, par définition, tous les organes, y compris le cœur, seront déplacés. Si l'image du miroir est parfaite et que, par conséquent, toutes les artères et les veines sont connectées à la caméra correspondante, la fonction du cœur est généralement accomplie de manière normale. La casuistique de l'hétérotaxie, au contraire, est très étendue, de sorte que les prévisions sont très variées [5]. Parfois, nous pouvons rencontrer de graves malformations cardiaques. Elles sont appelées cardiopathies congénitales et proviennent, au moins en partie, de formes inadéquates de boucle cardiaque. Pour citer deux exemples, l’échange de position de l’aorte et de l’artère pulmonaire, ou le fait que la paroi musculaire séparant les parties gauche et droite du cœur ne soit pas complètement fermée et ait des « trous » (Figure 8). Heureusement, certaines malformations ont été résolues chirurgicalement, tandis que d'autres sont excessivement complexes, de sorte que le patient devra vivre avec ce défaut et, souvent, provoquera une mort prématurée.
Que peut faire la science pour tout cela?
Une meilleure compréhension des causes des cardiopathies congénitales est indispensable pour pouvoir effectuer un diagnostic plus rapide chez les nouveau-nés et offrir des traitements chirurgicaux plus efficaces. La médecine a parcouru un long chemin jusqu'à aujourd'hui, mais il existe encore de nombreux cas qui ne peuvent pas être résolus.
Pour approfondir cette connaissance, comme d'habitude dans l'étude des biocides, des modèles animaux sont utilisés. Dans l'étude du développement cardiaque, les chercheurs étudient des modèles d'animaux avec des variations génétiques (mutations) et mesurent l'excitation concrète que chaque variante produit dans le développement. Ces ressources permettent de connaître de plus en plus précisément ce processus de conversion de la boucle cardiaque dans un cœur mature. En outre, l'homologation des gènes animal et humain permet de prédire l'effet des mutations humaines sur le développement, ce qui peut permettre un diagnostic précoce à un moment donné. La recherche exige cependant un investissement considérable en temps et en argent. En retour, nous avons un bon voyage pour comprendre la rémunération du développement des avancées médicales et la complexité de la biologie. Si la beauté est à l'intérieur, nous pouvons affirmer que la beauté est asymétrique.
Bibliographie
1] Shahbazi MN. Mechanisms of human embryo development: from cell fate to tissue shape and back. (2020) Development. 147(14):dev190629.
[2] Desgrange A, et al. Left-right asymmetry in heart development and disease: forming the right loop. Development. 145(22):dev162776.
[3] Desgrange A, et al. (2020) Transient Nodal Signaling in Left Précursors Coordinates Opposed Asymmetries Shaping the Heart Loop. Dev Cell. 55(4):413-431.e6
[4] Djenoune L, et al. (2022) A change of heart: new roles for cilia in cardiac development and disease. Nat Rev Cardiol. 19(4):211-227.
[5] Lin AE, et al. (2014) Laterality défécation in the national birth déféts ion study (1998-2007): birth primence and descriptive épidéiology. Am J Med Genet A. 164A(10):2581-91.