Muerte de moléculas

XVIII. finales del siglo XIX A lo largo del siglo XX se produjo una gran revolución en la química. Pertenecen a esta época, por ejemplo, los fundadores de la química moderna Lavoisier, la ley de conservación de la masa enunciada, o la teoría atómica de Dalton. Lógicamente, las nuevas teorías basadas en la experimentación supusieron la exclusión de las que hasta entonces fueron aceptadas. Quizá el ejemplo más conocido es el XVII. Científicos de finales del siglo --J. J. Becher y G. Stahl es el ocaso de la teoría del flogisto propuesta para explicar la combustión. La comunicación de los avances en diferentes áreas de investigación dio lugar a estrechas relaciones entre científicos. Academias, revistas científicas y encuentros se extendieron por todas partes. En la mayoría de los casos, los intercambios de ideas eran el origen de discusiones entusiastas o conflictos científicos, pero en ocasiones fueron fuente de reconciliaciones y colaboraciones científicas. En este último caso se puede situar la polémica que Friedrich Wöhler y Justus von Liebig tuvieron sobre la isomería de los compuestos químicos como punto de partida de numerosas colaboraciones.
Sin embargo, la eliminación de ideas científicas obsoletas fue un importante leitmotiv de muchos científicos, y los trabajos realizados con esta intención dieron lugar a grandes avances en la ciencia. Por tanto, no hay que olvidar que todas las teorías, incluso las erróneas, han cumplido su función en la historia de la ciencia y, por supuesto, de la química. Si bien los hechos anteriormente mencionados -el flogisto o la isomería - son realmente atractivos, lo que luego traeré a la plaza es otra de esas bellas historias de la historia de la química: F. Cuando Wöhler sintetizó la urea y sus consecuencias en la teoría bitalista.
Vitalismo
Vitalismo XIX. A principios del siglo XX era un pensamiento en estado puro. El principio básico de la teoría vitalista era que entre el mundo orgánico y el inorgánico hay un abismo impenetrable. Para el fisiólogo vitalista francés Xavier Bichat, los cuerpos vivos sobrevivían a la capacidad de enfrentarse a fuerzas inorgánicas que tendían a destruirse. La propia vida era una competencia entre las fuerzas inorgánicas destructivas enfrentadas y la fuerza de vida. Para mantener la vida era necesario que las fuerzas vitales tuvieran éxito frente a las fuerzas químicas. El objetivo de las fuerzas químicas era convertir los organismos vivos en elementos químicos básicos. Según este enfoque del vitalismo, la química orgánica y la inorgánica estaban reguladas por fuerzas absolutamente contrapuestas.
Otro ejemplo importante de teoría vitalista lo encontramos en el libro A Manual of Chemistry, escrito por John Webster, que se utilizaba en la Universidad de Harvard antes del experimento de Wöhler. Según las explicaciones de Webster, los cuerpos orgánicos estaban formados por cuatro elementos inorgánicos, pero la vida era más que la unión de estos cuatro elementos: existía un principio de vida independiente de las fuerzas químicas. En consecuencia, el mundo químico estaba dominado por dos fuerzas: la afinidad química y la fuerza de vida. Por un lado, la afinidad química servía para explicar las reacciones inorgánicas y, además, estaba en manos de los químicos dominar y utilizar esa fuerza. Por otro lado, la fuerza de vida regulaba el mundo orgánico, justificando la propia vida. Esta fuerza no estaba --y nunca dependía de los químicos del estar--. Por tanto, el vitalismo señalaba que era imposible sintetizar compuestos orgánicos en el laboratorio. La fuerza de vida no era la herramienta de la ciencia.
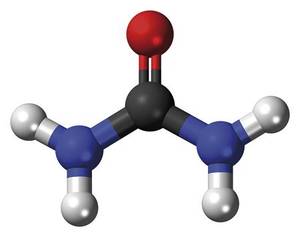
Síntesis de urea
En 1828 Wöhler buscaba una reacción para sintetizar el isocianato amónico (NH 4 NCO) debido a las investigaciones sobre isomería. Para ello calienta la solución que contenía isocianato de plata (AgNCO) y cloruro de amonio (NH 4 Cl), al considerar que se produciría la siguiente reacción química:
GaNCO + NH 4 ClNH 4 NCO + AgCl
Sin embargo, los cristales obtenidos como producto de la reacción correspondían a un compuesto que Wöhler no esperaba. Consciente de ello, analizó y analizó la sustancia blanca de diversas maneras y concluyó que debía ser urea. La urea, CO(NH 2 ) 2 , es un compuesto químico conocido desde 1773 que llega a la orina como consecuencia del metabolismo de las proteínas. Pero, ¿cómo se obtenía la urea? De hecho, el isocianato de amonio --de quien buscaba Wöhler - se transformaba nada más nacer de la causa de la reacción de isomerización dando urea:
Norma NH 4 NCO
La síntesis de urea no tenía mucho interés, pero el experimento de Wöhler demostró por primera vez que era posible sintetizar una molécula biológica sin necesidad de fuerza de vida. Dicho de otro modo, sintetizó una molécula orgánica a partir únicamente de componentes inorgánicos. Desde el punto de vista actual, aunque podemos considerar la síntesis de la urea como punto de partida de un nuevo campo científico --la química orgánica-, XIX. Muchos científicos de principios del siglo XX no veían tan claro el fin del vitalismo.
Revisión del mito de Wöhler
La visión que el propio Wöhler tenía del experimento ha sido objeto de múltiples discusiones y de diversas interpretaciones sobre la síntesis del urea: que era un ferviente rival de la teoría vitalista, que siguió siendo vitalista o que no se había dado cuenta de la importancia del experimento. De un modo u otro, ante las incorrectas interpretaciones de muchos autores, el mito de Wöhler estaba en marcha. Un mito que ha llegado hasta ahora. En este sentido, en 1996 P. S. Cohen y S. M. Cohen analizó 35 libros de texto de química y llegó a conclusiones preocupantes: en la mayoría de los libros, el suceso sobre Wöhler aparece con malas matizaciones históricas, afirmando que en muchas ocasiones la síntesis de urea descartó el vitalismo y surgió la química orgánica. Además, la importancia del experimento se manifiesta de forma confusa en la mayoría de los libros de texto, según la investigación.
Según las revisiones históricas del suceso, a pesar de la convicción extendida entre los químicos, es un error histórico inaceptable pensar que la síntesis de la urea provocó el fracaso del vitalismo o que el objetivo de Wöhler era anular la teoría vitalista. En su artículo de comunicación a la comunidad científica de la síntesis de la urea, Wöhler hace una sola vez referencia a la relación entre su experimento y su vitalismo. Da más importancia a la reacción de isomerización obtenida y J. J. De las cartas que escribió a Berzelius, químico de reconocido prestigio y ex profesor de Wöhler, se deduce que no creía que atravesara la frontera entre el mundo orgánico e inorgánico. Tras el descubrimiento, Wöhler siguió creyendo en la fuerza vital de las moléculas. La teoría vitalista estaba tan arraigada que entre los científicos de la época la síntesis de la urea no fue suficiente para romper esas ideas. Pero, al hilo de esto, ¿cuál es entonces la importancia del experimento, si quien lo hizo tampoco lo consideró importante? Según los vitalistas, era imposible sintetizar en el laboratorio un compuesto orgánico. Pero cuando Wöhler lo hizo, ¿por qué no cambió el pensamiento científico?
Un paso más cerca
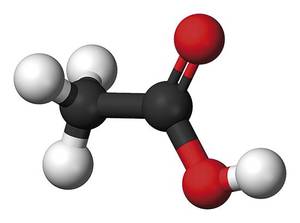
Aunque el fracaso del bitalismo no llegó de repente, algunos contemporáneos de Wöhler cambiaron su visión de la fuerza de vida. Posteriormente, quienes no estaban de acuerdo con el vitalismo, partiendo de la síntesis de la urea, sintetizaron otras moléculas orgánicas en el laboratorio: Kolbe, ácido acético; Berthelot, acetileno, benceno o metano --una lista muy extensa de este último -; Strecker, varios aminoácidos, etc. Así, poco a poco, los que apostaban por las teorías vitalistas disminuyeron, y se produjo un descenso notable tras la síntesis del ácido acético Kolbek (1845). La experimentación mostraba claramente que las moléculas orgánicas, al igual que la urea, estaban muertas.
Entre 1844 y 1870, el número de compuestos orgánicos conocidos pasó de 720 a 10.700 --el de los inorgánicos de 3.250 a 5.300.-. Fue, por tanto, una época muy próspera en la química orgánica. A medida que se fueron acumulando y acumulando argumentos contra el vitalismo, el vitalismo quedó obsoleto en el siglo XX. Para principios del siglo XX. Aunque la síntesis de urea de Wöhler no fue más que el primer paso de un largo camino, fue un paso imprescindible. En ello radica la importancia de la síntesis de la urea, que suscitó un debate sobre la fuerza de vida y el vitalismo, iniciando una de las etapas más prósperas de la química orgánica.
Retos de futuro
Las síntesis de moléculas mencionadas anteriormente, junto con otras muchas que se han realizado posteriormente, demuestran la capacidad de los químicos para elaborar compuestos presentes en la naturaleza o moléculas inexistentes. Mediante el estudio de las sustancias complejas presentes en la naturaleza y la comprensión de la reactividad y propiedades de las moléculas, los científicos obtienen cada día nuevas moléculas que pueden tener características realmente interesantes. La sinergia entre la química analítica y la orgánica ofrece amplias posibilidades --ilimitadas, agi-- en el campo de la síntesis molecular.
Por último, cabe recordar que, al igual que la química orgánica sintética, la biología sintética es también una ciencia puntera. Cabe destacar, por ejemplo, que en 2010 el biólogo Craig Venter logró una célula con genoma sintético cuando lo dio a conocer en la revista Science. Al igual que la química orgánica sintética, la biología sintética responderá a muchas preguntas en los próximos años y propondrá más retos de futuro. Y es que la ciencia ha dejado claro que las moléculas orgánicas no tienen fuerza de vida, pero ¿se puede conseguir la vida misma en el laboratorio? ¿Pronto conoceremos otro Wöhler o Kolbe?
Bibliografía
Agradecimientos al Departamento de Educación, Política Lingüística y Cultura del Gobierno Vasco por su colaboración con la beca predoctoral.