Electròlits polimèrics de bateries en la caça d'anions
Què passaria si una bateria només pogués emmagatzemar part de l'energia utilitzada per a carregar? O si només una petita part de l'energia que guarda pogués passar al dispositiu mòbil? Les reaccions laterals a l'interior de la bateria tenen molt a veure en això, i trobar un electròlit polímer adequat pot ajudar a millorar l'eficiència de la bateria.

Quan en 1991 Sony va llançar per primera vegada bateries d'ió liti (VOL), es van obrir les portes a la revolució dels dispositius portàtils. Gràcies a aquestes bateries s'han estès tant els telèfons mòbils, tauletes i ordinadors portàtils que utilitzem actualment. No obstant això, a mesura que les necessitats energètiques augmentin, és necessari fer un pas més.
Si en l'ànode d'aquestes bateries s'utilitza el metall liti (Li0) en lloc de grafit, la seva capacitat es multiplicaria per deu. El liti metall, no obstant això, és molt reactiu i té problemes combinant-los amb electròlits líquids inflamables i volàtils. En definitiva, és més fàcil que es produeixin reaccions entre un líquid i un sòlid que entre dos sòlids. Per això, quan s'utilitzen electròlits líquids juntament amb l'elèctrode Li0, la probabilitat de reacció lateral és major.
Una solució és la utilització d'electròlits polimèrics sòlids. En aquest sentit, María Martínez i les seves coautores del CIC Energigune han publicat recentment en la revista Advanced Functional Materials, que l'addició d'una mica de sal LiFSI de liti entorn del 2%) millora notablement les característiques de l'electròlit polímer PSTFSI/PEO.
Electròlit, pont entre elèctrodes
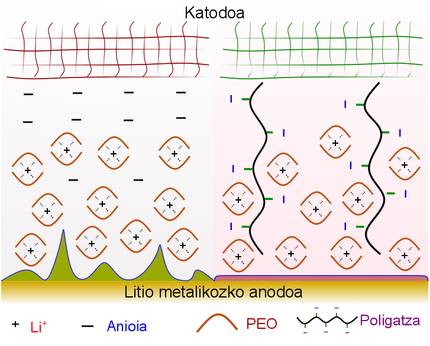
En els electròlits líquids o electròlits convencionals, els simples cations i anions tenen una gran mobilitat, la qual cosa pot provocar la polarització de l'electròlit. És a dir, acostar els cations a l'elèctrode negatiu i apilar els anions al voltant de l'elèctrode positiu, la qual cosa permet crear zones de càrrega parcial positiva i negativa dins de l'electròlit. En aquests casos es creen les sortides denominades dendritas a l'ànode de liti metàl·lic. Si les dendritas travessen l'electròlit i arriben fins a l'altre elèctrode, es produeixen curtcircuits que provoquen perill i pèrdua d'energia.
Per a solucionar aquest problema, actualment s'utilitzen electròlits amb polímers sòlids que dificulten la creació de dendritas. En qualsevol cas, tal com s'esmenta en la publicació dels investigadors del CIC Energigune, és necessari que existeixi alguna cosa que impedeixi la mobilitat dels anions de l'electròlit. Així, en els electròlits polimèrics que només són conductors d'ions de liti (SLIC), l'anió s'uneix covalentemente a un tronc de polímer que dificulta la mobilitat. En conseqüència, en aquests casos s'evita la polarització de l'electròlit i només el catió de liti (Li+) pot desplaçar-se cap a l'elèctrode.
Electròlit polímer LiPSTFSI/PEO
S'han realitzat nombrosos estudis sobre l'electròlit polímer sòlid LiPSTFSI/PEO. En general, es pot dir que el polietilè és un polígon de liti del tronc de poliestirè (PS) estès en òxid (PEO). Aquest electròlit, no obstant això, presenta una baixa conductivitat iònica. Això es deu al fet que el PEO i el PS associat a l'anió no són intrínsecament interactius, la qual cosa dificulta la dissolució de la sal LiPSTFSI.
A més, entre l'elèctrode Li0 i l'electròlit es crea una superfície molt resistent al liti. Tenint en compte que la funció de l'electròlit de les bateries de liti és transportar els cations Li+ de l'elèctrode a l'elèctrode, totes dues característiques redueixen l'eficiència de les bateries.
L'equip de recerca ha pogut comprovar que quan a aquest electròlit polímer se li afegeix una mica de sal LiFSI (només un 2%), la conductivitat dels ions Li+ a l'interior de l'electròlit augmenta considerablement. De fet, el RMN en estat sòlid (SSNMR) i l'espectroscòpia Raman han pogut comprovar que l'addició d'aquesta sal facilita la interacció entre l'òxid de polietilè i el poliestirè del tronc de l'electròlit i la dissolució del LiPSTFSI. En aquesta situació, la conductivitat iònica es deu principalment als cations de liti, ja que l'anió queda atrapat ja que està unit al poliestirè i interacciona amb el polietilè.
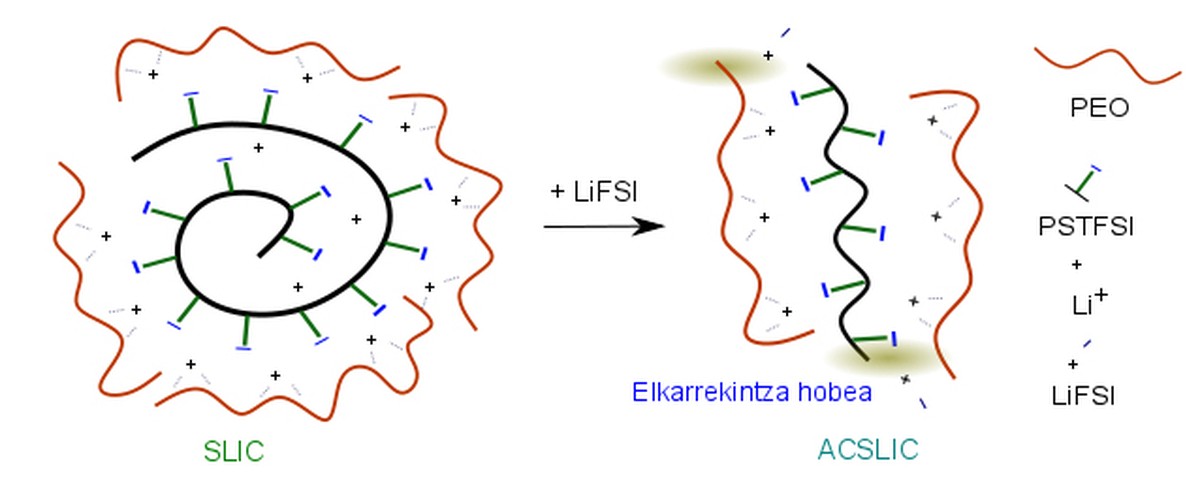
També s'ha comprovat que l'addició d'aquesta sal redueix la resistència al liti en la interfase elèctrode/electròlit. Gràcies als càlculs teòrics s'ha pogut comprovar que la sal LiFSI es redueix en arribar a la superfície de l'elèctrode de liti metàl·lic i es genera LiF. La presència de LiF en la superfície del metall liti facilita notablement el moviment del catió de liti.
I usant en bateria…
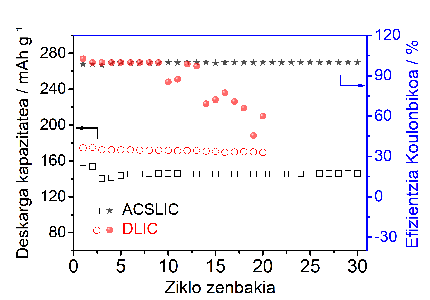
Experimentalment han pogut demostrar que amb aquest electròlit de polímer es trigaria el doble de temps a crear dendritas en l'ànode de liti metall i a produir-se un curtcircuit en la bateria.
Bàsicament, en utilitzar aquest electròlit polímer sòlid en una bateria amb càtode LiFePO4, s'obté una major eficiència de la bateria que amb altres electròlits polimèrics. És més, aquest polímer electròlit es pot utilitzar també per a altres càtodes de major tensió.
A més, el realitzat per l'equip de recerca de CIC EnergiGUNE (és a dir, dopar l'electròlit polímer amb una petita quantitat de sal) és més senzill i econòmic que sintetitzar altres electròlits polimèrics.
Bibliografia:
Martínez M., Sánchez E., Qiao L., Zhang I. Judez X, A. Santiago, Aldalur I, Sr. Carrasco, Ed. Zhu, Forshit M., Armand M., Zhang H.; Unprecedented Improvement of Single Li-Ion Conductive Solid Polymer Electrolyte Through Salt Additive; Adv. Fun. Mat. (2020)





