Cèl·lules en càpsules Nou enfocament en el tractament de malalties
Farmazian doktorea. Biofarmazia, Farmakozinetika eta Farmazia-teknologiako irakasle kolaboratzailea
Farmazia Fakultatea UPV-EHU, Vitoria-Gasteiz
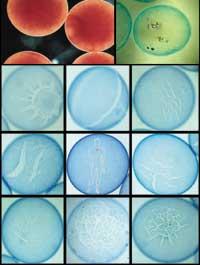
Microcápsulas XX. El seu ús es remunta a mitjan segle XX, concretament en l'àmbit farmacèutic. Al principi es pretenia desenvolupar compostos farmacèutics que flueixen a llarg termini, és a dir, produir sistemes de flux controlat del producte. D'aquesta forma s'aconseguia alliberar lentament el medicament i allargar l'efecte beneficiós al llarg del temps. En altres casos, la tecnologia de les càpsules es va utilitzar per a ocultar el sabor de certes susbancias o reduir la irritació gàstrica provocada per la medicació. Amb el temps, les microcápsulas es van estendre a l'alimentació (encapsulant vitamines i olors dolces) o a l'agricultura (amb pesticides i fertilitzants). La biotecnologia d'aquest nou segle també ha buscat la resposta als problemes mèdics en l'encapsulació.
Però, què és la microencapsulación cel·lular?
Aquesta tècnica consisteix a recollir el material biològic (cèl·lules, bacteris...) en esferes polimèriques no contaminants i biodegradables. Les cèl·lules encapsulades, a més de fluir productes beneficiosos per als pacients (insulina, hormona del creixement...), mantindran la funció en el temps.
Les cèl·lules són capturades en càpsules de forma circular. Les càpsules tenen un aspecte similar al de les cèl·lules normals: la membrana de la càpsula sembla una membrana lipídica de la cèl·lula i les cèl·lules encapsulades un conjunt d'organel·les intracel·lulars. Amb aquest disseny, la unió completa de les cèl·lules permet emmagatzemar-les en una esfera de materials no contaminants i construir una zona de protecció.
Aquesta tècnica ha de ser vesteixi com una nova estratègia d'administració de medicaments. A diferència dels productes farmacèutics convencionals (comprimits o càpsules), en el cas de cèl·lules encapsulades, a més de la farmàcia, la seva fàbrica, és a dir, la pròpia cèl·lula, està en el medicament. D'aquesta manera, una sola vegada és suficient perquè es noti el benefici durant molt de temps i el pacient no haurà de prendre la píndola o la injecció d'insulina cada dia. A més, el taller biològic encapsulat (les cèl·lules) comprendrà millor que ningú l'estat del cos, per la qual cosa la seva producció serà conforme amb les necessitats del cos.
Raons per a encapsular cèl·lules
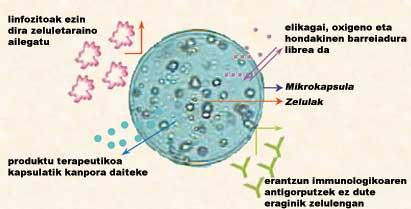
Tenint en compte que les cèl·lules són productores de productes beneficiosos, per què no sols se subministren cèl·lules? La resposta a la pregunta ha de buscar-se en la nostra resposta immunològica. De fet, la resposta immunològica que desenvolupa el cos contra partícules estranyes (virus, microorganismes...) destruirà qualsevol material biològic (a més del material del pacient). El cos no percep les cèl·lules donades des de fora com a pròpies i no entén que la seva funció és curar el cos. En conseqüència, activa els limfòcits i segrega anticossos per a destruir les cèl·lules.

Les cèl·lules, encapsulades en esferes polimèriques, s'oculten de la resposta immunològica. Per a això és absolutament necessari que els polímers siguin biocompatibles, és a dir, que no siguin nocius per a les cèl·lules i el cos. La resposta immunològica no considerarà cap càpsula desconeguda i les cèl·lules encapsulades treballaran durant molt de temps (mesos o anys). Les càpsules requereixen un disseny adequat per al seu correcte funcionament. El laboratori de Farmàcia i Tecnologia Farmacèutica de la Facultat de Farmàcia de la UPV/EHU es dedica a la recerca i producció de càpsules amb finalitats terapèutics.
Per a obtenir un bon producte, primer cal tenir en compte la grandària de l'esfera. En les microcápsulas el diàmetre de l'esfera és inferior a un mil·límetre. Això es deu al fet que quant menor sigui la grandària, major serà la vida de les cèl·lules, degut principalment a la major dispersió de nutrients i oxigen a les cèl·lules. Al mateix temps, la membrana de les microcápsulas ha de ser semipermeable.
Aquesta característica permet a les substàncies travessar la membrana en funció de la seva grandària i càrrega. És a dir, s'eliminaran els residus (lactat) i les substàncies beneficioses secretadas per les cèl·lules i s'introduiran sense obstacles molècules de petita grandària (oxigen, glucosa...). Però els limfòcits i anticossos no podran dispersar-se fins a l'interior de l'esfera i les cèl·lules estaran completament protegides. Aquesta característica es denomina inmunobabesa (Figura 1).
Procés d'encapsulació cel·lular

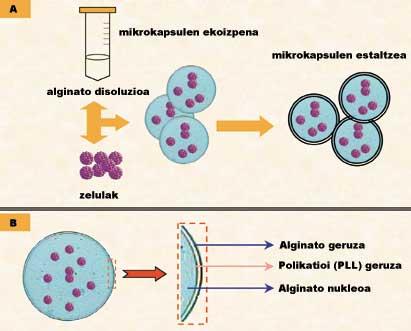
Les microcápsulas poden ser fabricades amb diferents materials i tècniques, però el procediment de microencapsulación segueix un protocol general: primer es barregen la solució de polímer i les cèl·lules i després es creen microcápsulas. Finalment, perquè siguin semipermeables, les càpsules es recobreixen amb altres materials (Figura 2-A). Per tot això, els factors més importants a controlar són dos: 1) eina d'encapsulat i material utilitzat i 2) tipus de cèl·lula seleccionada.
- La producció de càpsules pot ser molt variada, encara que probablement el material més investigat i utilitzat ha estat l'alginato polímer. L'alginato és un polisacàrid que s'extreu d'algues marrons. Es tracta d'una substància natural amb una càrrega negativa en dissolució i unes excel·lents propietats encapsuladoras. L'alginato, en barrejar-se amb una substància de càrrega oposada (principalment poli-L-lisina, PLL), produeix una membrana semipermeable d'alta estabilitat. Un altre recobriment realitzat amb una capa d'alginato generarà una membrana d'alginato pll-alginato d'alta estabilitat i biocompatibilitat (Figura 2-B). Existeixen diferents eines d'encapsulació cel·lular. En el laboratori de Farmàcia i Tecnologia Farmacèutica s'utilitza un generador de gotes electroestàtic que produeix càpsules de la mateixa grandària. Es diu generador de gotes perquè genera gotes molt petites de la suspensió polímer cel·lular i electroestàtic perquè utilitza un diferencial de potència per a aconseguir l'objectiu.
- La biologia és tan important com el desenvolupament tecnològic en la producció de microcápsulas. L'elecció de la mena de cèl·lula és fonamental, ja que encara que flueixi el mateix producte beneficiós, la biologia de cada tipus de cèl·lula condicionarà l'èxit de la tècnica. D'altra banda, per a aconseguir grans quantitats de cèl·lules és important que durant la fase de creixement les cèl·lules tinguin una alta capacitat de fragmentació. Però és encara més urgent perdre en la mesura que sigui possible aquesta capacitat després de la seva encapsulació.
I és que si les cèl·lules es multipliquen molt dins de la càpsula, no hi haurà aliment per a tots i moltes cèl·lules moren. A més, un augment excessiu del nombre de cèl·lules podria provocar l'explosió de la càpsula, que quedaria condicionada per la resposta immunològica de les cèl·lules (veure exemple en la Figura 3).
Resultats i benefici per a la societat
En la bibliografia científica es poden trobar fàcilment aplicacions reeixides d'encapsulació. Molts es refereixen a recerques realitzades amb animals de laboratori, però un alt percentatge són proves realitzades amb éssers humans. El protocol de preparació de les càpsules és molt similar per a totes les malalties: només varia el tipus de cèl·lula i la via d'administració.
En l'actualitat, les cèl·lules poden ser preses de fonts cada vegada més diverses, bé des del propi malalt (alogenéticos) o des d'un animal (xenogénicos). Per exemple, per a buscar una solució a la diabetis, diversos investigadors han encapsulat les illes de Langerhans obtingudes a partir de porcs (cèl·lules de l'àrea de producció d'insulina). De fet, la insulina porcina i la insulina humana se separen en un únic aminoàcid. En una sessió clínica es va aconseguir la incorporació de les illes encapsulades a un pacient i una reducció significativa de la dosi diària d'insulina. A més, va passar un mes sense prendre cap injecció. Altres malalties han estat tractades amb èxit mitjançant cèl·lules xenas i al·logèniques. Per exemple, hipoparatiroïdisme, inferioritat hepàtica i renal o dolor.
A aquests resultats cal afegir els avanços en teràpia gènica. En l'actualitat, les cèl·lules poden ser transferides perquè desprenguin el producte biològic desitjat, per a això la porció d'ADN corresponent al producte beneficiós s'estableix en el genoma de les cèl·lules i la cèl·lula que no fluïa res es converteix en la fàbrica del producte. Gràcies a la teràpia gènica i a la lectura del genoma humà, s'analitzaran milers i milers de fragments d'ADN desconeguts i molts es convertiran en receptes de nous productes beneficiosos.

Per exemple, VIII. i IX. factors de coagulació, citocines, factors neurotróficos, etc. S'ha produït durant molt de temps en animals de laboratori després de l'aplicació de microcápsulas als animals. Durant un estudi es van implantar en els ratolins del laboratori les cèl·lules encapsulades que segregaven l'hormona del cultiu. La figura 4 mostra les diferències entre els dos ratolins (control i càpsula). Els resultats són molt esperançadors.
Però la utilitat de l'encapsulació no es limita a les malalties hereditàries. Un dels mals més terribles de l'actualitat, el càncer, ha estat tractat amb èxit en animals de laboratori. Les càpsules utilitzades en aquesta recerca produïen un factor que frena el creixement del càncer. D'altra banda, l'acumulació d'aigua en l'intestí deguda a la inferioritat renal ha estat fàcilment reparada després de l'administració bucal de les càpsules que contenen bacteris. Finalment, moltes malalties degeneratives del sistema nerviós (Alzheimer, Parkinson, Malaltia d'Huntington, etc.) són tractats amb cèl·lules encapsulades, tant en recerques bàsiques com en assajos clínics.
Els investigadors estan investigant noves formes d'administració cel·lular, com la via oral, la via cranial, la subcutània, etc. Encara queda molt per investigar i provar, i queden per fer noves legislacions, però la tecnologia d'encapsulació cel·lular avança dia a dia.
L'ús de les cèl·lules és il·limitat, permet tractar moltes malalties i és segur. En el cas de la teràpia gènica, les cèl·lules poden portar gens de seguretat i gens reguladors. Tot això fa pensar en una tècnica prometedora.
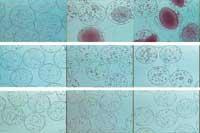
En ella es poden veure 3 tipus de cèl·lules de la mateixa mena de càpsules: hibridomes, fibroblastos i mioblastos. Cada tipus de cèl·lula tindrà una resposta dins de la càpsula. Per exemple, els hibridomes produeixen àrids d'alta densitat cel·lular. Aquesta situació és bastant perjudicial, ja que les cèl·lules sofreixen la falta d'oxigen i moren molt. Els fibroblastos produeixen àrids de menor grandària. No obstant això, estudis realitzats amb animals de laboratori han demostrat que els àrids de fibroblastos poden fer explotar càpsules i causar càncer o tumors. Com es pot apreciar en la figura, els mioblastos no produeixen agregats i es converteixen en una altra mena de cèl·lules sense poder multiplicador. D'aquesta manera, el nombre de cèl·lules no es veu alterat ni existeix risc d'explosió de la càpsula. Per tant, sembla que les cèl·lules més adequades per a encapsular són els mioblastos. (Figura 3. G. Orive Rierol)





