Contra el cáncer, combatiendo la metástasis

¿Y por qué decimos que cuando el cáncer se extiende en el cuerpo no hay nada que hacer? En un principio, una célula se maligna y crece incontroladamente, dando lugar a un tumor primario. En un momento dado, las células que componen el tumor crecen tanto que dejan su órgano original y son capaces de pasar a la circulación. Así, pueden pasar a la sangre y llegar a cualquier parte del cuerpo.
¿Y por qué son tan mortales las células que producen metástasis? Dicen que sólo el 1% de las células que pasan de un tumor primario a circulación son capaces de producir metástasis. En definitiva, estas células son sometidas a una presión selectiva muy elevada y sólo pueden prosperar en condiciones desfavorables.
Para empezar, es una célula muy dura capaz de alejarse de su órgano original y moverse por la sangre. La sangre humana fluye a gran velocidad y sus condiciones físico-químicas son muy inadecuadas para las células externas. Y eso es sólo el principio. Si ha sido capaz de superar este primer shock, el siguiente paso será parar en alguna parte del cuerpo, y teniendo en cuenta la velocidad a la que va la sangre, no es tarea fácil. Por último, cuando se detiene en una parte del cuerpo, sale de la circulación y pasa a otro órgano, tendrá dificultades para crecer en el lugar donde se ha establecido, ya que no es su órgano de origen y para él es un lugar extraño.
Está claro que una célula que consigue superar todos estos obstáculos tiene una enorme capacidad para afrontar cualquier problema. Y, cuando lo consigue, crece y, en ese crecimiento, los tejidos circundantes se van rompiendo y los órganos pierden sus funciones. Así, esta única célula que inicialmente ha superado el control de crecimiento podría llegar a destruir cualquier otro órgano del cuerpo.
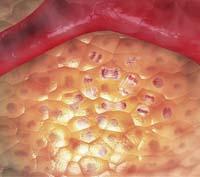
Semilla y tierra
La metástasis, así explicada, es la capacidad de una célula, una vez maleada, para expandirse a través de la sangre a cualquier otro órgano del cuerpo. Pero en este proceso hay más participantes. En 1889, el médico británico Stephan Paget escribió la teoría "Seed and soil". Para Paget, cada célula provoca metástasis en un determinado órgano, es decir, cada semilla (seed) le gusta un suelo concreto (simple).
Y eso está claro; si nos fijamos en los números, veremos que el cáncer de colon se extiende principalmente al hígado, el pulmonar al cerebro, etc. Se sabe que la cercanía también es un factor importante, pero en la actualidad se ha demostrado que el 'diálogo' que se produce entre ambas en cada órgano cuando aparece una determinada célula tumoral es fundamental para el éxito de la metástasis.
Un ejemplo conocido es el caso del cáncer de piel. Se sabe que las células que se forman en el cáncer de piel a menudo producen metástasis hepáticas, siendo especial la relación entre estas células tumorales y las células endoteliales de los sinusoides hepáticos. Las células tumorales de la piel tienen unas moléculas especiales y otras las células endoteliales del hígado, y ambos tipos de moléculas tienen una gran tendencia a asociarse. Por ello, una célula que nace en la piel y que circula por la sangre, puede quedarse en el sinusoide del hígado por su capacidad de adherirse a ella. Sin embargo, la capacidad de "diálogo" de la célula tumoral con las células del órgano en el que se ha implantado no se limita a la mera adhesión, sino que sólo es un principio.
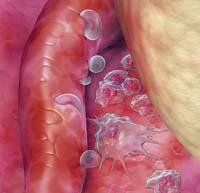
Una vez que ha tenido un contacto inicial, la célula tumoral empieza a enviar órdenes. Las células del órgano donde se ha detenido e implantado la célula tumoral ocupan sustancias que les son enviadas por la célula tumoral y, en muchos casos, las señales que reciben las células del órgano receptor modifican su comportamiento. En muchos casos se produce un proceso inflamatorio en el que aparecen citosina, quimiocina, H 2 O 2 y otras sustancias. Entonces se crea un 'ambiente' en el órgano receptor. Este ambiente se conoce como microambiente tumoral.
Microambiente tumoral
Cuando finalmente el tumor consigue su implantación en otro órgano, el medio que consigue mediante señales enviadas a las células del órgano receptor es sólo un abono para su supervivencia. Por ejemplo, es muy conocida la capacidad de muchas células tumorales de generar el factor VEGF (Vascular Endotheliall Growth Factor). Esta sustancia produce el crecimiento de las células que forman las venas, de forma que, con el tiempo, tras una fase inicial sin oxígeno, la célula tumoral genera a su alrededor unas venas a través de un proceso denominado angiogénesis, que a partir de ahora recibirá oxígeno y nutrientes a través de la sangre.
Sin embargo, cuando se habla de microambiente tumoral se habla más bien del proceso inflamatorio. En este proceso se dan los pasos que se dan en cualquier proceso inflamatorio y las sustancias que se extienden alrededor de la célula tumoral son muy similares a las que se producen en la inflamación. De hecho, estas sustancias son beneficiosas para las células tumorales, lo que favorece el crecimiento de las células tumorales y la aparición de nuevas venas. En definitiva, en este "diálogo" que la célula tumoral ha iniciado con las células del órgano receptor, consigue engañarlas, creando un medio inflamatorio y facilitando el avance del tumor.
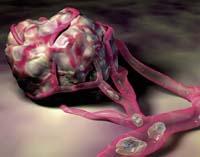
Metástasis
Sobre la teoría del microambiente podemos aprender muchas cosas en la lucha contra la metástasis. Por ejemplo, la estrategia de supervivencia de las células tumorales. De hecho, aunque en un principio residiendo en un medio sin oxígeno --tras su implantación en otro órgano y la destrucción de sus tejidos -, producen venas a largo plazo para facilitar su crecimiento, lo que constituye una estrategia de supervivencia del tumor. Por lo tanto, al cortar esta estrategia, se puede dificultar la capacidad de crecimiento del tumor.
¿Y qué medicamentos podemos utilizar? Pues una molécula que impide la generación de nuevas venas, por ejemplo una molécula que bloquee el factor VEGF. Las células que forman las venas tienen receptores especiales que conocen el VEGF en su membrana y cuando se le une el VEGF envía señales de crecimiento celular a su interior. Si generamos una molécula como la VEGF que se une al receptor pero que no genera señal, el VEGF tendrá un competidor y conseguiremos reducir la capacidad de generar nuevas venas. En consecuencia, el tumor no puede crecer tan fácilmente.
Pero las cosas no son tan fáciles. ¿Qué pasaría si donáramos esta molécula a una mujer que ha tenido una menstruación? Tendría problemas, ya que tras la menstruación es necesario crear nuevas venas. Y si a una persona con problemas cardiacos disminuyéramos su capacidad de generar venas con este medicamento, ¿no pondríamos en peligro su vida?

Otra estrategia para combatir la metástasis es reducir el medio inflamatorio. ¿Y cómo podríamos conseguirlo? Mediante antiinflamatorios. El ácido acetil salicílico es sólo un antiinflamatorio.
Medicamentos contra el cáncer
En el mundo hay miles de investigadores que buscan medicamentos contra el cáncer. ¿Pero algún día se conseguirá tratamiento contra el cáncer? ¿Cuánto tiempo tardará en conseguirlo? Como dice el investigador estadounidense Ishaia Fidler, "algún día conseguiremos que el cáncer se convierta en una enfermedad crónica, pero debemos tener en cuenta que cuando usamos la palabra cáncer hablamos de más de 200 enfermedades". Y así es, hay muchos tipos de cáncer, cualquier célula del cuerpo tiene el riesgo de malignarse y cada célula que se maligna tiene sus propios recursos.
Por ejemplo, cuando se malignan, un hepatocito y un melanocito cutáneo no tienen la misma estrategia de supervivencia y las sustancias químicas que generan no son las mismas, por lo que si queremos destruir estas células, los medicamentos que vamos a diseñar tampoco serán los mismos. Cada cáncer deberá ser tratado con un medicamento específico, no existiendo una respuesta general a una enfermedad tan especializada.
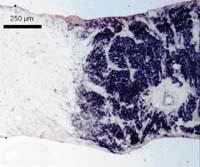
Lo mismo ocurre con la metástasis. Las células causantes de la metástasis han afrontado muchas dificultades. Quien ha conseguido crecer tras superar todas las dificultades ha sufrido una fuerte presión selectiva y una gran capacidad de vida. Por ello, estas células tienen muchas estrategias para vivir ante cualquier dificultad. Si generamos un medicamento bloqueando un receptor concreto para detener el crecimiento de una determinada célula, esta célula tumoral conseguirá reactivarlo a través de otro receptor y logrará crecer como antes, por lo que debemos ir cortando todas sus estrategias.
El tratamiento a desarrollar no sólo será específico para cada tipo de cáncer, sino también variado. En definitiva, se trata de un cóctel de medicamentos en el que cada medicamento corta una determinada estrategia de la célula tumoral. Si algún día conseguimos que el cáncer termine o se haga crónico con medicamentos, la clave será el cóctel de medicamentos, como en otras enfermedades, pero teniendo siempre en cuenta que cada cáncer tiene un origen determinado y que utiliza capacidades y recursos diferentes y que los tratamientos deben ser específicos y no generales.





