La terapia génica desde la esperanza a la realidad
Farmazian doktorea. Biofarmazia, Farmakozinetika eta Farmazia-teknologiako irakasle kolaboratzailea
Farmazia Fakultatea UPV-EHU, Vitoria-Gasteiz

La terapia génica pretende resolver el error de forma radical, ya que utiliza secuencias ADN para transformar células enfermas y conseguir un efecto terapéutico. De esta forma se consigue sintetizar la molécula que las células defectuosas fabricaban.
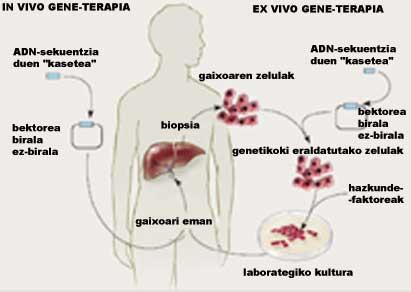
El cambio genético puede realizarse de dos formas. Ex vivo es una terapia que consiste en extraer células al paciente, modificarlas genéticamente en el laboratorio y aplicarlas de nuevo al paciente. En el modo in vivo las células se transforman sin ser extraídas. La figura 1 muestra las principales diferencias entre las dos terapias. Recientemente se ha desarrollado una tercera forma en la que las células universales (que no son del paciente) son modificadas genéticamente y aplicadas al paciente. En este caso, las células se insertan solo o en cápsulas.
Introducción a la terapia génica
La primera sesión clínica de terapia génica la realizó el grupo de Rosenberg en 1990. Los pacientes con cáncer cutáneo muy desarrollado fueron tratados con linfocitos genéticamente modificados. Desde entonces se han puesto en marcha más de 500 sesiones clínicas de terapia génica en todo el mundo. En un principio se trataba de resolver las alteraciones producidas por un único gen, sustituyendo el gen defectuoso por copias sin defectos. Por ejemplo, fibrosis quística, distrofia muscular de Duchenne o hipercolesterolemia familiar. Posteriormente, las células fueron modificadas genéticamente y tratadas enfermedades complejas de origen genético desconocido. Para ello se han utilizado estrategias citotóxicas (causantes de la muerte celular) y citostáticas (que impiden la proliferación celular) como el cáncer o algunos tipos de cardiopatías.

En resumen, a lo largo de estos 10 años las aplicaciones de la terapia génica han crecido de forma constante, al tiempo que se ha hecho un gran esfuerzo en la búsqueda de nuevas vías de aplicación. El objetivo es que estas vías sean más eficientes y menos tóxicas.
Requisitos esenciales de la terapia génica
¿Qué hay que tener en cuenta a la hora de definir la terapia génica? En primer lugar, tres cosas: con qué células o tejidos se va a trabajar, qué estrategia se va a utilizar (ex vivo, in vivo o células universales) y, por supuesto, qué producto (insulina, leptina, factores de coagulación...) quiere que las células las produzcan. La secuencia ADN. Una vez definida y adquirida la secuencia ADN se guarda en un ‘casete’. El ‘casete’ es una secuencia sintética en la que se encuentran los elementos que regulan la representación del ADN.
A continuación se detalla cómo se transportará la secuencia ADN hasta las células defectuosas del enfermo. Generalmente se utilizan vectores. Los vectores son transportadores de genes cuya misión es la transferencia del gen terapéutico a la célula defectuosa y asegurar la correcta expresión del gen. Existen muchos vectores, pero se clasifican en virales y no virales (ver figura 2).
Normalmente los vectores no virales mantienen el ‘casete’ dentro o en superficie. Las más comunes son las formadas por lípidos catiónicos (lipoplexos) y polímeros catiónicos (poliplexos). La mayor parte de ellas producen una baja respuesta immulógica que impide la inflamación del paciente. Sin embargo, los vectores no virales tienen poca efectividad en la transferencia del gen y, además, sólo lo expresan a corto plazo.
Los vectores virales, por su parte, se basan en la capacidad de los virus de llegar a las células y expresar los genes de forma significativa. Los avances científicos han conseguido mejorar sustancialmente la expresión y seguridad de los vectores virales, pero la toxicidad sigue siendo el principal obstáculo a superar por estos vectores.
Por último, se debe definir cómo se insertará el vector en los órganos o tejidos del paciente, es decir, si se realizará mediante jeringuilla, catéter, ... o de otra manera.
Situación actual
Actualmente la terapia génica se aplica en muchas enfermedades. Se han realizado sesiones clínicas en diferentes laboratorios y se ha probado la eficacia y toxicidad de la terapia génica en humanos. A la vista de los avances de la última década se puede afirmar que la terapia génica tiene un gran futuro, siempre y cuando se respeten las enfermedades y los pacientes. La Fundación Marcelino Botin organizó un seminario sobre el presente y futuro de la terapia génica en la Universidad Internacional Menéndez Pelayo, en el que se mostraron algunos ejemplos de los avances mencionados. Diabetes, hemofilia, enfermedades cutáneas, cáncer, alteraciones de las células sanguíneas, etc. se presentaron estrategias de tratamiento mediante terapia génica.
Los investigadores reunidos en Santander determinaron las condiciones para poder aplicar la tecnología de terapia génica. En primer lugar, la transferencia adecuada de la secuencia ADN a las células enfermas es imprescindible, así como la indicación del producto a largo plazo. Al mismo tiempo, se debe reducir al máximo la toxicidad de estos sistemas para evitar efectos secundarios adversos. Si se quiere trabajar con células que se van a implantar en animales o personas, es necesario encontrar buenos sistemas de cultivo en el laboratorio y procedimientos de trasplante adecuados y seguros.
Grupos del proyecto de Biología Molecular, Celular y Terapia Génica de Ciemat, Jose L. Bajo la dirección de Jorcano, utiliza la terapia génica para regenerar la epidermis y presenta sus resultados en Santander. Se pretende conseguir una piel artificial útil para pacientes con quemaduras, psoriasis o úlceras crónicas. Para ello se ha contado con la estrategia in vivo y han creado una piel que trabaja como bioreactor a través de la liberación de sustancias beneficiosas.
La hemofilia también despierta gran interés entre los investigadores. Gonzalo Hortelano, profesor de la Universidad Canadiense de McMaster, utiliza la terapia génica para combatir la hemofilia. Los pacientes con hemofilia fluyen pocos IX factores sanguíneos. El profesor Hortelano ha modificado genéticamente algunas células para que fluyan este factor y las ha introducido en microcápsulas. Por el momento sólo los ha probado con ratones de laboratorio, pero espera iniciar sesiones clínicas a medio plazo. Katherine A. El grupo de High utiliza vectores virales para el tratamiento de la hemofilia. Recientemente se han iniciado sesiones clínicas para analizar la eficacia y toxicidad de esta estrategia en los seres humanos. Según el Dr. High, los buenos resultados preliminares permiten que los primeros productos de terapia génica estén preparados en 2004.
Sin duda, el cáncer es la enfermedad que más sesiones de terapia génica ha impulsado. En el año 2000 se aprobaron en Estados Unidos más de 300 protocolos. Pero es tan grande como el interés que despierta la complejidad del cáncer. En el proceso de creación del tumor intervienen muchos genes y hay que tener en cuenta muchos factores.
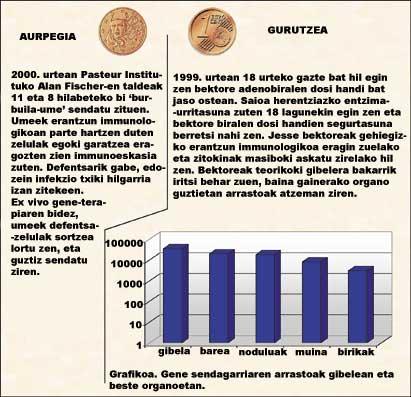
En general, los resultados de la terapia génica son positivos, pero no tan espectaculares como se pensaba al principio. Por tanto, procede analizar las dos caras de la moneda (ver figura 3). El mayor éxito lo obtuvo el Instituto Pasteur el año pasado, cuando curó ‘niños de burbujas’ mediante un programa ex vivo. Fue la primera vez que se curaba totalmente una patología mediante terapia génica. Desgraciadamente, en la cruz de la moneda se encuentra la muerte del joven Jesse. Falleció en 1999 en un intento clínico de prueba de adenobirus.
Obstáculos y futuro

Antes de llegar a los hospitales, la terapia génica debe superar una serie de obstáculos.
La mayoría de los investigadores consideran que las mayores dificultades son las tecnológicas. En este sentido, es evidente la necesidad de optimizar los tres componentes básicos de la terapia génica: Secuencia de ADN, vectores y vía de administración. Los genetistas han descubierto las bases genéticas de enfermedades causadas por un único gen o por un grupo de genes. Los vectores, tanto virales como no virales, son cada vez más eficientes y muestran seguridad a largo plazo. Es posible que en estos años se haya producido un menor desarrollo de la vía de tratamiento debido a la gran cantidad de factores tecnológicos y biofarmacéuticos a tener en cuenta para lograr una correcta obtención.
La transformación de los principios activos en dosis seguras y efectivas ha sido siempre uno de los objetivos fundamentales de la investigación farmacéutica. Parece, por tanto, razonable pensar que aumentarán los esfuerzos que las instituciones públicas y las empresas privadas realizan en este campo. De hecho, la expectativa de uso de la terapia génica depende en gran medida de la correcta administración de las dosis. Para ello será necesario que investigadores de diferentes áreas coordinen sus esfuerzos.
Como se ha visto, la terapia génica tiene más requerimientos que otras terapias, y las responsabilidades éticas también son mayores. La seguridad de los pacientes que participan en las sesiones clínicas no puede verse en ningún caso comprometida por los patrocinadores o por las expectativas creadas. Los investigadores deben dejar claro que la terapia génica está en desarrollo y que no curará muchas enfermedades antes de la próxima década. Además, es fundamental que los pacientes, sus familias y las organizaciones reguladoras conozcan con precisión los beneficios y riesgos potenciales de la terapia génica experimental.
Sin embargo, este enfoque realista no debe debilitar la ilusión por la terapia génica. La terapia génica y otras alternativas prometedoras como las células madre se encuentran en una fase inicial. Al contrario de lo que se hizo con la terapia con medicamentos, los avances se están realizando respetando el punto de vista científico y no probando los medicamentos con los pacientes y viendo su efecto. Es sin duda la mejor garantía de un futuro próspero.
Naturaleza del vector | Ventajas | Molestias |
BIRALA | BIRALA | VIRAL |
Adenobirus | VIRAL | VIRALA |
BIRALA | VIRALA | VIRAL Baja |
NO | NO | NO-VIRAL |
Opiniones punteras
¿Por qué optaron por investigar en terapia génica?
J.L.J. : Por un lado, porque se trata de un área de investigación prometedora y por tanto, de investigación. Por otro lado, al ser un laboratorio que realizamos la investigación básica de la piel, nos resultaba fácil realizar la parte terapéutica de la investigación y decidimos intentarlo.

S.W. : Porque la terapia génica es un tema científico apasionante que acaba de nacer y estamos en etapas preliminares. Las bases científicas y clínicas de la terapia génica son fecundantes y la utilización de nuestro material genético para tratar enfermedades hace una estrategia muy poderosa. Por estas razones estamos desarrollando la tecnología de liberación de genes en células y tejidos adecuados.
G.H. : Terapia génica XXI. Creo que va a desempeñar un papel importante en la medicina del siglo XX. En estos momentos es un tema científico incipiente y me parece muy atractivo participar en el desarrollo de este campo de investigación en la medida de lo posible.
¿Qué ofrece la terapia génica sin otros tratamientos?
J.L.J. : La terapia génica ofrece una alternativa a las enfermedades. Aborda la enfermedad desde un punto de vista científico y no como se ha hecho con los medicamentos ortodoxos, probando y observando los resultados. La terapia génica se basa en un conocimiento científico más profundo, en el conocimiento de los genes relacionados con las enfermedades y pretende utilizarlos para curarlos. Pero ha sido más complicado de lo que inicialmente se pensaba.
S.W. : La terapia génica tiene una ventaja importante que la diferencia de otras terapias. Otros métodos terapéuticos, como la cirugía, radiaciones, medicamentos, etc. están diseñados para extirpar una enfermedad o una función corporal. La terapia génica, en cambio, suministra el cuerpo, le da una sustancia que no tenía. En el caso de una enfermedad genética, la aplicación de un gen sin defectos permite curar la enfermedad. Este tipo de tratamientos también pueden aplicarse a otras patologías como el cáncer o el sida.
G.H. : Es cierto que la farmacología tradicional lleva décadas preparando fármacos eficaces para modificar determinadas funciones fisiológicas. Pero la terapia génica ofrece la posibilidad de administrar medicamentos de forma continua y constante. Los medicamentos tradicionales no pueden proporcionar esta estabilidad crítica en muchos procesos fisiológicos. Además, en algunos casos sólo es teraupeutico cuando el producto está dentro de las células, no en sangre. Entonces, los medicamentos no siempre son efectivos. Por otra parte, el uso de material genético abre las puertas a nuevas alternativas, como la posibilidad de generar nuevas respuestas inmunológicas en el cuerpo. Por último, y especialmente en el caso de las enfermedades crónicas, la terapia génica puede reducir considerablemente el coste de los tratamientos. En el caso de la hemofilia, por ejemplo, se espera que un único tratamiento de terapia génica sustituya a las inyecciones actuales. Ahora el paciente debe inyectarse varias veces por semana a lo largo de toda la vida.

¿Cuáles son los principales obstáculos que debe superar la terapia génica? ¿Tecnológicas? ¿Biológicos? ¿Éticas?
J.L.J. : Yo no creo que haya obstáculos éticos. Hay que tener en cuenta la ética, pero cambia de persona a persona. Por ejemplo, la ética del paciente es diferente de la del investigador, y la del investigador y la del periodista. Con ello no quiero despreciar a nadie, sino decir que la ética es importante y a tener en cuenta en nuestra sociedad. Pero hoy en día nuestros problemas son tecnológicos, no éticos. Los vectores para la introducción de genes terapéuticos en las células no son tan perfectos como queríamos y las enfermedades son mucho más complejas de lo que pensamos. Sabemos demasiado poco y de momento sólo podemos curar enfermedades causadas por un único gen defectuoso. Pero en la mayoría de las enfermedades intervienen muchos genes, donde predomina el desconocimiento.
S.W. : Desde el punto de vista tecnológico, el principal inconveniente es la especificidad, es decir, cómo liberar selectivamente el gen en la célula deseada. El control de la actividad del gen también es muy importante. Queremos que el gen se exprese de forma que se produzca un efecto terapéutico y evitar los efectos nocivos. Por otro lado, es importante investigar qué enfermedades se pueden curar mediante terapia génica y cuáles no. Desde el punto de vista ético, la comunidad científica tiene muy claro que lo utilizará para curar la terapia génica, no para mejorar al hombre. La terapia génica es una estrategia para tratar enfermedades, no una técnica para estimular las habilidades de una persona.
G.H. : Creo que las mayores dificultades técnicas están relacionadas con los vectores. El vector opcional debe garantizar la seguridad del paciente y tener una eficacia terapéutica en este orden, además de permitir su reemisión. Por otra parte, considero que la gran variabilidad de una persona a otra es un factor a tener en cuenta. Adelanto que el éxito de la terapia génica se limitará al principio a unas pocas enfermedades. Posteriormente se irá extendiendo progresivamente.
¿Las grandes expectativas generadas por la terapia génica han beneficiado o perjudicado vuestro trabajo?

J.L.J. : A mí no me han influido nada, pero es cierto que ocurre muchas veces y, por ejemplo, lo que viven en el genoma. En estos momentos la biología ha recogido conocimientos suficientes para pasar de ser ciencia básica a ciencia aplicada, es decir, antes nos acercábamos a estudiar a biología, pero ahora queremos sacarle partido a ella. La terapia génica y la genómica han nacido de este cambio y las percibimos como una aplicación. En el caso de la terapia génica la idea es bastante sencilla. Pretendemos conocer las bases moleculares de las enfermedades e identificar los genes defectuosos para su posterior curación.
Tenemos medios y capacidad para hacerlo todo en el laboratorio, pero todo ha sido más complicado de lo que pensamos al principio. Y por tanto, hemos pasado de la cima del optimismo a la presión de las expectativas. Pero la realidad está a medio camino. La terapia génica ha dado buenos resultados en los últimos años y gracias a ello sabemos que los objetivos no son imposibles, pero tampoco fáciles. La cuestión es que la biología es ciencia aplicada. Hay gente que vende ideas y se está enriqueciendo en 24 horas y de ahí surgen las expectativas.
S.W. : Creo que la pesimismo apareció sobre todo hace dos años, cuando murió un paciente en una sesión clínica. Fue entonces cuando surgió la mala imagen de la peligrosa terapia génica. En consecuencia, investigadores y responsables de la regulación de las sesiones clínicas volvieron atrás y revisaron exhaustivamente todos los protocolos. El incidente ha hecho que los requisitos para iniciar una sesión clínica sean mayores y el control sea mucho más estricto. La muerte de hace dos años fue trágica, pero aprendimos mucho.
G.H. : Yo creo que le ha hecho daño. Han despertado falsas expectativas entre enfermos y familiares y el mismo sentimiento se ha extendido a toda la sociedad. En este ambiente de calidez se han iniciado numerosas sesiones clínicas, aunque algunas con escasa base científica. Como consecuencia, muchas sesiones han fallado. A la vista de estos resultados desalentadores, se ha puesto más énfasis en aumentar los conocimientos básicos de terapia génica y se han obtenido los primeros resultados esperanzadores.
Gorka Orive Arroyo





