Aditivos alimentarios

Desde que entramos en la Unión Económica Europea, nuestra legislación alimentaria ha ido ajustándose, destacando la composición y etiquetado de los conservantes. El Real Decreto 2058, de 12 de agosto de 1982, regula las etiquetas, etc., exigiendo que el punto 8.10 indique los aditivos alimentarios; para los que se utilizan en la CE con el símbolo E... o para los que aún no tienen número admitido mediante el símbolo H...
La definición de los aditivos se puede hacer de muchas maneras y utilizaremos uno de los más adecuados para cada caso. Las sustancias añadidas a los alimentos por el aditivo son no nutritivas. Las cantidades añadidas son muy pequeñas, casi infinitesimales y su objetivo no es otro que la remodelación o mejora de la elaboración y conservación de algunas de las características organolépticas de los alimentos y/o bebidas.
Desde siempre se han utilizado aditivos como sal, azúcar, alcohol, maceración, colorantes... Los aditivos son sustancias químicas cuyo origen puede ser natural o sintético. Añadimos aditivos a los alimentos para retrasar la descomposición de la comida, cambiar el sabor, etc. En general, los aditivos naturales pueden considerarse más adecuados que los sintéticos, aunque sólo se diferencien si son tóxicos o no por los organismos.
Los aditivos no deben mezclarse con contaminantes como el dioxano plaguicida, los plaguicidas que se añaden a las plantas de tomate o los que causaron el síndrome tóxico de los aceites de colza. Por supuesto, los efectos de los restos de sustancias químicas utilizadas como plaguicidas en nuestros cuerpos, debido a su carácter acumulativo, pueden ser muy notorios. En consecuencia, los plaguicidas no se consideran aditivos sino contaminantes.
Desde el punto de vista químico, se puede plantear de forma sencilla qué son los aditivos; el alimento en sí mismo sufre cambios morfoestructurales a lo largo del tiempo, que son reflejo de algunos cambios químicos y reacciones químicas. Por tanto, para comprender el comportamiento de los aditivos en la conservación de los alimentos y defender sus opiniones científicas al respecto, se analizarán los procesos que se producen de forma espontánea en los alimentos.
Degradación de los alimentos. Agentes
Existen tres tipos de agentes: agentes físicos (congelación, presión mecánica, luz, calor...), químicos (no enzimáticos, entre los que se pueden citar el ungulado, el proceso de entumecimiento y el proceso de remate; y enzimáticos) y vivos (insectos, roedores, microbios,...)

Se pueden utilizar diferentes técnicas o procesos de conservación de alimentos, como el calentamiento, la refrigeración, el secado, etc., o compuestos químicos (naturales o sintéticos) llamados aditivos a los que se añaden de forma apropiada, como los famosos E-... Estas últimas presentan alguna especificidad para algunas reacciones químicas que se producen de forma espontánea.
Los alimentos están basados en compuestos químicos, como glúcidos, lípidos y protidos. Los glúcidos, lípidos y protésidos son componentes de los alimentos, constituidos por diferentes compuestos químicos, tales como hidratos de carbono, ácidos grasos y sus ésteres glicéridos (grasas y aceites), y las proteínas están formadas por aminoácidos, respectivamente. En los alimentos hay más compuestos, como vitaminas, oligoelementos, etc. Pero dado que los que hemos mencionado anteriormente son los más numerosos, los analizaremos a continuación. Todo ello lo explicamos en el número doble 85-86 de esta revista.
Procesos o técnicas físicas empleadas en conservación (congelación, calentamiento, etc.) son bien conocidos aunque no sepamos con exactitud la complejidad y la explicación técnica (por ejemplo, no son necesarios), los abandonamos y nos limitaremos a los cambios químicos.
Los procesos químicos que se producen en los alimentos, fundamentalmente reacciones químicas, son procesos cinéticos, por lo que a mayor temperatura, mayor velocidad de reacción. Como consecuencia, en general, en verano la comida se pudre más rápido que en invierno.
Cambios químicos en los alimentos
Proceso de arrastre
Esto es consecuencia de un conjunto de reacciones complejas que tienen lugar en ciertos alimentos, quedando al descubierto pigmentos negros o pardos. También se producen compuestos volátiles que alteran el olor y el sabor. A menudo dichos efectos y reacciones se utilizan intencionadamente, por ejemplo en el caso de la cerveza o el queso.

Sin mencionar cuál es el proceso concreto, hay que decir que el calor (la temperatura) tiene una gran importancia e influencia. Por ello, en los alimentos que se obtienen mediante técnicas a altas temperaturas (pasteurización, ebullición, etc.), como las leches condensadas o el zumo de los frutos, está presente un enorme riesgo de ardor.
Desde el punto de vista químico, el proceso de envejecimiento está relacionado principalmente con el grupo carbonílico (C=O) de azúcares y vitaminas. El proceso enzimático de arrastre es, en general, el que se realiza en los compuestos fenólicos y está influenciado directamente por la luz y el calor. Un ejemplo es el que aparece a corto plazo tras cortar la patata, la manzana o el plátano.
Estos grupos fenólicos se oxidan con oxígeno, luz y metales (también por sus enzimas) y como consecuencia de la reacción aparecen polímeros denominados melaninas. En los alimentos de origen animal no se lleva a cabo el proceso de remate, sino que es habitual en las frutas y hortalizas y se acelera cuando se produce un proceso de manipulación o un golpe.
Los frutos ácidos, como los cítricos, no contienen enzimas oxidantes. En limón, naranja, piña, etc. no se realiza el proceso de atención. En otras ocasiones, los sustratos químicos y las enzimas pueden estar colocados en diferentes microcélulas, y si al adquirirlas se produce un golpe y se rompe la membrana, se producirá el proceso de arrastre (golpear una manzana y ver qué pasa! ).
Sin embargo, los polímeros coloreados denominados melaninas, crean una membrana protectora que impide la entrada de microorganismos posteriores. Este fenómeno se puede observar al cortar el plátano.
Proceso de Minado
A continuación se analiza químicamente el proceso de irritación de los alimentos. De hecho, el proceso de membrana es sólo una transformación química de los compuestos lípidos, que puede ser un proceso hidrolítico o una oxidación normal. Por tanto, se producirá en alimentos grasos como aceites y grasas. El producto de reacción se caracteriza por compuestos químicos de mal olor y sabor tan conocidos.

En el denominado proceso hidrolítico o lipolítico se rompe el enlace éster de los lípidos. La velocidad de esta reacción depende principalmente del calor y de la catálisis enzimática.
Recordar que los ácidos grasos son ácidos carboxílicos de cadena alifática larga y que el doble enlace C=C separa los aceites y grasas de la cadena.
En reacciones de saponificación, muy conocidas para los químicos, se generan moléculas de ésteres y agua. Cinéticamente analizada en condiciones estándar de laboratorio es muy lenta, pero en la naturaleza gracias a las enzimas es muy rápida.
El proceso inverso de este equilibrio es conocido por completo, la hidrólisis de los ésteres, y es un proceso muy lento incluso estudiado cinéticamente. Sin embargo, las catalizadas por enzimas (proteínas) son mucho más ligeras. No hay que olvidar que en estos procesos cinéticos la temperatura influye muchísimo. Estimamos que al pasar la temperatura de 25ºC a 100ºC, la velocidad de reacción aumenta aproximadamente 50 veces. Por tanto, como es fácil de entender, es un factor a tener en cuenta en la elaboración de productos lácteos.
Esta hidrólisis es frecuente en las mantequillas. El sabor picante y el olor que desecha es debido al ácido butírico.

Los productos de reacción son ácidos grasos que, lógicamente, acidificarán el pH en la medida en que son ácidos y que, junto con su olor, alterarán sus características organolépticas. Por lo tanto, no es casualidad que para minimizar el contenido de ácidos grasos, el refino del aceite utilizado para la alimentación se realice.
Aunque lo dicho hasta ahora ha sido por el proceso hidrolítico de la membrana, existe un proceso oxidante de membrana que se lleva a cabo gracias al oxígeno en el aire que oxida los ácidos grasos insaturados. Es más, si en lugar de combinar estos ácidos grasos insaturados (es decir, compuestos triglezíridos) están libres, su autooxidación es más rápida. De hecho, este proceso es una polimerización radical (que no analizaremos químicamente).
El calor, la luz, los metales y las radiaciones ionizantes como los truenos son catalizadores. Como producto de reacción tenemos de todo: ácidos grasos de cadena alifática corta, aldehídos, ésteres, peróxidos, cetonas... Algunas de estas sustancias pueden ser tóxicas por lo que no se utilizan aceites/grasas picantes.
Antioxidantes
Para evitar la oxidación de los lípidos se añaden a los alimentos sustancias antioxidantes. Su objetivo puede ser eliminar los radicales libres o eliminar los peróxidos. Sin embargo, deben cumplir una serie de requisitos: no ser tóxico, no dar gustos, olores y colores, actuar en cantidades muy pequeñas y, por supuesto, ser solubles en grasas.
Entre los antioxidantes naturales destacan los tocoferoles (vitamina E). Entre los antioxidantes sintéticos, los más utilizados son el BHA (butilhidroxianisol) y el BHT (butilhidroxitolueno). El humo de la madera, al contener compuestos fenólicos, parece presentar comportamientos protectores.
Antes de seguir adelante, explicaremos los conceptos básicos de los microbios y de los cambios microbiológicos, ya que es difícil comprender el crecimiento poblacional microbiano y su dependencia de la concentración, temperatura, pH, humedad y oxígeno, como el enfriamiento (su efecto en la estructura celular), la congelación (ligera o lenta) y la desecación (solar, industrial, liofilizada).
Cambios microbiológicos en los alimentos
Plantearemos este tema de forma somera y ágil para facilitar la comprensión tanto de las técnicas experimentales como de los comportamientos de algunos aditivos utilizados en la conservación.
Los microorganismos, al igual que nosotros, son heterótrofos, por lo que nos enfrentamos entre sí. Es decir, la comida de estos microorganismos es la nuestra. Como nosotros, los microorganismos también deben comer para satisfacer todas las funciones energéticas, plásticas y químicas. Además, no podemos olvidar que algunos de los microorganismos pueden ser patógenos, como la salmonella. Los microorganismos o microorganismos pueden ser: (con núcleo separado, como protozoos, hongos, algas...) y microorganismos procarioóticos (con núcleo indiferenciado, como bacterias, cianofas...).

Los responsables de los cambios en los alimentos son principalmente bacterias y hongos. El crecimiento poblacional de estos microorganismos es exponencial, es decir, de una célula se generan otras dos nuevas, cada una de ellas generará otras dos, etc. La población de bacterias en menos horas puede ser de un millón. Las técnicas o procedimientos utilizados en conservación consisten en la interrupción o inertización del proceso de crecimiento de estos microorganismos.
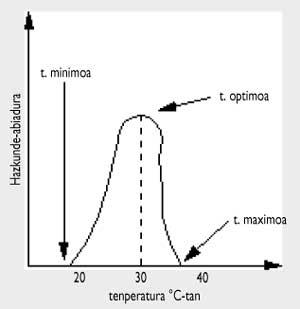
Como se puede observar en la figura adjunta, la temperatura influye enormemente en el crecimiento de los microorganismos.
La máxima velocidad de crecimiento se produce a temperatura óptima. Si durante un período de tiempo calentamos el alimento por encima de la temperatura máxima, los microorganismos morirán. En eso consiste la técnica de calentamiento para la conservación. Por debajo de la temperatura mínima la mayoría de las bacterias se “congelan”, es decir, no mueren, pero no se reproducen.
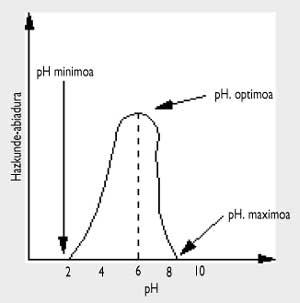
En la figura adjunta se puede observar que la acidez o pH también es importante. En general, tanto los mohos como las levaduras pueden soportar un pH más ácido, mientras que cuando el pH<4,5 las bacterias no atacarán. Algunos alimentos son muy ácidos, como las frutas, y otros pueden conservarse añadiendo vinagre.
El componente básico de los microorganismos es el agua, que sin ella muere, por lo que no hay crecimiento. En el caso de la temperatura y el pH, por cada microorganismo existe una actividad máxima (aw), mínima y óptima del agua, donde la máxima actividad del agua, la presión de vapor del agua en disolución es dividida por la presión de vapor del agua pura.
La mayoría de las bacterias no pueden crecer en un medio con una actividad máxima de agua inferior a 0,90, por lo que en base a esta propiedad en la conservación de los alimentos se utilizan técnicas como la reducción del agua (por sublimación o evaporación), la congelación y la reducción de la velocidad máxima mediante la disolución de la sal o el azúcar.
Aditivos o aditivos
Como se ha mencionado al principio, el objetivo de este artículo no ha sido explicar las técnicas experimentales de conservación, sino explicar los aditivos o aditivos utilizados para la conservación de los alimentos y comentar sus causas.
De lo dicho hasta ahora se deduce fácilmente que los alimentos se “pudren” o se descomponen, es decir, que se producen unas reacciones químicas en su interior y que el crecimiento de microorganismos puede ser evidente. Por lo tanto, se pueden utilizar procedimientos o técnicas que permitan la máxima conservación de los alimentos, entre las que se encuentran los aditivos o aditivos químicos.
Los aditivos son sustancias químicas que se añaden intencionadamente a los alimentos y que modifican, modifican o estabilizan las características organolépticas de la comida. En sentido estricto, el azúcar, la sal, el vinagre, etc. que se utilizan en conservas, aunque pueden ser considerados aditivos, los consideramos como conservantes químicos. Es decir, las sustancias que no alteran las características organolépticas de los alimentos, pero también retrasan o eliminan la presencia microbiana, se denominarán conservantes.
Como se ha indicado anteriormente, cualquier aditivo debe estar autorizado. La lista de aditivos utilizada en España incluye colorantes; conservantes; antioxidantes y sinérgicos; emulsificantes, estabilizantes, espesantes y gelificantes; acidificantes y correctores de la acidez; antimalutantes; potenciadores del sabor; espumantes; edulcorantes artificiales; almidones modificados; gasificantes y otros.
En lugar de hacer una descripción de cada aditivo, se agrupará esta lista larga y se indicarán las características químicas más importantes del conjunto.
Colorantes
Se utilizan para colorear y/o decorar los alimentos. Son aditivos desde el E-100 hasta el E-175. De hecho, los colorantes no tienen ningún interés ni tecnológico ni fisiológico, y su uso se centra en la demanda de los consumidores. Algunos técnicos consideran los colorantes como el mejor ejemplo de aditivos superfluos, ya que sólo cambian su apariencia.
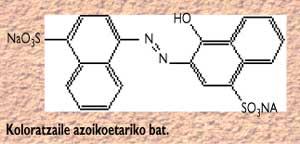
En general, se dice que los colorantes naturales y sus derivados (como carotenoides, xantofilas, clorofilas) no son tóxicos, mientras que los sintéticos, sobre todo los colorantes azoicos (E-102, E-105, E-110, ...) pueden producir efectos secundarios. La estructura química de un colorante azoico es la siguiente:
Se trata de las líneas de ferrocarril que se dirigen a la calle San Martín. Los más utilizados son el ácido bencónico (E-210), el sórbico (E-200), el acético (E-260) y el propónico (E-280) y sus sales y nitritos, nitratos y sulfitos.
Ácido benzoico y sus derivados (E-214, 215...) (conocidos como parabenos) son probablemente los más utilizados, y su estructura es la siguiente:
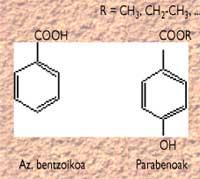
El efecto antimicrobial se debe a las especies no disociadas de todos estos ácidos, por lo que son efectivas en pH ácidos (entre 2,5 y 4,0). No son tóxicos en las concentraciones habituales empleadas en conservación. Sin embargo, no son muy adecuados para nuestro organismo en concentraciones elevadas, por lo que puede ocurrir que el ácido salicílico que antes se utilizaba (que puede considerarse como un derivado del bencónico) era tóxico y que hoy en día no se utiliza prácticamente si no se conserva en casa.
El ácido acético CH3-COOH, es decir, el vinagre, es muy utilizado. Las sales sódicas y potásicas de nitritos y nitratos (del E-249 al E-252) se utilizan en productos cárnicos, principalmente embutidos. El trabajo de estas sales es triple: por un lado, desarrollan un color especial en la formación de nitrosilmioglobina, por otro, evitan el crecimiento del Clostridium botulinum y, por último, dan al sabor un “indicio” especial.
Antioxidantes y sinérgicos
Su objetivo es impedir los procesos de oxidación que se producen en productos grasos o oleosos.
Los más utilizados son el BHA (E-320) y el butilhidroxitolueno BHT (E-321), cuya estructura es la siguiente:
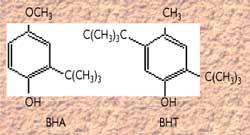
En este anillo la presencia del grupo hidroxílico es importante ya que es un donante de hidrógeno. No son tóxicos ni dan sabor especial.
Algunos antioxidantes, como el sulfito y el óxido de azufre (del E-220 al E-226), también tienen propiedades conservadoras y son muy utilizados en la elaboración de vinos.
Emulsionantes, estabilizadores, espesantes y gelificantes
Muchos de los alimentos, como la leche o el huevo (la yema), son sistemas dispersos por naturaleza, es decir, están colocados en dos fases inmiscibles como el aceite y el agua. Como no podía ser de otra manera, existen sustancias químicas especiales que disminuyen la tensión superficial del agua y muchas que se homogeneizan ambas fases. Estas sustancias se denominan surfactantes, emulsionantes, tensoactivos, etc.
La estructura química de estos tensoactivos o emulsificantes es muy similar en la mayoría de los casos; la cadena alifática hidrocarbonada, soluble en la fase orgánica y frecuentemente denominada hidrófobo o lipofílico, y el extremo iónico soluble en la fase acuosa, también conocido como hidrófilo.

El uso industrial de los emulsificantes se aplica frecuentemente a la emulsión agua/aceite, como helados, mayonesa, margarinas. La propia leche y otros alimentos contienen este tipo de emulsificantes, como la lecitina, el colesterol.
En panadería se conoce la propiedad del almidón de cristalizar. Por tanto, en este tipo de “geles” (mezclas) se utilizan moléculas denominadas gelificantes, como estearil-2- lactilato sódico (E-481). Este aditivo reduce la velocidad de endurecimiento del pan.
La acción de los fosfatos (E-450) es múltiple, ya que estabilizan las emulsiones, son amortiguadores al pH y pueden ser hidratantes captando agua. Los más utilizados son los hidrogenofosfatos (Na2HPO4), dihidrogenofosfatos (NaH2PO4), polifosfatos, hexametafosfato sódico (Na6P6O24), pirofosfato sódico (Na4P2O7). Son muy utilizados en productos de carnicería.
Acidificantes y correctores de acidez
Los ácidos utilizados en los alimentos, como el fumarico (E-296; E-297), el acético (E-260), el adípico (E-355), el fosfórico (E-338), el cítrico, etc., también pueden considerarse conservadores. La fuente de la mayor parte de los ácidos es natural (manzana, plátano, zanahoria...) y además de ser conservantes, son amortiguadores al pH y sinérgicos a los antioxidantes. Probablemente el ácido cítrico sea el más común y utilizado.
Todos los ácidos dan un sabor especial y claro a la comida. Estos acidificantes no son tóxicos.
Otros
La elaboración de alimentos, además de los ya mencionados, suele utilizar muchos otros aditivos. Su función y función, por decirlo de alguna manera, ha sido “decorar el producto” o elegirlo. Entre ellos se encuentran los aromatizantes (E-620 a E-637) que permiten recuperar el sabor que han perdido los alimentos por procesos industriales. Los aromatizantes pueden ser sintéticos o naturales.
Adicionalmente, la industria utiliza aditivos como antienlazantes o antimalutantes (del E-535 al E-573), almidones (del H-4381 al H-4394) o edulcorantes.