Buriles, tortugas gigantes e hidra inmortal
¿Envejecimiento, escrito en genes?

Aunque sólo a los datos anteriores parece existir un "programa" de envejecimiento en los genes, hay otros factores a tener en cuenta. De hecho, si el envejecimiento sólo dependería de los genes, los gemelos monocigóticos, que tienen el mismo material genético, deberían tener el mismo proceso de envejecimiento. Esto no es así, ya que en el desarrollo del feto, en la infancia y a lo largo de toda la vida influyen múltiples factores como la alimentación y las condiciones ambientales. Además, aunque en el xixare C. elegans se han conseguido mutaciones que pueden alargar la vida, no se ha conseguido frenar totalmente el proceso de envejecimiento mediante mutaciones genéticas.
Aplicando la asignatura de Darwin
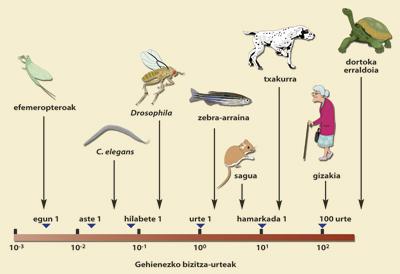
Cuando Charles Darwin publicó en 1859 On the Origin of Species by Means of Natural Selection, sacudió las bases de la biología de entonces para sentar nuevas bases. En la actualidad, la idea de que la selección natural es la esencia de la evolución de las especies está ampliamente extendida, pero ¿se puede explicar el proceso de envejecimiento a la luz de la selección natural? Hemos visto que es imposible explicar que sólo desde el punto de vista de los genes, no se puede decir que haya un programa de envejecimiento, pero sí que hay genes relacionados con el envejecimiento. Entonces podemos intentar aplicar la asignatura de Darwin para explicar este proceso. Pero si la naturaleza elige mutaciones beneficiosas para la vida, ¿cómo es posible que haya genes que llevan al envejecimiento y que la selección natural no los excluya?
Hay dos grandes teorías para explicarlo. La primera es la teoría de la congestión, presentada por Medawar en 1952. Según esta teoría, las mutaciones que provocan las consecuencias más negativas del envejecimiento escapan a la selección natural, ya que sólo afectan a la parte final de la vida. Dado el escaso número de individuos que han llegado a este punto en la historia de las especies, estas mutaciones han quedado fuera de la presión evolutiva, pero a la vez se han ido acumulando generación tras generación en el genoma de las especies.
La segunda teoría se llama pleiotropía antagonística y atribuye la responsabilidad del envejecimiento a unos genes especiales. Según esta teoría, algunos genes, llamados pleiotrópicos, tienen un doble efecto. Por un lado, son beneficiosos en la juventud y, por ello, son elegidos por la selección natural. Sin embargo, en la vejez influyen negativamente en la supervivencia de los individuos. Como la selección natural tiene cada vez menos fuerza a medida que avanza la vida, hay menos individuos y la reproducción es menor, el efecto positivo de la juventud tiene más fuerza que los efectos negativos de la vejez. Esta teoría fue presentada por George Williams en 1957 y desde entonces se han propuesto varios genes para demostrar la pleiotropía antagonística.

Sin embargo, al igual que en el caso de la congestión de mutaciones, no hay pruebas concluyentes, y aunque ambas teorías pueden explicar la aparición y persistencia de ciertos genes especiales, no pueden explicar todo el proceso de envejecimiento.
Un problema de optimización
Si el envejecimiento no está programado en los genes y no podemos explicarlo totalmente a través de la evolución, ¿por qué ocurre? Se trata de la teoría del some de usar y tirar teorías que armonizan de alguna manera las explicaciones vistas hasta ahora. La base de esta teoría es la separación entre el some y el germen. En un organismo, el germen es el conjunto de células reproductoras y no diferenciadas precursoras de las mismas, y el resto de células forman el soma. De alguna manera, el germen sería inmortal, porque permanece de generación en generación, mientras que el soma sería desechable, diferente en cada generación.
Los organismos deben utilizar los recursos disponibles para su supervivencia y reproducción. De hecho, el desarrollo, mantenimiento y reparación de los somas requieren una gran cantidad de energía. Pero la reproducción también requiere una gran cantidad de energía, y la energía destinada a la reproducción no puede dirigirse a la vigilancia del some. Entonces, ¿hasta qué punto merece la pena asignar energía para mantener el soma en buen estado, al margen de otros procesos como la reproducción?

Según la teoría del some desechable, los organismos deben estar en buen estado fisiológico mientras tienen la posibilidad de sobrevivir en la naturaleza y con ese fin realizan la asignación de recursos. Se puede observar como un problema de optimización: con una cantidad limitada de energía es necesario cumplir una serie de requisitos (crecer, mantener el soma, reproducirse, etc.).
En lo que respecta al mantenimiento del soma, no tiene sentido abusar de ella la energía, siendo limitada su supervivencia en la vida salvaje. Un claro ejemplo de ello son los ratones salvajes. El 90% de ellos muere antes de los 10 meses de su nacimiento, normalmente en frío. De esta forma, los ratones utilizarán una gran cantidad de energía para la termogénesis (generación de calor) y la reproducción, si bien esto permite una menor cantidad de energía para el mantenimiento del soma. Y es precisamente esta energía limitada la que provoca el envejecimiento, ya que los daños que se producen en el soman no se reparan adecuadamente.
Los salmones del Pacífico son un ejemplo extremo del some de usar y tirar. Desde su nacimiento en los ríos del Pacífico Norte crecen y obtienen los recursos necesarios para su reproducción. Cuando están en el océano, una señal les dice que es hora de reproducirse y todos los recursos se destinan a ello. Cuando se produce la puesta cerca de los nacederos de los ríos, éstos mueren sin excepción. Soma desechable, germen inmortal.
Más cerca: células y biología molecular en el envejecimiento
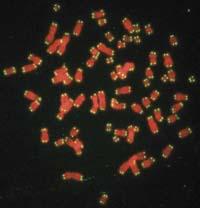
Hasta ahora, para entender el envejecimiento, hemos observado la selección natural y el organismo como sistemas completos. Pero muchos investigadores han tomado como punto de partida otro punto de vista: las células aisladas y sus mecanismos moleculares internos. En este campo se considera que los telómeros que forman los bordes de los cromosomas (del griego, telo : "último", mero : "parte") tienen gran importancia. Cada telómero está formado por secuencias repetitivas de ADN, cuya función principal es proteger los cromosomas. Cada vez que una célula se divide por mitosis, los telómeros se acortan. Cuando llegan a una longitud crítica, las células entran en estado de senescencia, es decir, no mueren del todo (apoptosis), pero dejan de fragmentarse. Esta situación se produce tras aproximadamente 50 divisiones. Entonces, ¿qué pasaría si en cada división los telómeros mantuvieran su longitud? Es lo que ocurre en la mayoría de las células cancerosas gracias a la enzima llamada telomerasa. A través de la generación de mucha más telomerasa que las células convencionales, las células cancerígenas son capaces de evitar la reducción de los telómeros y de hacerlos inmortales.
Si la telomerasia puede evitar la reducción de los telómeros, ¿no sería ésta una vía para alargar la vida? Para demostrarlo se han utilizado ratones transgénicos, cuya actividad era alta. Los resultados muestran, sin embargo, un ligero aumento de la supervivencia, pero también un aumento del riesgo de cáncer. No es de extrañar, ya que, como hemos explicado, la telomerasa es uno de los mecanismos que utilizan las células cancerígenas para hacerlas inmortales.
Se sabe que al envejecimiento los tejidos pierden su capacidad de regeneración, y está claro que en esta pérdida de funciones, además de los telómeros, las células madre también tienen mucho que decir. En los mamíferos, las células madre adultas se encuentran en diferentes órganos (cerebro, corazón, piel, hígado, etc.) y se pueden distinguir en distintos tipos de células. De este modo, son capaces de asegurar el mantenimiento del organismo y responder a los daños. Con el envejecimiento estas capacidades disminuyen, pero aún no sabemos exactamente por qué. Las hipótesis principales son el envejecimiento natural de las células madre (por medio de la reducción de los telómeros) o la dificultad de su función como consecuencia del tejido envejecido. El mejor conocimiento de estos mecanismos puede hacer posible el uso de estas células para curar enfermedades derivadas del envejecimiento.

Programada para sobrevivir
Todos los organismos (¡o casi todos!) el envejecimiento y la muerte pueden hacer pensar en un programa genético. Sin embargo, desde una perspectiva amplia de los mecanismos del envejecimiento se puede afirmar que no es así. La consecuencia es muy distinta: el envejecimiento es el resultado de vivir. En otro orden de cosas, se puede decir que la vida se mantiene al margen del equilibrio termodinámico. El mantenimiento del soma requiere un esfuerzo constante y el germen es más importante en la selección natural. Por tanto, la segunda ley de la termodinámica, que impulsa el aumento de la entropía del sistema, lleva al organismo al envejecimiento de los programas de supervivencia.
Ha apostado por una estrategia de uso y desecho de las selecciones naturales en todas las especies. Es una apuesta de gran sentido, porque ¿para qué gastar demasiado energía en mantener el soma si cualquier accidente, cualquier depredador, en cualquier momento puede acabar con ese individuo? Mejor repartir la inversión: parte de la energía para mantener el soma en estado de bala durante un tiempo y otra parte para mantener el germen para siempre. ¿Y entonces cuál es la diferencia entre las gijeras, las tortugas gigantes y el resto de especies? Es sólo una diferencia proporcional de gastos. Es decir, cuanta energía puede invertir cada cual y invierte en mantener, crecer, reproducirse y en el resto de procesos necesarios para vivir.
¿Y hidra? Como ocurre en la ciencia, cada respuesta abre nuevas puertas...





