Miúdo cheiro a molécula!

O olfacto é, sen dúbida, o sentido máis sensible e é especial, xa que o epitelio olfativo está formado por simples terminacións nerviosas. Isto non ocorre con outras sensacións (excepto a dor), xa que normalmente un transductor actúa como amortiguador entre o mundo exterior e o sistema nervioso.
A través do olfacto, o sistema nervioso está directamente relacionado co mundo exterior. Basicamente, o cerebro está visible no nariz, o que indica que o olfacto é o máis antigo e primitivo dos sentidos. O olfacto está, ademais, moi relacionado pola proximidade física dos seus centros de procesamiento con polo menos una das partes máis primitivas do cerebro: o sistema límbico, o centro de control das emocións. Isto pode explicar o forte impacto do olfacto e ás veces a causa do inconsciente.
Nas seguintes liñas falaremos sobre a química da sensación. Todas as sensacións son, en definitiva, químicas, xa que toda a actividade neuronal do noso cerebro baséase no transporte de moléculas e iones e nas reaccións nas que interveñen. Algunhas mensaxes que os seres vivos recibimos do mundo exterior dependen da percepción de certas moléculas que actúan como mensaxeiras. O olfacto é un exemplo de quimiorecición.


Aquí non quero explicar a complexa fisiología do olfacto, nin a relación entre a estrutura molecular e o olfacto. O obxectivo deste traballo é analizar que compostos producen cheiros coñecidos paira todos.
Cando as moléculas aromáticas se evaporan no aire, chegan á medula dos nosos orificios nasais e disólvense nela. A continuación, os nervios olfativos envían impulsos nerviosos ao cerebro, o que provoca una sensación ás veces positiva e ás veces negativa.
Vivimos rodeados de moléculas e non debemos temer. Respiramos, comemos, bebemos, cheiramos, excretamos ou vestimos moléculas, e aínda así só coñecemos a uns poucos. Algúns son moi complexos estruturalmente e outros moi simples, pero a súa influencia nos seres non está en absoluto relacionada coa complexidade da estrutura.
Una molécula

Toda a materia de todo o mundo, ben sexa un anaco de roca, unha árbore, un pito ou un Rolex, está composta por un tecido de sustancias simples chamadas elementos químicos. Entre eles atópanse o hidróxeno, o carbono, o osíxeno ou o cobre.
A parte máis pequena dun posible elemento é o átomo (do grego, atomos, incortable). Parte dun elemento puro, como un anaco de ouro, é só un conxunto de átomos. Os átomos son moi pequenos. O diámetro dun átomo de carbono é de 0,00000000015 metros (1,5 x 10 -10 m), polo que una liña de carbono de 1,5 cm de lonxitude aproximada é: ) é dun centenar de millóns de átomos de calcaria desde o bordo até o bordo, e dun millón de átomos ou indirectos. No po máis pequeno que podemos ver hai máis átomos na nosa galaxia que estrelas.
Moitos compostos están formados por moléculas. A molécula é una combinación específica de dúas ou máis átomos que se unen nunha determinada disposición xeométrica. Aínda que na natureza hai máis de cen átomos, todas as moléculas que se describen a continuación son combinacións de até cinco átomos de hidróxeno, carbono, nitróxeno, osíxeno e xofre. Vexamos agora o aspecto que adoitan ter as moléculas que nos introducen nas nosas fosas nasais e que nos producen sensacións.
Cheiros bos...

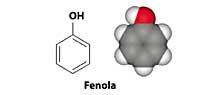
Un cheiro pode producir recordos, ás veces positivos e ás veces negativos. Moitas persoas teñen recordos da súa infancia, por exemplo, ao cheirar o fenol (C 6 H 6 Ou), “porque cheira a pinturas de uso escolar.”
Cando falamos de cheiros agradables, moitas veces véñennos á cabeza os perfumes. De feito, os perfumes fabrícanse paira iso, paira fascinar á xente co pracer do olfacto.
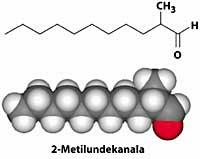
2-O metatardecano (C 12 H 24 Ou) é a molécula principal da fragrancia Channel N> 5, presentada por Coco Channel en 1921. Con este perfume, a industria do perfume comezou a utilizar por primeira vez compostos sintéticos para que os perfumes chegasen a todo o mundo.
Os químicos dedicados á perfumaría utilizan unha linguaxe única paira describir os seus logros: "Paco Rabanne pour home nace paira lembrar un paseo de verán con aire fresco polos outeiros da Provence; cheiros herbáceos, romeu e tomiño; e frescura brillante mesturándose co frío vento mariño e o cálido aire dos Alpes. Paira lograr o efecto necesario, o perfumista mesturou os aceites de herba con toques de madeira e o aroma químico do dimetilheptanol, de forma que a súa frescura penetrante pero indefinible lembra ao aire exterior ou ao liño recentemente lavado". (J. Ayres, Chemistry and Industry , 1988, 579).
O contido en fragrancia dos perfumes redúcese ao 5-10%, mentres que o resto adoita ser xeralmente una mestura etanol/auga (90:10). Por tanto, na industria do perfume requírese una gran cantidade de etanol e, como pode pensarse, non tanto de compostos aromáticos. A produción anual de diversas fragrancias importantes, como a do xasmín, adoita roldar as 10.000 toneladas. E os ingredientes puros paira perfumaría como Cis -Jasmona (C 11 H 16Ou, principal compoñente do xasmín) custan centos de euros por gramo.
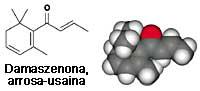

Damaszenona (C 13 H 18 Ou) é a principal responsable do cheiro a rosa. Con todo, se abrimos a botella e metemos o nariz, levarémonos un desencanto duro, xa que ten un cheiro similar ao camforra ou a trementina. Pero á mañá seguinte, nós e as roupas que nos vestían darannos un cheiro a rosa que se desenvolve con dilución.
Nos aceites vexetais esenciais abundan os compostos aromáticos da familia dos terpenos, que provocan a case todos sensacións agradables como o alcanforra (C 10 H 16 Ou), o mentol (C 10 H 20 Ou) e o geraniola (C 10 H 18 Ou). Os dous primeiros, ben coñecidos, utilízanse en produtos Reflex ou Vicks VapoRub, xerando en xeral una agradable sensación de frescura. A segunda, como se pode deducir do nome, atópase no geranio e participa no seu cheiro.
...e malos cheiros
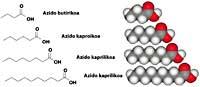
O noso cheiro a suor débese, en gran parte, a uns ácidos carboxílicos de cadea curta e media (compostos con grupo COOH).
O ácido formado por catro átomos de carbono, CH 3 (CH 2 ) 2 COOH, é o principal responsable do cheiro a manteiga minada e coñécese como acedo butírico ( butirum , latín, manteiga). Este composto é moi común no vómito e na suor dos pés. Non nos equivocamos ao cheiro a suor dos pés cando o chamamos cheiro a queixo, xa que nalgúns queixos de forte cheiro hai ese mesmo composto. Segundo un estudo estadounidense, a percepción do cheiro deste composto varía moito segundo o contexto. Normalmente, o cheiro do butírico provoca una reacción desagradable na xente, pero si dicir que pensan sobre a comida, o cheiro faise máis agradable.

Os ácidos caprílico, caprílico e caprino teñen 6, 8 e 10 átomos de carbono respectivamente, e son líquidos aceitosos con cheiro a cabra ( caper , latín, cabra). Ademais das cabras, as persoas segregamos estes compostos (uns máis que outros) e forman parte do cheiro de nosa axila. Os cans poden coñecer o cheiro a suor do seu dono polo seu contido en ácido carboxílico.
Os homes e as mulleres gastamos cada ano grandes cantidades de diñeiro en xabóns, xeles e desodorizantes que evitan estes cheiros, xa que o cheiro a cabra é antiestético e antisocial paira nós. É curioso que os mesmos compostos malolientes gastemos aínda máis paira reproducirse no noso corpo, xa que o ácido caproílico, caprílico e caprílico atópanse na maioría dos perfumes e aceites esenciais.
O amoníaco, NH 3, é un gas picante incoloro e inflamable en condicións normais. Moi soluble en auga, inflúe no seu cheiro xa que se disolve facilmente na mucosa acuosa que cobre o epitelio olfativo nasal. O cheiro da auga sería probablemente tan picante como o amoníaco se os nosos órganos dos sentidos non estivesen tan afeitos a el.
O Camembert ou Brie humedecido tamén cheiran ao amoníaco, gas que se forma a medida que se descompoñen as proteínas nitrogenadas. Debemos agradecer aos microbios o cheiro que adoita existir nos cantóns das rúas dos nosos pobos os domingos pola mañá, xa que co seu traballo, a urea que a xente deixou alí a véspera coa mellor vontade, é dicir, o principal compoñente dos ouriños, convértese en amoníaco.
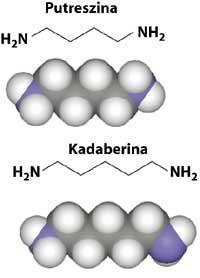
O cheiro a carne podrecida lémbranos ás aminas, derivados orgánicos do amoníaco. As aminas conservan a granularidad do amoníaco, pero moitas veces dunha maneira máis transformada e inagradable. No caso da putrescina (C 4 H 12 N 2) e a cadabina (C 5 H 14 N 2), o propio nome dános una idea bastante clara do seu cheiro. Ademais de ser os principais responsables do cheiro a carne podrecida, participan en menor proporción nos cheiros do seme e os ouriños, así como na respiración.
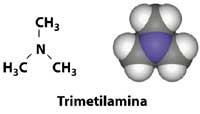
A próxima vez que cheiramos peixe podrecido, deberiamos pensar en trimetilamina, a molécula que teremos no interior do nariz. Este composto despréndese da degradación encimática das proteínas de peixe. Os cans de casa tamén teñen ás veces cheiro a peixe, xa que poden desprenderse desta amina. A enfermidade denominada trimetilaminurea, máis frecuente nas mulleres que nos homes, débese a unha encima defectuosa que provoca a degradación das proteínas e que segrega este composto de cheiro a peixe na suor.
Á vista de todos estes exemplos, parece que sabemos ben que moléculas producen o sinal que chega ao noso cerebro cada vez que cheiramos una flor ou un café recentemente feito. Agora, lamentablemente, aínda estamos moi lonxe de comprender que pasa na nosa mente, como responden as nosas emocións ou en que consiste o noso pracer, aínda que os avances da ciencia sexan cada vez máis emocionantes.


Xofre, rei de malos cheiros
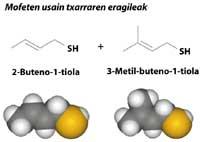

En canto aos malos cheiros, moitos dos derivados do xofre non quedan atrás. Por exemplo, o cheiro do spray que segrega o mofet é una mestura de dúas tioles, os derivados de xofre con grupo SH.
Pero, ao parecer, o peor de todos os cheiros é o que provocou a evacuación da cidade de Freiburg en 1889, segundo os alí presentes. Durante a realización dun ensaio de obtención de tioacetona mediante o cracking da tritioacetona, constituíuse un "cheiro ofensivo que se repartiu rapidamente a gran parte do pobo" que provocou mareos, vómitos e evacuación ao carbón. Por suposto, suspendéronse os traballos de laboratorio.
Os traballadores dun laboratorio de investigación Esso, quizais cunha gran valentía, repiten o mesmo experimento ao sur de Oxford en 1967. A pesar de que o tapón dunha botella de residuos saltou por accidente e pechouse inmediatamente, non transcorreu moito tempo ata que os membros que estaban a traballar no outro edificio, situado a uns douscentos metros, queixáronse polo botijo e o malestar.
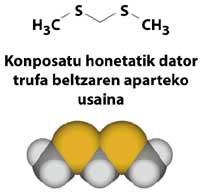
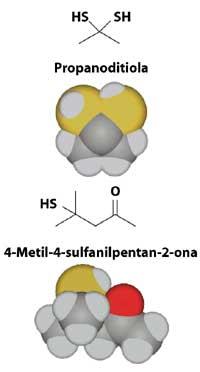
Só uno destes dous compostos parece ser responsable deste insoportable cheiro: propanoditiola ou 4-metil-4-sulfanilpentan-2-ona. Seguramente pasará moito tempo ata que alguén teña a valentía de resolver ese debate.
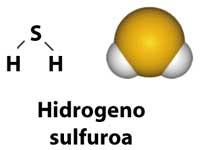
O sulfuro de hidróxeno, H 2 S, pode considerarse como un xofre análogo á auga. No centro ten un átomo de xofre en lugar do de osíxeno. Con todo, esta simple substitución leva diferenzas notables, non o penses.
O sulfuro de hidróxeno é un gas venenoso con cheiros irritantes. O cheiro característico dos ovos podrecidos débese a el e, en menor concentración, ao agradable cheiro dos ovos recentemente cocidos.

Quen coma algunha vez Aza xa saberá (tanto el como os demais) que o cheiro a sulfuro de hidróxeno non é broma. As follas de col son ricas en aminoácidos con xofre, e cando se descompoñen por bacterias do intestino groso, libérase gas H2S, entre outros. Iso, claro, salgue por detrás.
Os cheiros molestos teñen os seus usos. Ao gas que chega aos nosos fogares a través do tubo engádenselle derivados de xofre como ter-butiltiol (CH3)3CSH a baixas concentracións, xa que o propio gas non ten ningún cheiro e pola contra non poderiamos detectar fugas de gas. Por concentración baixa, enténdese que é realmente baixa; os seres humanos podemos detectar una parte de 50.000.000.000 de gases naturais.
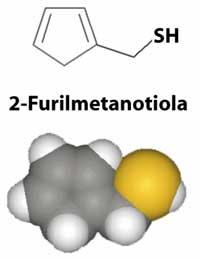
Con todo, non pensedes que todos os derivados de xofre teñen cheiros asquerosos. Paira deshonrar a honra destes compostos hai que mencionar o prezado cheiro da trufa que os porcos poden atopar baixo o chan a un metro de profundidade, que polo seu excelente cheiro e sabor véndese máis caro que o ouro. O agradable cheiro do café recentemente feito débese tamén a un derivado de xofre, 2-furilmetanotiol (C 5 H 6 VOS).
Máis información
- Atkins, P. Atkins' Molecules Cambridge University Press Cambridge, UK. 2003. Clayden, J., N. Greeves, Warren S. and Wothers, P. Organic Chemistry Oxford University Press, Oxford, UK. 2001. Meierhenrich, U. J. Golebiowski, J., Fernández, X., and Cabrol-Bass, D. Angew Chem. Int. Ed. 43, 6410-6412. 2004 Chemical Engineering News October 11, 11. 2004