Esperança a l'oblit de l'Alzheimer
L'Alzheimer és el tipus de demència degenerativa més freqüent. És suportat per persones de la tercera edat i atenta a les funcions d'intel·ligència dificultant les activitats diàries. El mal és persistent i progressiu, limitant amb el temps l'autonomia del pacient. Finalment, com a conseqüència dels danys causats als òrgans necessaris per a la vida, el malalt porta a la mort.
Desgraciadament, avui dia no hi ha manera de curar l'Alzheimer. Els tractaments farmacològics i no farmacològics utilitzats només serveixen per a reduir l'evolució de la malaltia i millorar la qualitat de vida del pacient i el seu entorn.
Ara, no obstant això, el fàrmac experimental Aducanumab obre les seves portes a l'esperança de trobar un tractament que pugui curar definitivament l'Alzheimer.
Sobre l'origen de l'Alzheimer
Encara que l'origen de l'Alzheimer encara no és clar, la hipòtesi del b-amiloide (bA) es considera la principal raó. Segons això, l'acumulació de proteïnes bA al cap produeix unes plaques extracelul·lars i internes que són tòxiques per al cervell. Això és probablement pel fet que el cos produeix aquesta proteïna de manera desproporcionada o no pot ser eliminada.
Un factor important de risc per a l'Alzheimer és el genètic. Sembla ser que en el gen de l'apolipoproteïna E del cromosoma 19 es troba un dels orígens de la malaltia, ja que el seu quart al·lel (ApoE4) es relaciona amb la producció de A. < Però hi ha altres factors de risc associats a l'aparició d'aquesta mena de plaques en el cervell, com l'edat, l'estil de vida portat, l'abús d'antiinflamatoris o l'alumini.
Aducanumab
El fàrmac aducanumab va ser desenvolupat per l'associació americana Biogen. Es tracta d'un anticòs humà monoclonal selectiu tipus IgG1, oposat a l'A < (Figura 1). La part variable del fàrmac és l'obtinguda a partir de la rata i la part fixa l'obtinguda d'un pacient que va sofrir un cas especialment prolongat d'Alzheimer. El primer atacarà a l'antigen (en aquest cas a l'A), < mentre que la part d'origen humà servirà per a evitar que el pacient sofreixi rebutjos del sistema immunitari.
Segons els científics, encara que l'Alzheimer es diagnostica en el moment de l'aparició dels símptomes, les plaques de porten < anys emmagatzemant-se en el cervell del pacient. Per això creuen que totes les proves realitzades fins al moment amb pacients amb Alzheimer molt desenvolupat han fallat. Ara, no obstant això, s'estan realitzant nous assajos clínics amb pacients amb baix i mig grau de malaltia, com els que s'estan realitzant amb aducanumab. El fàrmac encara està en desenvolupament, però els creadors han demostrat que elimina les plaques < A del cervell d'aquests pacients. Si les recerques són reeixides en el futur, l'objectiu dels assajos és detectar les plaques molt primerenc i que el metge pugui prescriure-les com qualsevol altre medicament.
Primers resultats
Fa dos anys Biogen va posar en marxa l'assaig clínic de la fase 1b denominat PREVALGUI. Durant un any, les injeccions mensuals d'aducanumab s'administraven als participants i van voler conèixer la seva eficàcia, seguretat i farmacocinètica.
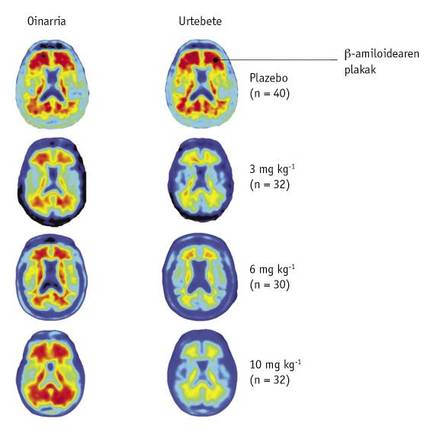
Per a això van participar 165 pacients, alguns amb placebo i uns altres amb diferents dosis de fàrmac (1, 3, 6 o 10 mg/kg). La influència dels duaners es va mesurar mitjançant la Tomografia d'Emissió de Positrons (PET).
Passat un any, es van comparar les imatges PET dels pacients amb la referència prèvia al tractament. En aquesta comparació, els científics van observar que la disminució dels nivells d'A < se veia clarament en funció de la dosi del fàrmac (Figura 2). Les imatges mostraven a més que aquest descens es va produir en totes les parts del cervell.
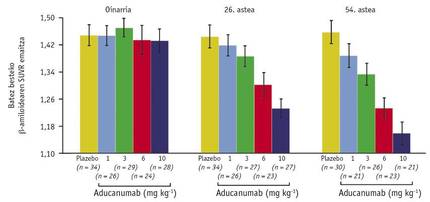
Així mateix, un altre dels resultats obtinguts amb aquest escàner va llançar una nova satisfacció: l'escala entre la dosi utilitzada i la quantitat mitjana d'en < el cervell (Figura 3). A través d'ella es van poder comparar els nivells de de les < setmanes 26 i 54 amb la referència i van concloure que l'efecte del fàrmac depèn del temps i de la dosi. Aquest descobriment pot considerar-se històric, ja que fa pensar que per primera vegada es pot curar la malaltia de l'Alzheimer. I per si tot això fos poc, els pacients que van rebre una dosi de 10m/kg en la Setmana 54, tenien un nivell d'1.16<molt pròxim al límit d'1.10 que discrimina resultats positius i negatius.
També es van emprar els mètodes denominats “Mini Mental State Examination (MMSE)” i “Clinical Dementia Ràting (CDR)”, dos mètodes de puntuació utilitzats per a detectar, registrar i analitzar les evolucions de les deterioracions cognitives. En aquests mètodes el pacient ha d'emplenar un qüestionari i depenent de la puntuació obtinguda, el metge és conscient del grau de demència del pacient. El temps de resposta a totes les preguntes oscil·la entre els 5 i els 10 minuts, per la qual cosa són freqüents les anàlisis dels nivells de demència. En utilitzar MMSE i CDR en aquesta fase 1b, van poder comprovar que la disminució dels nivells de reporta < beneficis.
Des del punt de vista de la seguretat Aducanumab, pot considerar-se un fàrmac bastant segur. Els efectes adversos més freqüents van ser mal de cap, infecció d'orina, infecció del tracte respiratori i els denominats ÀRIA (Amyloid-Related Imaging Abnormalities). Aquestes últimes són anomalies oposades en les imatges per ressonància magnètica, causades per edemes, microhemorragias i siderosis. Encara que els pacients que van sofrir tots aquests efectes adversos van ser tractats en urgències, ningú ha estat hospitalitzat. Tampoc va haver-hi morts.
Finalment, la farmacocinètica duanera (concentració màxima i superfície sota la corba normal) va ser lineal a dosi en totes les persones tractades. La semi-vida biològica en plasma és de vint-i-un dies. D'altra banda, l'anticòs contra aducanumab només va desenvolupar el 3% del total de pacients. I com la influència dels anticossos va ser transitòria i a través dels títols mínims d'anticòs, van concloure que no afecten la farmacocinètica i seguretat de les aducanumas.
Per a donar continuïtat a aquests resultats es van posar en marxa les tres fases de l'assaig clínic.
Fases finals de les sessions clíniques
La tercera i última fase de l'assaig clínic es denomina EMERGEIX i ENGAGE. Van començar en 2015 i duraran set anys. El seu objectiu és comprovar les troballes de la fase 1b i continuar amb l'estudi de l'eficàcia i seguretat dels aducanumab en persones amb un grau d'Alzheimer baix i mitjà.
Per a això, realitzaran sessions amb 3.000 pacients procedents de 400 hospitals de tot el món. Però no serveix perquè qualsevol pacient pugui participar en la recerca. El pacient haurà de complir una sèrie de criteris per a poder participar en les proves: Que l'escàner PET tingui un resultat positiu de A, < permetre la identificació del genotip ApoE4, una puntuació entre 24 i 30 en el mètode MMSE i un resultat de 0,5 en el mètode CDR, entre altres. Els pacients amb història clínica d'angina inestable o infart de miocardi, anèmia o malaltia crònica hepàtica o renal no podran participar en les proves.
En aquesta fase, com en l'anterior, s'injectaran als pacients diferents dosis d'anticòs una vegada al mes i l'any 2022 es compararan els resultats de PET, CDR i MMSE amb el placebo.
Seguiment des de farmàcia
Igual que qualsevol altre fàrmac, també podem realitzar un seguiment farmacoterapèutic des de la farmàcia amb aducanumab.
Es tracta d'un servei ofert en l'oficina de farmàcia que té com a objectiu millorar la qualitat de vida del pacient. Per a això es pretén augmentar l'eficàcia i seguretat dels tractaments del pacient, reduint els riscos associats a l'ús de medicaments. El seguiment farmacoterapèutic es realitza seguint una metodologia o sistemàtica concreta, per a això és imprescindible la incorporació d'un farmacèutic a l'equip sanitari multidisciplinari que atén el pacient.
Per a poder dur a terme el servei és necessari mantenir entrevistes periòdiques en la farmàcia amb el pacient o el seu cuidador. I en aquestes entrevistes podem adonar-nos dels petits problemes de salut que l'aducanumab pot ocasionar al pacient. Cal tenir en compte que els pacients amb Alzheimer són persones majors i pacients amb múltiples tractaments farmacològics, la qual cosa augmenta considerablement el risc de nous problemes de salut. Això pot provocar efectes perniciosos dels aducanumab per l'efecte directe del propi fàrmac o per la interacció amb altres medicaments. Una vegada deixats registrats aquests problemes de salut detectats en la farmàcia, es comunicarien al metge que participa en l'assaig clínic. També ens posaríem en contacte amb el metge de capçalera si es considera necessari. Per a finalitzar el cicle, en sortir els pacients de la consulta mèdica, es definiria una data per a una nova entrevista.
Així, els farmacèutics podem participar i col·laborar en aquesta tercera fase de l'assaig perquè l'aducanumab sigui el medicament definitiu contra l'Alzheimer en el futur.
Finalment, cal esmentar que aquestes reunions en farmàcia serviran per a continuar fent un seguiment farmacocinètic al pacient en el futur. A més de tota la informació que tinguem registrada, les relacions amb el pacient i amb metges de diferents àmbits seran més estretes, sempre en benefici del pacient.








